Sepsis ve Septik fiok
advertisement

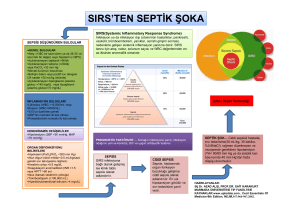
‹.Ü. Cerrahpafla T›p Fakültesi Sürekli T›p E¤itimi Etkinlikleri Ak›lc› Antibiyotik Kullan›m› ve Eriflkinde Toplumdan Edinilmifl Enfeksiyonlar Sempozyum Dizisi No: 31 • Kas›m 2002; s. 131-140 Sepsis ve Septik fiok Uz. Dr. Gökhan Aygün Sepsis; enfeksiyona karşı gelişen sistemik inflamatuvar yanıtı tanımlamaktadır. Hayatı tehdit eden bir enfeksiyondur ve Yoğun Bakım Ünitelerinde (YBÜ) ölümlerin en önemli nedenidir. Hızlı, uygun ve yoğun bir tedavi yaklaşımı mortaliteyi azaltabilecek en önemli unsurdur. Klinik bulguların çeşitliliği ve farklı klinik seyir nedeniyle tanıda gecikmeler sıklıkla yaşanmaktadır. Klinik tabloyu tanımlamak ve ortak bir terminoloji geliştirebilmek için yapılan çalışmalar sonucunda sepsis kliniğini tanımlayan ve derecelendiren bir uzlaşı sağlanmış ve kullanılmaya başlanmıştır. Bu uzlaşı raporunda kabul edilen tanımlar şu şekildedir: Enfeksiyon: Mikroorganizmaların varlığına karşı ortaya çıkan inflamatuar yanıt ya da steril konak dokusunda mikroorganizmaların invazyonunu gösteren durum. Bakteriyemi: Kanda canlı bakteri bulunması. Sistemik ‹nflamatuar Yan›t Sendromu (SIRS): Farklı klinik uyarılara karşı konakta gelişen yanıtı tanımlar. Aşağıdaki bulgulardan en az ikisinin varlığı ile tanımlanır: • Vücut ısısı > 38 °C ya da < 36°C • Kalp hızı > 90 vuru/dakika • Solunum hızı > 20/dakika ya da PaCO2 < 32 mmHg • Lökosit sayısı > 12.000/mm3 ya da < 4000/mm3 ya da > %10 genç nötrofillerin saptanması Sepsis: Sistemik inflamatuar yanıt sendromu ile birlikte klinik veya mikrobiyolojik olarak dökümante enfeksiyonun varlığı. A¤›r Sepsis: Organ disfonksiyonları, hipoperfüzyon ve hipotansiyon ile birlikte görülen sepsis. Perfüzyon bozuklukları; laktik asidoz, oligüri ya da mental durumdaki bozulmayı içermektedir. Hipotansiyon sistolik kan basın- 131 • Gökhan Aygün cının < 90 mmHg ya da hipotansiyona yol açabilecek bilinen başka bir neden yokken başlangıçtakinden > 40 mmHg düşme görülmesiyle tanımlanmaktadır. Septik fiok: Yeterli sıvı tedavisine rağmen hipotansiyon ve perfüzyon bozukluklarıyla seyreden sepsis. İnotropik ya da vazoaktif ilaç verilen hastalar perfüzyon anormallikleri saptandığında hipotansif olmayabilirler fakat yine de septik şok olarak kabul edilmelidirler. Multi Organ Yetmezli¤i Sendromu: Akut olarak hastalananlarda girişim yapılmadan homeostaz sağlanamayacak ölçüde organ işlev bozukluklarını tanımlar. Unutulmamalıdır ki bu konsensus kriterleri özellikle epidemiyolojik çalışmaları standardize edebilmek amacıyla oluşturulmuştur ve klinikte sepsis tanısı için çok uygun bir yaklaşım olarak düşünülmemelidir. Kriterler hem pekçok enfeksiyon ve enfeksiyon dışı klinik tabloda oluşabilirler hem de sepsis kliniği çok farklı bir seyir izleyebilir. Pankreatit, multitravma, doku yaralanmaları, hemorajik şok, iskemi gibi klinik durumlar ve tümör nekroz faktör (TNF), sitokinler gibi inflamatuar mediyatörlerin dışarıdan verilmesi SIRS tablosunu ortaya çıkarabilir. Klinik olarak sepsisin ayrımında kliniğin ilerleyici karakteri önemli bir noktadır. Açıklanamayan klinik değişikliklerde sepsisi hatırlamak ve araştırmak akılcı bir yaklaşımdır. Klinik tablo sepsisten septik şoka ve multiorgan yetmezliği tablosuna doğru ilerledikçe mortalite de belirgin olarak artmaktadır. Klinikte; ateş/hipotermi, açıklanamayan taşikardi ya da taşipne, periferik vazodilatasyon bulguları, açıklanamayan şok, mental durumda bozulma sepsisi akla getirmelidir. Lökositoz ya da lökopeni, açıklanamayan laktik asidoz, renal ya da hepatik fonksiyonlarda açıklanamayan değişiklikler, trombositopeni ya da yaygın damariçi pıhtılaşma (DIC), artmış oksijen tüketimi, düşük sistemik vasküler direnç/artmış kardiak atım da sepsisi düşündürmelidir. Bazen prokalsitoninde, sitokinlerde ya da C reaktif protein (CRP) seviyelerinde belirgin artış sepsisle ilişkili olabilmektedir. Her sepsis olgusunda hemokültürde üreme olması gerekmez. Hemokültürde üreme olması ile tablonun ağırlığı arasında bir ilişki olmadığı bilinmelidir. EP‹DEM‹YOLOJ‹ Sepsis, Amerika Birleşik Devletleri’nde yaklaşık yılda 500.000 olgu olarak bildirilen ve ortalama mortalitesi %10-90 bulunan bir enfeksiyondur. Mortalite altta yatan hastalık, enfeksiyon etkeni, enfeksiyona yanıt yeteneği, uygun antimikrobiyal tedavi ve septik şok gelişim süreciyle ilgilidir. Ülkemizde sepsis olgularının sayısı konusunda yeterli bir bilgi yoktur. Hem çok farklı klinik tablolara yol açması hem de bildirimi zorunlu olmaması nedeniyle belirlenen- 132 Sepsis ve Septik fiok • den daha sık bir enfeksiyon olduğu söylenebilir. En sık üriner sistem (ürosepsis), solunum sistemi enfeksiyonları, deri enfeksiyonları ve varlığında damariçi kateterler önemli sepsis kaynaklarıdır. Sepsise zemin hazırlayan durumlar şöyle sıralanabilir: • İmmun sistemde eksiklik (immunsupresyon, nötropeni, uç yaşlar, ...) • Altta yatan hastalıklar (Diabet, siroz, renal yetmezlik, ...) • Majör cerrahi • Yabancı cisim varlığı (İdrar kateteri, damar-içi kateter, ...) • Tıkayıcı bir oluşum (Renal taş, safra kesesi taşı, ileus, ...) • Steroid tedavisi • Kemoterapi • Daha önce antibiyotik kullanımı Yaşlı hastalar, enfeksiyonlara fizyolojik cevap oluşturabilme rezervleri daha kısıtlı olduğundan sepsise daha yatkın hastalardır. Ayrıca yaşlı hastalarda sepsis sıklıkla atipik ya da nonspesifik bir klinik tablo ile meydana çıkabilir. ETYOLOJ‹ Gram negatif, Gram pozitif ya da funguslarla oluşan enfeksiyonlarda klinik tablo aynıdır. Etkenler hastanın hastanede yatıyor olup olmaması, yaşı, altta yatan hastalığı gibi birçok faktöre bağlı olarak değişiklik gösterebilir. Toplum kökenli sepsislerde genelde en sık rastlanan etkenler; Escherichia coli, Streptococcus pneumoniae, Staphylococcus aureus’dur. Hastane kaynaklı sepsislerde ise asıl belirleyici etmen o hastanenin hatta o birimin florasıdır. Son yıllarda koagülaz-negatif stafilokoklar (KNS), Candida cinsi mayalar ve enterokoklara bağlı sepsis olgularında belirgin artışlar saptanmaktadır. Ayrıca hastanede gelişen sepsisler oransal olarak da artmaktadır. Bunun en önemli nedeni hasta sayısında ve invaziv girişimlerdeki, antibiyoterapi uygulmalarındaki artıştır. Splenektomize bir hastada ilk akla gelecek sepsis etkenleri Haemophilus influenzae, pnömokok, meningokok, Capnocytophaga ve Babesia olmalıdır. Batın içi odak varlığında mikst enfeksiyon (aeroplar ve anaeroplar) olasılığı düşünülmeli Bacteroides fragilis olasılığı mutlaka hatırlanmalıdır. İmmunsuprese konakta, özellikle nötropeni varlığında Pseudomonas aeruginosa akla gelmeli fakat çok geniş bir yelpazenin etken olabileceği de hatırlanmalıdır. Tamamen sağlıklı birinde ani başlayan sepsis tablosunda öncelikle pnömokok ve meningokok olasılığı akla gelmelidir. Yenidoğan sepsisi erken (< 7gün) ya da geç başlangıçlı olabilir. Etkenler intrauterin döneminde ya da doğum sırasında ve sonrasında bulaşabilirler. Bu tabloda grup B streptokoklar (GBS) ve E.coli öncelikle hatırlanmalıdır. 133 • Gökhan Aygün Çoğu hastada etken bakteriler iken diğer mikroorganizmalar da sepsis nedeni olabilirler. Mycobacterium avium-intracellulare AIDS olgularında sepsis nedeni olabilir. Mycobacterium tuberculosis’in de sepsis kliniği oluşturabileceği belirtilmiştir. Viruslar arasında CMV sepsisten sorumlu tutulmuş, sepsis olgularında belirgin artışı saptanmış fakat ilişki tam olarak ortaya konamamıştır. Candida cinsi mantarlar giderek daha çok sepsis etkeni olarak saptanırken intravenöz lipid solüsyonları ile beslenen hastalarda Mallessezia furfur sepsis etkeni olarak ortaya çıkabilir. Yanık hastalarında Fusarium cinsi mantarlar da sepsis oluşturabilirler. Parazitler içinde Plasmodium falciparum’un etken olduğu sıtma olgularında sepsis kliniği belirlenmiştir. Özellikle damar-içi kateterle ilişkili sepsis son yıllarda büyük artış göstermektedir. En sık etkenler arasında KNS, S.aureus, Candida spp., P.aeruginosa, Corynebacterium jeikeium sayılabilirken pekçok mikroorganizmaya bağlı kateterle-ilişkili sepsis olguları da bildirilmektedir. PATOGENEZ Mikroorganizmalar ve onların ürünleri genelde karmaşık bir immun yanıt sürecini başlatırlar ve sonuçta SIRS gelişir (Şekil 1). Gram-negatif bakterilerin hücre duvarındaki endotoksin, formil peptidler, ekzotoksinler, proteazlar sep- LPS+LBP Monosit LSP reseptörü Proteaz ve serbest radikal sal›n›m› Dengranulation TNF-α IL-1 Faktör XII aktifleflmesi (temas ve p›ht›laflma sisteminin aktifleflmesi yoluyal) Damar geçirgenli¤i Kollejenaz›n do¤rudan kan ile temas› 134 Sepsiste patogenez Gram-negatif bakteri Aktifleflmifl doku makrofaj› Pirojen maddeler IL-6 IL-8 Fagosit PAF kemotaksisi MPIC Fagositlerin dokuya göçü fiekil 1. Gram-pozitif bakteri CD14 CD14 Damar geçirgenli¤i faktörü Tromboksan sal›n›m› Trombositler LPS si me LPS+LBP tiflefl k a fil Proteaz ve tro serbest radikaller Nö LPS Serotonin LBP Monosit aktifleflmesi Doku faktörü ekspresyonu Serbest radikal hasar› Endotel hücresi Bazal membran Yüzey trombomodülin miktar›nda azalma Hücre adezyon molekülleri üretimi Fibrin çökmesi Trombositlerin bazal membran›na yap›flmas› Sepsis ve Septik fiok • sise yol açabilirler. Gram-pozitif bakterilerde ekzotoksinler, enterotoksinler, hemolizinler, peptidoglikanlar ve lipoteikoik asit yapıları immun sistemi uyarabilir. Gram-pozitif bakterilerde süperantijen olarak rol oynayan toksinler Toksik Şok Sendromu olarak adlandırılan özel klinik tablolara yol açarlar. Stafilokok Toksik Şok Sendromu Toksini-1 (TŞST-1) ve streptokokal pirojenik ekzotoksin-A en iyi bilinen örneklerdir. Mantarların hücre duvarındaki yapısal elemanları (mannan, galaktomannan, ...) ile SIRS sürecini başlatan tetiği çektikleri düşünülmektedir. Tetik çekildikden sonra gelişen olaylar oldukca karmaşık bir süreci başlatırlar. Bu süreç tamamen aydınlatılmamıştır ve olasılıkla daha iyi tanımlanmamış aracı etmenler/sitokinler bulunmaktadır. İlk aşamada aşırı bir immun yanıt ortaya çıkar. Bu yanıtın oluşumunda mikroorgnizmalara ait öğelerin mononükleer hücreleri (makrofajlar) uyararak pro-inflamatuar sitokinlerin salınımını uyarmaları önemlidir. Hatta bazı antibiyotiklerle (seftazidim, ...) yapılan tedavinin başlangıcında bu ürünlerin, aşırı yıkım sonucu çok artacağı ve klinik durumu biraz bozabileceği belirtilmiştir. Tümör nekroz faktör (TNF), İL-1, İL-12, İL-6 ve interferon-gamma bu aşamada en etkili mediyatörlerdir. Aynı zamanda mikroorganizma ürünleri nötrofilleri uyararak proteaz ve serbest radikallerin salınmasına neden olurlar. Mikroorganizma ürünleri için aynı zamanda endotel hücrelerinde de reseptörler bulunmaktadır. Organizma hücreleri ile mikroorganizma ürünlerinin etkileşiminde lipoprotein bağlayıcı proteinlerle (LBP) bağlanan lipopolisakkarid (LPS) yapısındaki ürünler için çok sayıda reseptör rol oynamaktadır. Bu ilk uyarı sonucunda kompleman sistemi, prostoglandin/lökotrien metabolizması, koagülasyon kaskadı ve diğer bazı sekonder interlökinler aktive olurlar. TNF ve İL-1, endotoksin gibi endotel hücrelerini aktive ederek fibrin depolanmasına ve yaygın damar içi pıhtılaşmaya (DIC) yol açar. Organizma bu sırada anti-inflamatuar yanıt oluşturarak dengeyi kurmaya çalışır. Bu amaçla İL-10, erimiş inhibitörler (TNF reseptörleri, İL-1 reseptör tip II, İL-1 inaktif form) salınır. Bu durum immunsupresif bir süreç oluşmasına neden olur. Sonuçta dengelerde inflamasyon antiinflamatuar yanıta, koagülasyon fibrinolizise hakim konuma gelir ve yaygın damar içi pıhtılaşma (DIC) ile erişkinin sıkıntılı solunum sendromu (ARDS) belirginleşir. Tablonun devamında mikrovasküler tromboz, hipoperfüzyon, iskemi ve doku hasarı gelişir. Bu durumun klinik yansımaları; ağır sepsis, septik şok, multiorgam yetmezliği ve ölümdür. KL‹N‹K YAKLAfiIM Sepsis acil bir klinik tablodur ve hızlı, uygun ve yoğun tedavi ile mortalitesi azaltılabilir. Sepsis düşünüldüğünde ilk olarak hasta stabil duruma getirilerek (sıvı replasmanı, oksijenizasyon, ...) klinik parametrelerle yeniden değer- 135 • Gökhan Aygün lendirilmelidir. İdrar çıkışı, mental durum, vital bulgular kaydedilmeli ve izlenmeye başlanmalıdır. Bu aşamada sıvı tedavisi ve vazoaktif tedavi önem taşımaktadır. Mümkünse santral venöz kateter takılarak tedaviyi izlemek en uygun yaklaşımdır. Hemen sonraki aşamada olası sepsis odağını belirlemek ve mümkünse ortadan kaldırmak için yeniden hasta değerlendirilmelidir. Bu değerlendirme uygun antibiyoterapi için çok önemlidir. İlk aşama toplum kaynaklı ya da hastane kaynaklı sepsis ayrımı yapılmasıdır. Daha önceki girişimler ve kullandığı ilaçlar etkenin belirlenmesinde fayda sağlayabilir. Daha önce antibiyotik tedavisi kullanan bir hastada Pseudomonas aeruginosa olasılığını düşünmek ve ona göre antibiyotiği seçmek önemlidir. Çünkü P.aeruginosa sepsisinde mortaliteyi azaltabilecek en önemli nokta erken ve etkili antibiyoterapi başlanabilmesidir. Altta yatan hastalık, etkenin tahmin edilmesinde önemli bir ipucu sağlayabilir. Enfeksiyon etkenini tahmin etmek, olası odağı belirleyebilmek için en önemli yaklaşımlardan biri ayrıntılı ve tekrarlanan fizik muayenelerdir. Özellikle deride saptanabilecek bazı bulgular etkenin belirlenmesinde önemli olabilir. Meningokoksemide makül, peteşi, purpuralar, gonokoksemide ellerde peteşi, püstül ve papüller, S.aureus enfeksiyonlarında septik emboliler, P.aeruginosa sepsislerinde ektima gangrenosum, Candida sepsislerinde deride kırmızı-pembe nodüler lezyonlar izlenebilir. Yaralar, özellikle enfeksiyon bulguları olanlar odak olabilir. Diğer sistemler hızla ve dikkatle gözden geçirilmelidir. Batın içi abse varlığı yönünden değerlendirme, perianal ve kadınlarda pelvik inceleme, osteomiyelit olasılığı yönünden ekstremitelerin gözden geçirilmesi de unutulmamalıdır. Tüm bu incelemelerden sonra mutlaka hemokültür ve olası odaklardan örnekler alınmalı, bu örnekler etkenler açısından hızla incelenmeli (Gram boyama) ve olası etken belirlenmeye çalışılmalıdır. Özellikle–varsa-damar içi kateterler özellikle incelenmeli klinik yanıt yeterli değilse ya da bazı özel etkenler belirlendiyse (P.aeruginosa, Stenotrophomonas, C.jeikeium, Candida, ...) klinik yanıt ne olursa olsun çıkarılmalıdır. Laboratuvar parametreleri de hastanın izleminde yer almalı ve tedavinin izlenmesinde ihmal edilmemelidir. Hemokültür en az iki tüp olarak farklı yerlerden en az 10 ml olarak alınmalı; kateteri olan (SVK) bir hasta söz konusu ise hemokültürün biri kateterden alınmalı ve bu ilgili laboratuvara bildirilmelidir. Bu uygulama ile katetere bağlı bakteriyemi/sepsis tanısı otomatize sistem kullanan (BACTEC, ...) merkezlerde sinyal verme süreleri izlenerek konulabilmektedir. Sepsis odağı olarak düşünülen örnekler laboratuvara gönderilirken "acil değerlendirme (Gram)" isteği mutlaka bildirilmelidir. Periferik yayma ve lökosit sayımı sepsis tanısı için önemlidir. Arter kan gazları, laktik asit, karaciğer fonksiyonları, üre, kreatinin, fibrin yıkım ürünleri, fibrinojen gibi para- 136 Sepsis ve Septik fiok • metreleri izlemek klinik takiple beraber önemli parametrelerdir. İlk değerlendirmede tam idrar tetkiki ve akciğer grafisi de yer almalıdır. C-reaktif protein (CRP) ve son yıllarda kalsitonin sepsis tanısında ve tedavinin izlenmesinde önemli parametreler olarak ortaya konulmuşlardır. Prokalsitonin, CRP’ye kıyasla daha çabuk yükselen ve nisbeten inflamasyon gerilerken daha erken azalan bir göstergedir. Prokalsitonin seviyesi ile sepsisin ağırlığı ve mortalite arasında ilişki olduğu belirlenmiştir. Yoğun bakım ünitelerinde yapılan çalışmalarda CRP >50 mg/L ve prokalsitonin ≥ 1.5 nanogram/ml sınır kabul edildiğinde sepsis tanısını %100’e yakın duyarlılıkla fakat %70 özgüllükte koyabildiği bulunmuştur. Bilinen en önemli nokta tek bir ölçümün faydalı olmadığı, belirli aralıklarla ölçüm yapılmasının sepsis tanısı ve izlemi için daha faydalı olacağıdır. Prokalsitonini klasik inflamasyon yanıtını belirleyen CRP, TNF-alfa, İL-6, lökosit sayısı ve vücut sıcaklığına karşın daha üstün bulan çalışmalar da vardır. Bununla beraber diğer klinik tablolarda da yükselebilmesi, eşik değeri konusunda fikir birliği olmaması nedeniyle, prokalsitonin ölçümlerinin tek başına değil, ancak klinik, diğer laboratuvar bulguları ve hastanın özellikleriyle birarada anlamlandırılması gerektiği unutulmamalıdır. Endotoksin, inflamatuar mediyatörlerin ölçümlerinin (TNF, İL-6, İL-8, İL10) sepsis tanısındaki değeri bilinmemekte ve günümüzde ancak deneysel çalışmalar düzeyinde devam etmektedir. Ayırıcı tanıda enfeksiyon dışı SIRS nedenleri hatırlanmalıdır. Doku hasarı (cerrahi, travma, venöz tromboz, hematom, myokard, akciğer enfarktüsü, transplant reddi, pankreatit, eritroderma), metabolik tablolar (tiroid krizi, akut adrenal yetmezlik), maligniteler (hipernefroma, lenfoma, tümör lizis sendromu), subaroknoid kanama, tedavide kullanılan ajanlara karşı gelişen yanıt (kan ürünleri, sitokinler, koloni stimüle edici faktörler, anesteziklere bağlı malign hiperpreksi, opiatlar, nöroleptik sendromu,...) sepsisle karışabilir. Unutulmamalıdır ki kesin kanıtlanmadıkca ve ayrım net olarak yapılamadıkça bu olguları sepsis olarak değerlendirmek gerekmektedir. TEDAV‹ Sepsise yaklaşım multidisipliner olmalı, mümkünse mutlaka yoğun bakım ünitelerinde (YBÜ) izlenmelidir. En azından yoğun bir tedavi ve takip protokolü uygulanmalı ve YBÜ ile iletişim sağlanmalıdır. Sepsis tedavisi başlıca üç başlık altında incelenebilir: 1. Hızla hastayı stabil duruma getirmek 2. Hızla kandaki mikroorganizmaları temizlemek (antibiyoterapi) 3. Enfeksiyon odağını ortadan kaldırmak 4. Destek tedavisi 137 • Gökhan Aygün 1. Sepsisteki hastanın kliniği çok değişkendir ve mutlaka çok iyi bir takip gerektirir. Tedavide gelişen komplikasyonlara göre uygun tedaviler verilmelidir. Sepsis servis ortamında iyi bir takiple de tedavi edilebilirse de özellikle hipotansiyon sıvı ve sempatomimetik ajanlarla tedavi edilemiyorsa ve /veya oksijenasyon bozulmuş ise (PaO2 < 60 mmHg) mutlaka YBÜ’nde izlenmesi sağlanmalıdır. En önemli destek tedavisi sıvı replasmanıdır. Sıvı replasmanı ve hemodinamik değişiklikleri izleyebilmek için santral kateterizasyon ile basınç izlenmesi gerekir. Santral venöz basınç 10-15 cm H2O ve pulmoner kapiller "wedge" basıncı 14-18 mmHg basıncında tutulmaya çalışılır. Uygun sıvı replasmanısağlandığında vazopressör ilaçlar kullanılabilir. İmkanlar kısıtlıysa arteryal tansiyon, kalp hızı ve idrar çıkışı ile sıvı replasman ihtiyacı izlenebilir. Sıvı kristaloidler ya da kolloidlerle yerine konabilir. Kolloid kullanımıyla akciğer ödemi riski daha az bulunmuştur. Anemisi olanlara taze kan ya da eritrosit süspansüyonu verilebilir: bu hastalarda ortak görüş bulunmamakla beraber Hb 9-10 g/dl seviyelerinde tutulmaya çalışılmalıdır. Uygun sıvı tedavisine rağmen ya da pulmoner kapiller basıncı 14-18 mmHg olduğu halde hipotansiyon düzelmiyorsa vozoaktif ilaçlar kullanılmalıdır. Bu ilaçlar arasında en çok dopamin kullanılır. Dopamin 20 mikrogram/kg/dakika dozuna kadar artabilen dozlarda infüzyonla verilir. Daha düşük doz dopamin ile norepinefrin kombinasyonunun daha etkin olduğunu ileri süren çalışmalar da bulunmaktadır. Dobutamin diğer önerilen bir vazoaktif ilaçtır. En uygun seçenek hastadan hastaya farklılık gösterebilir ve iyi bir izlem ile tedavi sürdürülmelidir. Sepsiste solunum yükü ve akciğer yetmezliği nedeniyle oksijen ihtiyacı artar. Mutlaka hastalara oksijen desteği sağlamak gerekir. Hastalarda mental durum bozuluyorsa, solunum hızı > 40 oluyorsa ve oksijen desteğine rağmen hipoksemi sürüyorsa hemen mekanik ventilasyon uygulanmalıdır. Hastayı stabil duruma getirmek için diğer destek tedavileri içinde asidoz devam ederse bikarbonat infüzyonu yapılması, DIC geliştiğinde heparin kullanımı, kanama bulguları varlığında taze dondurulmuş plazma, trombositleri yerine koyma tedavisi sayılabilir. Steroidlerin sepsis tedavisinde etkinliği gösterilememiştir. Bazen düşük dozlarda 5 gün tedavinin faydalı olabileceği belirtilmektedir. Naloksan, antiinflamatuar ilaçlar, antihistaminikler, pentoksifilin, ibuprofen denenmiş fakat klinik etkinlikleri tam olarak bulunamamıştır. Son zamanlarda nitrik oksit ve serbest oksijen radikallerinin sepsisteki önemleri daha iyi belirlenmiş ve antioksidanların etkin bir tedavi seçeneği olabilecekleri üzerinde durulmuştur. Hayvan modellerinde nitrik oksit sentetaz inhibitörleri başarıyla denenmektedir. İmmunglobulinler bazen kullanılıyor olsa da klinik etkinlikleri kanıtlanmamış ve önerilmeyen ajanlardır. Nötropenik olmayan hastalarda koloni stimüle edici ilaçlar da faydalı bulunmamışlardır. 138 Sepsis ve Septik fiok • Endotoksinin etkin bölümü Lipid A’ya karşı oluşturulan monoklonal antikorlar (HA-1A, E5), Gram-negatif bakteri sepsislerinde denenmiş fakat klinik fayda beklenildiği kadar olmamıştır. Sitokinlerin etkisini bloke etmeye yönelik tedavilerden de beklenen sonuçlar alınamamıştır. 2. Antibiyoterapi: Geriye dönük çalışmalar göstermiştir ki uygun antibiyoterapi sepsiste mortaliteyi düşürmekte etkili bir uygulamadır. Eldeki klinik ve mikrobiyolojik verilerin hızlı ve dikkatli incelenmesi sonucunda en uygun seçeneklerden birisi belirlenerek antibiyoterapi gecikmeden başlanmalıdır. Mutlaka parenteral, en uygun dozda ve bakterisidal antibiyotikler seçilmelidir. Hemokültür sonuçlarına göre antibiyoterapi yeniden düzenlenmelidir. Tedavi süresi için öneri kesin olmamakla beraber 10-14 gün sürmesi tercih edilir. Eradikasyon gecikir, ateş, lökositoz, akut faz yanıtı gerilemezse yeniden değerlendirilip olası komplikasyonlar aranır ve süre uztılabilir. Sepsiste antibiyoterapi için önerilebilecek antibiyotikler enfeksiyon odağı ve hastanın klinik özelliklerine göre şu şekilde özetlenebilir (Tablo 1): Tablo 1. Sepsiste antibiyoterapi önerileri TANI ÖNER‹LEN ANT‹B‹YOTERAP‹ Toplumdan edinilmifl ürosepsis (3. kuflak sefalosporin ya da Anti-pseudomonal penisilinler ya da Kinolon) ± aminoglikozid Toplumdan edinilmifl sepsis (kaynak ?) (3. kuflak sefalosporin +metronidazol Tikarsilin-klavulanat ya da Ampisilin-sulbaktam ya da Piperasilin-tazobaktam) ± aminoglikozid Hastaneden edinilmifl sepsis (nötropenik olmayan olgular) !!! Hastane floras› ve primer odak en önemli belirleyicidir. (3. kuflak sefalosporin +metronidazol Tikarsilin-klavulanat ya da Ampisilin-sulbaktam ya da Piperasilin-tazobaktam ya da ‹mipenem/Meropenem) ± aminoglikozid Nötropenik hastada sepsis Seftazidim+metronidazol+aminoglikozid Tikarsilin-klavulanat ya da Piperasilin-tazobaktam + aminoglikozid ‹mipenem/meropenem± aminoglikozid Sefepim ± aminoglikozid Kateterle iliflkili sepsis ? +Glikopeptid (vankomisin ya da teikoplanin) 139 • Gökhan Aygün Glikopeptidlerin ve antifungal ilaçların ampirik kullanımı önerilmez. Sadece kateterle ilişkili sepsis şüphesinde ve metisiline dirençli stafilokokların baskın olduğu hastanelerde gelişen enfeksiyonlarda ampirik tedavide glikopeeptidler yer alabilirler. 3. Primer oda¤›n tedavisi: Eğer bir odak belirlendi ise odak ortadan kaldırılmalıdır. Abse drene edilmeli, nekrotik dokular uzaklaştırılmalıdır. Vücuttaki yabancı cisimler odak olarak düşünülüyorsa mutlaka çıkarılmalıdır. 4. Erken enteral beslenme ve sepsis sürecinde stres ülser profilaksisi uygulanması önerilen destek tedavilerindendir. KAYNAKLAR 1. Ahuja SS, Ahuja SK, Phelps KR, Thelmo W, Hill AR. Hemodynamic confirmation of septic shock in disseminated tuberculosis. Crit Care Med 1992;20:901-3. 2. American Colege of Chest Physicians /Society of Critical Care Medicine Concensus Conference. Definitions for sepsis and organ failure and guidelines for the use of innovative therapies in sepsis. Crit Care Med 1992; 20:86475. 3. Bone RC. Sepsis, the sepsis syndrome, multiorgan failure: A plea for comparable definitions. Ann Intern Med 1991;114:332-3. 4. Carcillo JA, Cunnion RE. Septic shock. Crit Care Med 1997;13:553-74. 5. Dellinger RP. Current therapy for sepsis. Infect Dis Clin North Am 1999;13: 495-50. 6. Doğanay M. Sepsis tedavisi. Türkiye T›p Dergisi 1998;5:42-7. 7. Guidelines for the management of severe sepsis and septic shock. Sprung CL. Bernard GR, Dellinger RP (eds). Intensive Care Med 2001; 27(Supp.1). 8. Prins JM, van Agtmael MA, Kuijper EJ, van Deventer SJH, Speelman P. Antibiotic-induced endotoxin release in patients with gram –negative urosepsis: a double blind study comparing imipenem and ceftazidime. J Infect Dis 1995:886-91. 9. Rangel-Frausto MS. The epidemiology of bacterial sepsis. Infect Dis Clin North Am 1999;13: 299-312. 10. Sriskandan S, Cohen J. Gram positive sepsis. Mechanisms and differences from Gram-negative sepsis. Infect Dis Clin North Am 1999;13: 397-412. 11. Uzun Ö (ed). Sepsis ve sekelleri. Ankara: Hacettepe, 1996. 12. Uzun Ö. Yaptıklarımıza eleştirel bakış. 16. ANKEM Kongresi sunuları. ANKEM Derg 2001;15:234-7. 13. Warren HS. Strategies for the treatment of sepsis. NEJM 1997;336:952-3. 14. Weinstein MP, Towns ML, Quartey SM, Mirrett S, Reimer LG, Permigiani G, Reller LB. The clinical significance of positive blood cultures in the 1990s: a prospective comprehensive evaluation of the microbiology, epidemiology, and outcome of bacteremia and fungemia in adults. Clin Infect Dis 1997; 24:584-602. 140