Kan Bankacılığında tarama testlerinde güncel durum tarama
advertisement

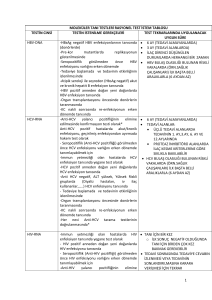
Kan Bankacılığında tarama testlerinde güncel durum Dr. Rüçhan Yazan Sertöz Ege Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı Temel tarama testleri İmmunoassay temelli testler Enzim immunoassay Kemiluminesan immunoassay Hemaglutinasyon/partikül aglutinasyon testleri Hızlı/basit yöntemler Nükleik asit amplifikasyon temelli testler Hangi testtest-Hangi etken Lab kalite sistemi GYSH Alt yapı Maliyet etkililik Epidemiyolojik veriler Deneyimli eleman Kaynaklar HBV Serolojik tarama HBsAg anti-HBc anti-HBs HBV Gizli HBV HBsAg mutantları HBIG kullanımı Aşılama programları Antiviral tedavi Düşük düzey perzistan HBV replikasyonu Geçirilmiş B hepatitinin reaktivasyonu Yöntemin analitik duyarlılığı anti--HBc anti HBc,, antianti-HBs anti-HBc uygulaması kanın güvenliğini arttırmaktadır ancak %2 ve altı pozitifliklerde öneriliyor Spesifite yüksek değil, doğrulama gereksinimi Allain, Vox Sang, 2007 anti-HBc anti-HBs ile birlikte bakılabiliyorsa ve 100miü/mL’nin üzerinde ise kan kullanılabilir DSÖ, Screening Donated Blood for TTI anti-HBc 2.104 altı, 2.105 üzeri +200miü/mL üzeri-NAT 2.105 üzeri +200miü/mL altı- İmha Yugi H, JCV, 2006 anti--HBc anti Ülke Avusturya Belçika anti-HBc Hayır İlk bağış İngiltere Evet Finlandiya Hayır Fransa Evet Almanya Hayır Yunanistan Hayır Italya Hayır Hollanda Hayır Norveç Slovenya İsviçre İlk bağış/6 aydan uzun ara Hayır İlk bağış Avustralya Hayır Kanada Hayır Hong Kong Hayır ABD Evet Guidelines for the Blood Transfusion Services HBsAg standardı 0.2 iü/mL (NIBSC) 0.1ng HBsAg/mL ≈ 0.025 IU/mL HBsAg ≈ 2000 HBV/mL Dünya Sağlık Örgütü standardına göre Deguchi M ve ark. Virol Methods 2004 HCV Serolojik göstergeler anti-HCV HCV Ag HCV çekirdek antijen testleri 1. Kuşak (Ortho Clinical Diagnostics, NJ, ABD) Kalitatif, mikroplak EIA, serbest HCV Ag Sadece serokonversiyon öncesi dönem pozitif 2. Kuşak Trak-C assay (Ortho Clinical Diagnostics, NJ, ABD) (1.5pg/mL) Serokonversiyon öncesine ek olarak antikor varlığında kullanılabilme Lumispot EIKEN HCV antigen assay (Eiken Chemical Diagnostics, Tokyo, Japonya) Ortho IRMA HCV Core assay (Ortho Clinical Diagnostics, NJ, ABD) Lumipulse HCV antigen assay (Ortho Clinical Diagnostics, Tokyo, Japonya) Architect HCV Ag kit, Abbott (0.06pg/mL) Genotip Genotip Genotip Genotip 1b 1a 2a 3a - 428iü/mL 896iü/mL 2700iü/mL 1002iü/mL HIV Serolojik göstergeler p24 Ag anti-HIV 1 (grup O dahil) + anti-HIV2 HIV GENOTİP, SUBTİPLERİ http://www.avert.org/hiv--types.htm http://www.avert.org/hiv HIV Weber B, Expert Review of Molecular Diagnostics,2008 HIV EIA -NAT Weber B, Expert Review of Molecular Diagnostics,2008 DSÖ ref panel 306 pozitif örnek 101-228 0.505 IU/mL-1.901 IU/mL NAT GenProbe-Novartis/Chiron Procleix duplex assay (HIV1-HCV) (Chiron) - 16’lı havuz Procleix Ultrio-Tigris (HIV1-HCV-HBV) (Chiron) – tek tek Roche Molecular Systems Cobas Ampliscreen HIV1 / HCV / HBV Cobas s201 Multipleks sistem Hamilton pipetlemeCobas Ampliprep-Cobas Taqman - 6’lı havuz Zelos x100 Alman Kızıl Haçı Kleinman, ISBT Science Series, 2008 MP 6 NAT ile ID-NAT ile Ülkemiz 11 HBV DNA pozitif - %0.06 2 HCV RNA pozitif - %0.01 8.333 kan verici 1 HBV DNA pozitif % 0,012 4.Ulusal Viroloji Kongresi Tek tek NAT EÜTF-MÜTF 4800 kan verici HBV DNA %0 Yeni Yöntem ve Teknolojiler Ne Zaman Test, infekte donörün tanımlanmasında yetersizse Mevcut tarama programının genel etkinliğini azaltmadan önemli ölçüde maliyet ve verimlilik avantajları sunuyorsa Altyapı, finansman, personel düzeyleri, eğitim ve kalite sistemleri yeterliyse Artımlı maliyet etkililik oranları (ICER) olumluysa GSYİHx(1-3) ICER: Toplam maliyet - önlenebilir tedavi giderleri NUYY Yöntem Seçimi Analitik duyarlılık Mutasyon saptama duyarlılıkları Duyarlılık, özgüllük Test süresi Testiçi, testlerarası tekrarlanabilirlik Maliyet Miyad Teknik destek Valide ve etkin Yöntem Seçimi Kalitatif testlerde ‘doğruluk’ için, bir niceliğin ölçüm değerinin asıl gerçek değerine olan yakınlık derecesi 3 adet pozitif 3 adet düşük pozitif 3 adet negatif örnek Kalitatif testlerde “kesinlik” için, aynı şartlarda tekrarlanan ölçümlerin aynı sonucu verme derecesi 1 adet pozitif 1 adet düşük pozitif CV %30’u 1 adet negatif geçmemeli Test-içi tekrarlanabilirlik Aynı çalışmada her örnek tek bir çalışmada 3’er kez Testler-arası tekrarlanabilirlik Farklı çalışmalarda her bir örnek 3 ayrı günde 1’er kez Rabenau HF. J Clin Virol 2007 Yöntem Seçimi kalite kontrol örnekleri akredite bir laboratuvardan alınan örnekler Pozitif referans: 3xsaptama limiti Düşük pozitif referans: saptama limiti - 3xsaptama limiti Rabenau HF. J Clin Virol 2007 Test performansının sürekli izlenmesi İç kalite kontrol (her sabah, her lot) Dış kalite kontrol Kit kontrol (PK, ZP, NK) (her çalışma) Kalibratörler Tekrarlayan Reaktivite Tekrarlayan Reaktivite Doğrulama test stratejileri Tekrarlayan reaktif donörler… Epidemiyolojik veri Özel donanım Deneyimli eleman Referans laboratuvar Doğrulama testleri Analitik antikor testleri RIBA (“recombinant immunoblot assay”) LIA (“line immuno assay”) EIA sonuçlarında gerçek pozitifliği ayırt eder Yüksek özgüllük Belirsiz sonuçlar Düşük duyarlılık ! HTLV--EÜTF HTLV Doğrulama testine alınan 54 örneğin ikisi pozitif Sonuç Algoritmalardaki doğrulama testleri yöntem adları ve duyarlılıklarıyla detaylandırılmalı RIBA, LIA temelli testler ile doğrulamalarda, tarama testleri negatifleşene kadar bağışçı aktif hale getirilmemeli Tekrarlayan reaktif olmayan örnekler için kullanıp kullanmama kararı, güncellenmesi planlanan Ulusal Rehber’de açıkça belirtilmeli DSÖ önerilerinde belirtilen etkin kalite sistemi Ulusal rehberlerde olması gereken minimum analitik düzeyler tüm göstergeler için belirlenmeli Seroloji negatif NAT pozitiflikleri artabilir (ICER’i yanlış etkiler) TM’de kalite sistemi ne olacak acil durumda ne yapılacak İKK, DKK planlaması bu merkezlerde nasıl uygulanacak