Proteinlerin yapısında bulunmayan aminoasidler
advertisement
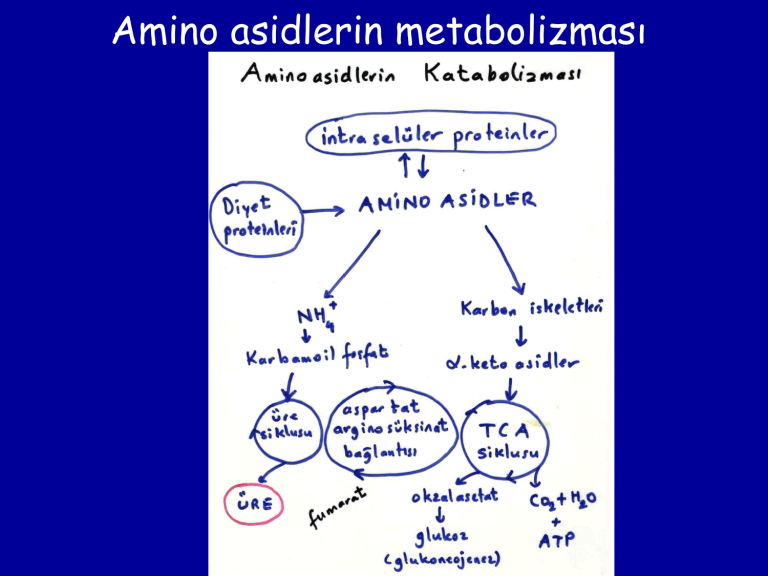
Amino asidlerin metabolizması Transaminasyon Piruvik asid CH3 Alanin CH3 C=O CH-NH2 COOH COOH NH2 CH2CH Fenilalanin O CH2C COOH transaminaz (kofaktör B6 vit= piridoksal fosfat) COOH Fenilpiruvik asid Transaminasyon COOH COOH CH2 + Piridoksal fosfat Piridoksamin fosfat COOH CH2 COOH CH2 CH2 CH-NH2 C=O COOH COOH glutamat okzalasetat transaminaz (GOT) = aspartat transaminaz (AST) Aspartik asid 2-Oksoglutarik asid CH2 + CH2 C=O CH-NH2 COOH COOH Okzalasetik asid Glutamik asid sülfit oksidaz SO32- + O2 + H2O SO42- + H2O2 İdrarda SO42- iyonu halinde atılır Zehirsizleştirmede rol oynar Bazı bileşiklerin suda, kanda çözünen bileşikler haline gelmesini sağlar. C- terminal (uç) N-terminal (uç) Glutationun organizmadaki işlevleri 1- Doğal bir hücre içi antioksidanıdır. Hücre içi oksido-redüksiyon reaksiyonlarına katılır. 2-Ksenobiyotikleri vücuttan atılacak hale getirir (sistein sağlayarak). 3-Bazı enzimlerin aktivasyonunda rol oynar. 4-Amino asidlerin hücre içine taşınmasında rol oynar (-glutamil siklusu). • G-SH + Kse G-S-Kse Glutation-S-transferaz • Glutation katepsinler ve Fibrini stabilize eden faktör gibi –SH içeren enzimler için aktivatördür. • -glutamil siklusu ile amino asidlerin hücrelerin içine taşınmasında rolü vardır. • Karnosin N-(-alanil) histidin • Anserin N-(-alanil) 3-metilhistidin Peptid yapısındaki hormonlar • Oksitosin ve vazopressin, 9 amino asid (hipofiz arka lob) • Adrenokortikortikotropik hormon (ACTH), 39 amino asid (hipofiz ön lob) • İnsulin, 51 amino asid (pankreas) • Glukagon, 29 amino asid (pankreas) • Tirokalsitonin, 32 amino asid (tiroid) Proteinlerin yapısı • • • • Birincil yapı İkincil yapı Üçüncül yapı Dördüncül yapı Linus Pauling 1901-1994 1954 Nobel Kimya; 1962 Nobel Barış • 1930 ve 1940’lı yıllarda Linus Pauling ve Robert Corey polipeptid zincirinin yapısını X ışınları ile tayin etmişlerdir. İkincil Yapı • α – Helezon konformasyonu (molekül içi hidrojen bağları), 3.6 kalıntıda bir α–heliks oluşur. β – Konformasyon (kırmalı tabaka yapısı, moleküllerarası hidrojen bağları) Bu bağlarda oluşan üçüncül yapı sonucunda • Globuler (yumak şeklinde) protein • Fibriler (lifsel) protein meydana gelir. Fibriler (lifsel) proteinler • a) İkincil yapıları -helezon tarzında olan polipeptid zinciri aynı şekilde ikincil yapısı oluşmuş bir başka polipeptid zinciriyle yeni bağlar oluşması sonucunda birleşir, bu suretle fibriler (lifsel) proteinler meydana gelir. (Miyozin, fibrinojen, α-keratin) • b) İkincil yapısı -konformasyon tarzında olan bir çift polipeptid zinciri, ikincil yapısı konformasyon tarzında olan başka bir çift polipeptid zinciri arasında meydana gelen bağlar sonucunda birleşir ve fibriler proteinler oluşur. (βkeratin, ipek fibroini) • Fibriler proteinler, üçüncül yapılarındaki güçlü disfülür (-SS-) bağları nedeniyle dış etkenlere ve proteinleri hidroliz eden enzimlere karşı çok dayanıklıdırlar ve suda çözünmezler. Fibriler proteinler, dokuların yapısını oluşturur. Dördüncül yapı • Üçüncül yapıları bulunan proteinlerin, protomer denilen alt birimlerinin hidrojen bağları, van der Waals çekmeleri, iyon bağları ile polimerize olmalarıyla dördüncül yapı oluşur. Skleroproteinler Skorbüt Sıcak su ile jelatin oluşur Ehlers-Danlos Sendromu Kollajen moleküllerinde amino asid dizisinin tekrarlayan tripeptid şeklindedir. Bu tekrarlayan tripeptid, (GlisinXProlin) veya (GlisinXHidroksiprolin) şeklinde gösterilebilir ki burada X, herhangi bir amino asid olabilir. Kollajen, bulunduğu dokulara dayanıklılık verir, doku şeklini korur ve dokuya gerilme direnci sağlar. Kollajen, kanın pıhtılaşmasında etkilidir; kan pıhtısı ile etkileşerek yara deliğini kapatır, Deriden elde edilmiş kollajen liflerinin elektron mikroskoobunda görüntüleri Elastin bulunduğu dokulara (damar, deri, akciğerler) esneklik sağlar. Elastinin esnekliği çapraz dezmosin bağları ve amorf yapısından kaynaklanır. Dört lizin molekülü bir araya gelince ortaya dezmosin çapraz bağı gelir. Yün keratininde disülfür bağı az, kolayca eğilebilir, bükülebilir. Boynuz, saç, tırnakta disülfür bağı çok bu nedenle çok serttirler. Saç lifi sıcakta gerildiğinde -heliks hidrojen bağı kopar ve -kırmalı tabaka yapısına döner ve saçın boyu uzar. Bir saç telinde ortalama 20 000 polipeptid zinciri bulunur. Bazı Önemli Proteinler • • • • • Kan serumu ve kan plazması proteinleri: Kan Kan serumu Kan + antikoagülan Kan plazması Kanda total protein %6-8 g’dır. Serumda %3-4 g serum albumin, %2-3 g serum globulinler, plazmada ise bunlara ilaveten fibrinojen vardır. Fibrinojen • • • • • Glikoprotein yapısındadır. Mol.ağ. 341.000. Kan plazmasında %0.4 g. Karaciğerde sentezlenir. Ağır karaciğer hastalıklarında kanda azalır, bazı infeksiyonlarda artar. Fibrini stabilize eden faktör (Faktör XIII) Kan pıhtılaşması tromboplastin 1. Protrombin F III Trombin Diğer faktörler F IIa F II trombin 2. Fibrinojen Fibrin (monomer) Fibrin (agregat) FI FSF trombin Ca2+ Aktif FSF Ca2+ F XIII F IV Fibrin (polimer, gerçek pıhtı) Kan pıhtılaşması İntrensek yol XII Ekstrensek yol XIIa XI XIa doku faktörü IXa IX X VII VIIa Xa antitrombin Va V II IIa I Ia fibrinojen çözünür fibrin XIII XIIIa çözünmez fibrin PIHTI K vitamininin pıhtılaşmadaki rolü • Preprotrombin (Glutamik asid) Protrombin (4-karboksi glutamik asid) • Faktör VII, IX ve X’un biosentezi için K vitamini gerekli. • K vitamini antagonisti heparin ve dikumarol (çürümüş tatlı yoncada bulunmuştur) tromboza engel olmak için tedavide kullanılırlar. • K vitamini eksikliğinde kanın pıhtılaşma zamanı uzar, organizmanın kanamalara eğilimi artar. Buna sebep kandaki protrombin eksikliğidir. HEMOFİLİ •Hemofili A. Kral sülalesi hastalığı. Faktör VIII (% 85) •Hemofili B: Faktör IX (%15) Hemofiliyle ilgili yazılı ilk kaynaklar, MS II yy Yahudilerin Talmud adlı kitabında yer alan el yazmalarına dayanır. 12. yüzyılda yaşamış olan Endülüs’lü bilim adamı Ebu-l Kasım el Zehravi’nin eserlerinde hemofiliden bahsedilmektedir. Hemofilinin toplum tarafından tanınması, 1800’lerde hastalığın İngiltere kraliçesi Victoria’dan kendisinden sonra gelen nesillere ve onun neslinden olan diğer kraliyet ailelerine (İspanya, İtalya, Rusya) geçmesine dayanmaktadır Serum albumin • Serum albumin: Kan serumunda %3-4 g serum albumin bulunur. • Mol. ağ. 69.000. • Özellikle karaciğerde sentezlenir. • Elektroforezde (kan serumu) albuminden daha ileride göç eden bir fraksiyon vardır, buna prealbumin denir. Globulin Kan serumunda %2-3 g serum globulin bulunur. Globulinlerin -, -, olmak üzere alt sınıfları vardır Molekül ağırlıkları 160.000 ile 1.000.000 arasında değişir. Globulinler RES hücrelerinde ve özellikle karaciğerde sentezlenir. • Molekül ağırlıkları: Çok farklı • Denatürasyonları: Isı, UV ve X-ışınları, asid, alkali, organik çözücüler ile denatüre olurlar. 2., 3., ve varsa 4. yapıları bozulur. • Amfolit özellikleri • Elektroforezi Protein elektroforezi Çöktürülmeleri • Proteinler; ısı, çeşitli tuzlar (amonyum sülfat, magnezyum sülfat, sodyum sülfat), organik çözücüler, ısı, asid ve bazlarla çöktürülebilir, • Tuzlar dışındakilerle yapılan çöktürme proteinleri denatüre eder ve proteinler bir daha doğal şekillerine dönemez. • Tuzlarla yapılan çöktürme proteinleri denatüre etmez, yani koruyucu çöktürmedir. Dializ