BİY 315 BİY 315 PEPTİTLER
advertisement

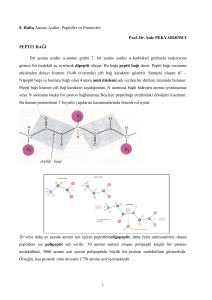
BİY 315 PEPTİTLER Yrd. Doç Yrd Doç. Dr Dr. Ebru SAATÇİ 2008-2009 Güz Yarı Dönemi PEPTİTLER Lineer amino asit polimerleridirler. Kuramsal olarak bir amino asidin αolarak, α karboksil grubunun OH’i ile ğ amino asidin α-amino diğer grubu arasından su ayrılarak peptit bağı oluşur. Peptit bağı, rijit ve düzlemseldir. • Düzlemsel (hareketsiz) peptit bağının etrafındaki atom grupları cis/trans izomerizm gösterirler. a C H C O N a Ca Trans (Tercih edilen konfigürasyon) C C N O H Ca Cis (x-pro sıralanışı) Komşu α-C atomları arasındaki uzaklık: 0.3 nm Peptitler, peptit bağı sayısına göre değil, AA sayısına göre sınıflandırılırlar. fl d l l İki amino asitten dipeptit, dipeptit Üç amino asitten tripeptit,… 10’a kadar olan amino asitten oligopeptit, li tit daha d h çokk amino i asitten ise polipeptit meydana gelir. Proteinler, yüzlerce amino asitten oluşan polipeptitlerdir. Gli i Glisin Alanin C-terminal N-terminal N terminal Amid grubu düzlemi su G s aa Glisilalanin Adlandırılmaları • Adlandırmada, serbest karboksil grubu içeren AA kalıntısından öncekilerin adlarına –il- eki ggetirilir ve en sonda serbest karboksil grubu içeren AA in ismi eklenir. Dipeptit Karnozin = β-alanil-histidin Tripeptit Gl Glutatyon = γ-glutamil-sisteinil-glisin l il i i il li i Peptitlerin Özellikleri Amino-terminal N-terminal Karboksi-terminal C-terminal Tetrapeptit: Alanil-tirozil-Aspartil-Glisin (Al T A Gl ) (Ala-Tyr-Asp-Gly) İyonlaşma Özellikleri Fizyolojik pH’da, • Peptit (amid) bağı: yüksüz • Peptitler: yüklü Peptitlerin asit-baz özelliği: -Amino Amino ve karboksi terminaller -İyonize yan zincirlerin sayısı ve cinsi etkilerler. Peptit bağını oluşturan amino ve karboksil grupları, peptitlerin asit-baz özelliklerine katkıda b l namazlar bulunamazlar. Noniyonize yan zincir taşıyan peptitlerin İ İyonizasyon şekilleri pH H <3 Alanilalanin CH3 CH3 O ԡ + H3N – CH – C _ N- CH - COOH ⏐ H pI CH3 O CH3 ԡ H3N+ – CH –C _ N - CH – COO- > 10 CH3 O CH3 ԡ HN2 – CH – C _ N - CH – COO- ⏐ İyonizasyon Katyonik K ik form f ((+1)) İzoelektrik form (0) H ⏐ H Anyonik y form (-1) İyonize yan zincir taşıyan peptitlerin iyonizasyonu COOH +NH 3 (CH2)4 (CH2)2 O CH2SH CH3 O O H3N+CH – C – N – CH – C – N – CH – C – N – CH – COOH H H H Alanil - glutamil - pH lizil - Net yük <3 +2 >10 -3 74 7.4 0 sistein Alfa - Karbon Etrafında Rotasyon Peptit bağı düzlemi hareketsiz olmasına rağmen, α - karbon etrafındaki rotasyon polipeptid zincirine esneklik kazandırır. Amid düzlemi Amid dü düzlemi lemi α-karbon Protein iskeleti boyunca rotasyonu sağlayan bağlar Peptitlerin Kimyasal Reaksiyonları 1. Asit / Baz Hidrolizi Peptit/Protein 6 M HCl 110°C, 24 h Serbest Amino Asitler AA1 • Peptit bağı hidrolizi, hidrolizi proteinlerin AA dizisinin belirlenmesi için gerekli bir basamaktır. AA2 2 Enzimlerle Hidrolizi 2. Proteazlar -Endoproteazlar Endoproteazlar Tripsin, Kimotripsin, pepsin -Ekzoproteazlar Aminopeptidaz Karboksipeptidaz Aminopeptidaz, -Papain Papain (in vitro şartlar) Fizyolojik Olarak Aktif Peptitler Peptit p AA sayısı y AA Dizisi Karnozin Anserin dipeptit dipeptit Glutatyon (GSH) tripeptit γγ-Glutamil-sisteinil-glisin Glutamil sisteinil glisin Bradikinin nanopeptit Plazma proteinlerinin hidrolizi ile açığa çıkarlar -Düz kasları gevşetir -Antienflamatuvar Kallidin dekapeptit (Lizil-bradikinin) Histidil-ß-alanin Metilhi tidil ß l nin Metilhistidil-ß-alanin Kas yapısı Peptit Yapılı Hormonlar HORMON PEPTİT AA Sayısı y TRH Tripeptit 3 AA Enkefalinler Pentapeptit 5 AA Gl k Glukagon P li Polipeptit tit 29 AA ACTH Polipeptit p p 39 AA İnsülin Polipeptit A zinciri: 21 AA B zinciri: 30 AA PROTEİNLER Lineer p polimerler: H2 N ( A i asitler Amino il AA sayısı: n AA sekansı: 20n )nCOOH Sınırsız sayıda farklı protein yapıları Bazı proteinler tek polipeptit zinciri içerirler; diğerleri ise iki veya daha çok sayıda nonkovalent birleşmiş polipetitten oluşurlar. Protein Yapısı Kovalent bağlarla (başlıca peptit bağları ve disüfit bağları) polipeptit zinciri birincil yapıdır. İkincil yapıda ise amino asit kalıntıları kısmen kararlı düzenlemelerle tekrarlayan yapısal modeller oluşturur. oluşturur Üçüncül yapı, polipeptidin tüm üç boyutlu katlanmalarının bir görüntüsüdür. Bir protein iki veya daha çok sayıda polipeptit altbirimi içerdiğinde uzaysal dü i dördüncül düzeni dö dü ül yapı olarak l k tanımlanır. l Proteinlerle ilgili kimyasal çalışmalar 1.. Kolon o o Kromatografisi o a og a s Bu yöntemle proteinler yük, büyüklük, bağlanma afinitesi fi i i ve diğer diğ özelliklerine ö llikl i göre ö ayrılabilinmektedirler. l bili k di l Uygun kimyasal özelliğe sahip katı maddeyle (kolon dolgu maddesi, örn: Sephadex, Hidroksiapatit, Mono Q, gibi jeller) kolon doldurulur (stasyoner ‘duran’ faz) ve g tampon çözelti (mobil ‘hareketli’ faz) kolondan devamlı geçirilerek akış sağlanır. A- Katyon–değiştirme kromatografisinde net yüklü proteinler net negatif yüklülere göre matriks boyunca mobil fazda daha yavaş göç ederler, ederler çünkü duran fazda net pozitif yüklülerin ilişkisi sonucu göç ö yavaşlar. l B- Size-exclusion kolon kromatografisi C- Affinite kolon kromatografisi • Yüksek Yük k tuz d derişimlerinde i i l i d proteinlerin i l i çözünürlüğü ö ü ü lüğü dü düşüktür ük ü ve b bu etki ki tuzlayarak çöktürme (salting out) olarak adlandırılır. Amonyum sülfat ((NH4)2SO4) suda yüksek çözünür olduğu için bu amaçla sıklıkla kullanılır. Elektoroforez (SDS-PAGE) • Yüklü proteinlerin elektrik alanındaki güçlerini esas alan yöntemdir. Proteinlerin izolelektrik noktaları ve yaklaşık molekül ağırlıkları ğ l kl gibi ibi çok k önemli ö li özelliklerini ö llikl i i de d tanımlamaya l olanak l k sağlar. Yük/kütle oranına göre proteinlerin gücü jel üzerinde yavaşlar. Göç, proteinin şeklinden de etkilenir. Elektroforezde makromolekülü hareket ettiren güç elektriksel potansiyel (E)’dir. Elektroforetik mobilitesi (µ) , partikülün hızının, (V) elektriksel potansiyele oranıdır. • Elektroforetik yyöntem ççoğunlukla ğ saflık ve molekül ağırlığını tahminlemek için seçilir ve deterjan olan sodyum dodesil sülfat (SDS) kullanılır. • SDS proteine, proteine proteinin molekül ağırlığının belirlediği miktarda, iki amino asit k l t kalıntısına bir bi molekül l kül SDS olacak şekilde bağlanır. Bağlı SDS net negatif yükü artırır, SDS bağlandığında proteinin doğal şeklide değişir ve birçok protein benzer şekil alır (lineer). 2D-Elektroforez İzoelektrik odaklama, bir proteinin izoelektrik noktasını (p p (pI)) tanımlamada kullanılan bir yöntemdir. Düşük Dü ük molekül l kül ağırlıklı ğ l kl organik ik asitler ve bazların (amfolitler) karışımın jjel boyunca y elektriksel alandaki dağılımları farklı pH değerlerini (pH gradyanı) oluşturur. oluşturur Sırasıyla izoelektrik odaklanma ve SDS elektroforezin birlikte kullanımı iki-boyutlu elektroforez olarak adlandırılır. 2D-Elektroforez jel görüntüsü SDS PAGE jel görüntüsü SDS-PAGE