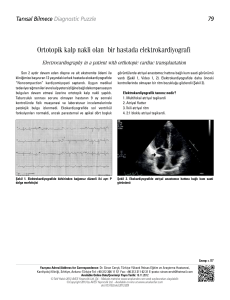
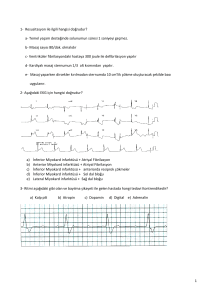
atriyal fibrilasyonun romatizmal mitral kapak hastalığında
advertisement

T.C. SAĞLIK BAKANLIĞI KARTAL KOŞUYOLU YÜKSEK İHTİSAS EĞİTİM VE ARAŞTIRMA HASTANESİ KOŞUYOLU KALP DAMAR CERRAHİSİ KLİNİĞİ ATRİYAL FİBRİLASYONUN ROMATİZMAL MİTRAL KAPAK HASTALIĞINDA RADYOFREKANS ABLASYON KATETERİ KULLANILARAK CERRAHİ TEDAVİSİ DR. BÜLENT MERT UZMANLIK TEZİ İSTANBUL / 2006 1 İÇİNDEKİLER ÖZET 4 ABSTRACT 7 GİRİŞ 10 GENEL BİLGİLER 12 1. 12 Tarihsel Gelişim 1.1. Aritmilerin cerrahi tedavisi 12 1.2. Atriyal fibrilasyonun cerrahi tedavisi 13 2. 15 Atriyal fibrilasyon ve cerrahi tedavi yöntemleri 2.1. Atriyal fibrilasyonun tanım ve sınıflaması 15 2.2. Atriyal fibrilasyonun epidemiyolojisi ve nedenleri 16 2.3. Atriyal fibrilasyonun patofizyolojisi 17 2.4. Atriyal fibrilasyon mekanizmaları ve cerrahi teknik ile ilişkisi 19 2.5. 22 Atriyal fibrilasyonun cerrahi dışı tedavisi 2.5.1. Farmakolojik tedavi 23 2.5.2. Elektriksel kardiyoversiyon 22 2.5.3. Pacemaker tedavisi ve kateter ablasyonu 24 2.6. Cerrahi tedavi teknikleri ve değişik enerji kaynakları ile ablasyon 24 2.6.1. COX MAZE III prosedürü ve modifikasyonları 24 2.6.2. Mikrodalga ablasyon 27 2.6.3. Kriyoablasyon 28 2.6.4. Lazer ablasyon 29 2.6.5. Ultrason ablasyon 29 2.7. 30 Radyofrekans ablasyon 2 MATERYAL VE METOD 35 1. Amaç 35 2. Hasta Seçimi ve Endikasyonlar 35 3. Unipolar ablasyon uygulaması 37 4. Bipolar ablasyon uygulaması 38 5. Postoperatif takip 40 6. İstatistiki Karşılaştırmalar 42 SONUÇLAR 43 TARTIŞMA 48 KAYNAKLAR 51 ŞEKİLLER 64 3 ÖZET Atriyal fibrilasyon (AF) günümüzde en sık rastlanan uzun süreli bir aritmidir. Atriyal fibrilasyon tüm nedenlere bağlı mortaliteyi ve kardiyovasküler hastalığa bağlı mortalite ve morbiditeyi (ani ölüm, kalp yetmezliği, tromboembolik komplikasyonlar, hastanede yatış süresinde uzama, tedavi maliyetinde artış, yaşam kalitesinde azalma) önemli ölçüde arttırmaktadır. Diğer kardiyovasküler rahatsızlıklar giderildikten sonra bile AF ölüm açısından önemli bir risk faktörüdür. Büyük bir kısmı organik kalp hastalığıyla (koroner arter hastalığı, kalp kapak hastalığı, konjestif kalp yetmezliği ve hipertansiyon) ilişkili iken yaklaşık % 31’inde altta yatan bir kalp hastalığı yoktur. Dr Cox ve arkadaşları tarafından geliştirilen ve sol atriyal izolasyon prensibine dayanan COX- MAZE III prosedürü altın standart olmuştur. Bu yöntemin yüksek başarısına rağmen tecrübe gerektirmesi, invaziv olması, uzun sürmesi nedeniyle aynı prensiple daha pratik yöntemler kullanılması amaçlanmış ve değişik enerji kaynakları kullanılarak tedavi yöntemleri geliştirilmiştir. Bu amaçla kriyoablasyon, mikrodalga, elektrokoterizasyon, ultrason, lazer ve radyofrekans ablasyon ile çalışmalar yapılmıştır. Bu enerji kaynakları arasından en sık kullanılanlar uygulama kolaylığı ve geniş bilgi birikimi nedeniyle kriyoablasyon ve radyofrekans ablasyondur. Bu çalışmanın amacı kronik atriyal fibrilasyonu olan, açık kalp cerrahisine aday, romatizmal mitral kapak hastalarında intraoperatif olarak radyofrekans ablasyon ile sinüs ritmini tesis etmek ve böylece atriyal fibrilasyonun olası mortalite ve morbiditesini en aza indirmek, hastaların yaşam kalitesini arttırmak ve tedavi maliyetini azaltmak, 4 kulandığımız radyofrekans ablasyon kateterlerinin etkinliğini ve güvenilirliğini denetleyerek klinikte yaygın kullanımını sağlamaktır. Çalışmamıza romatizmal mitral kapak hastalığı olan ve bu amaçla açık kalp ameliyatı uygulanacak atriyal fibrilasyon ritminde olan 25 hasta dahil edildi. Ablasyon işlemi standart kardiyopulmoner bypass altında, kros klemp sonrası primer cerrahi girişimden (rekonstriksiyon, replasman vs.) önce cerrahi Maze prosedürü prensipleri esas alınarak uygulandı. Onbir hastaya bipolar, 14 hastaya monopolar ablasyon uygulandı. Kardiyopulmoner bypass (KPB) çıkışında 21 hasta normal sinüs ritmine dönmüşken, 2 hasta AF’de, 1 hasta atriyal fibroflatter ritminde, 1 hasta nodal ritimde idi. Taburcu olurken 16 hasta (% 64) sinüs ritminde, 8 hasta (% 32) AF’de ve 1 hasta da (% 4) nodal ritimdeydi. Post operatif 3. ayda yapılan kontrolde toplam 19 hasta (% 76) normal sinüs ritmine dönmüştü 4 hasta (% 16) halen AF’de, 1 hasta (% 4) fibroflatter ritminde 1 hasta da (% 4) nodal ritimde idi. Erken dönemde mortalite ve morbidite gözlenmedi. Bir hastaya postoperatif 8. ayda kalıcı pacemaker implantasyonu uygulandı.. Sonuç olarak erken dönemde atriyal fibrilasyonun radyofrekans ablasyon yöntemiyle tedavisinde elde edilen başarı yüzdesi tatmin edici düzeydeydi. Bu yöntem, uygun hasta profili seçildiğinde ve titiz bir uygulamayla hastalar bir protokole göre takip edildiğinde başarılı, güvenle uygulanabilen ve uzun dönemde hasta yaşam kalitesini arttıran, tedavi maliyetini azaltan etkili ve kolay uygulanabilir bir prosedürdür. 5 ABSTRACT Atrial fibrillation (AF) is a long lasting arryhthmia and is the most frequently encountered arryhthmia nowadays. Atrial fibrillation significantly increases both total mortality rates and mortality and morbidity related to cardiovascular disease (sudden death, heart failure, thromboembolic complications, prolonged duration of hospital stay, increased cost, decreased quality of life). Even after all cardiovascular pathologies have been cured, AF still remains as a significant risk factor of mortality. Although in most of patients AF is related to an organic heart disease such as coronary artery disease, heart valve disease, congestive heart failure and hypertension, in about 31% of cases no underlying heart disease is present. COX- MAZE III procedure, created by Dr Cox et al., is based on the principle of left atrial isolation and has become the gold standart for surgical treatment of AF. Although this procedure has a high rate of success, it is highly invasive, requires experience and duration of procedure is quite long. For these reasons, new more practical procedures using the same principle but different sources of energy have been developed. Studies including cryoablation, microwave, electrocauterization, ultrasound, laser and radiofrequency ablation have been performed. Among these energy sources, radiofrequency ablation and cryoablation have been used most frequently due to the ease of use and a broad spectrum of knowledge on these sources. 6 The chief aim of this study is to restore sinus rhythm by use of radiofrequency ablation intraperatively in patients with rheumatic mitral valve disease who undergo open heart surgery and has chronic atrial fibrillation. Also we aimed to reduce the mortality and morbidity related to AF, to increase the quality of life and to decrease cost of medical treatment by achievement of sinus rhythm. We tried to achieve more common use of radiofrequency ablation catheters by thorough testing of efficacy and safety of them. Our study included 25 patients with rheumatic mitral valve disease who underwent open heart surgery and had chronic atrial fibrillation. The ablation procedure was performed with standart cardiopulmonary bypass after aortic cross clamping and before the main surgical intervention (valve reconstruction or replacement). The ablation procedure was based on the same principles as surgical Maze procedure. Bipolar ablation was performed in 11 patients whereas monopolar ablation was performed in 14. Upon cessation of cardiopulmonary bypass normal sinus rhythm was restored in 21 patients whereas AF was persisting in 2 patients. One patient had atrial fibroflutter and one had nodal rhythm. On discharge, 16 patients (64 %) had sinus rhythm, 8 (32 %) had atrial fibrillation and 1 (4 %) had nodal rhythm. On postoperative third month 19 patients (76 %) were in normal sinus rhythm. Atrial fibrillation was present in 4 patients (16 %), atrial fibroflutter was present in one (4 %) and nodal rhythm was present in one (4%). We didn’t observe any early morbidity and mortality. Permanent pacemaker implantation was performed in one patient in postoperative 8th month. 7 We had satisfactory early results with radiofrequency ablation for treatment of atrial fibrillation. This procedure is a successful, safe, easily performed and effective method which increases quality of life and reduces costs of treatment. It is important to choose patients suitable for this treatment and follow a standart protocol carefully. 8 GİRİŞ Atriyal fibrilasyon (AF) toplumda sık rastlanan, uzun süreli bir ritim bozukluğudur. İlk olarak 1909 yılında Lewis tarafından tanımlanmıştır (1). Genel popülasyonda görülme sıklığı % 0.4 ila % 2 iken bu oran 60 yaş üstünde % 10’a ulaşmaktadır. Mitral kapak için ameliyat edilecek hastalarda bu oran % 30 ila % 84 arasında, koroner kalp hastalığı nedeniyle opere edilecek olgularda ise % 5 olarak bildirilmiştir (2). Kalıcı AF görülen kişilerin büyük bir çoğunluğunda altta yatan bir kardiyovasküler hastalık olmasına rağmen, yaklaşık % 31’inde bu durum görülmemektedir (3). Kalıcı AF tüm nedenlere bağlı mortalitenin ve kardiyovasküler hastalığa bağlı mortalitenin ikiye katlanması ile ilişkilendirilmiştir (3). Diğer kardiyovasküler rahatsızlıklar giderildikten sonra bile AF ölüm açısından önemli bir risk faktörü oluşturmaktadır (4). İnme riskini 5 ila 7 kat arttırmaktadır ve bütün inmelerin % 15’inden sorumlu tutulmaktadır. Ayrıca sağlık harcamalarında önemli bir maliyet artışı getirmektedir (5). Atriyal fibrilasyon bu derece yaygın olmasına rağmen uzun süre medikal tedavi denenmiş fakat bunda istenen başarı düzeyine ulaşılamamıştır; bazı yayınlarda % 50 ila % 84 başarısızlık oranı bildirilmiştir (6). Birçok AF hastası sistemik emboli, hemodinamik dengesizlik, çarpıntı ve baygınlık hissi gibi akut fiziksel rahatsızlıkların yanı sıra antiaritmik ve antikoagülan tedaviye bağlı diğer birçok yan etkiye maruz kalmaktadırlar. Bu nedenle AF’yi düzeltmek için düşük riskli, minimal düzeyde invaziv ve maliyeti düşük yöntemlerin geliştirilmesi büyük önem taşımaktadır. Bu amaçla değişik cerrahi teknikler (sol atriyal izolasyon prosedürü, His düğümünün kateter ablasyonu, koridor prosedürü, pulmoner 9 düğme izolasyonu, atriyal kompartman operasyonu vb.) geliştirilmiştir (7). Son olarak James Cox ve arkadaşları (8) tarafından geliştirilen ve daha sonra iki kez modifiye edilen ‘‘MAZE III Prosedürü’’ % 100’e yakın başarı oranı ile bu konuda altın standart olmuştur. Atriyal fibrilasyonun tedavisinde amaç sadece ritmin sinüse döndürülmesi değildir. Atriyo-ventriküler senkronizasyonun ve atriyal transport fonksiyonunun yeniden sağlanması da en az onun kadar önemlidir. MAZE III Prosedürü’nün bu konudaki başarısının yüksek olmasına rağmen her iki atriyumda muhtelif kesiler yapılarak yeniden dikilmesi (cut and sew) prensibine dayanan bu işlem çok zaman alması, komplikasyon riskinin yüksek olması, çok deneyim gerektirmesi ve oldukça komplike bir girişim olması yaygın nedenleriyle kullanım alanı bulamamıştır. Bu nedenle kesip dikme işlemi sonucu oluşturulan lezyonların (skar) değişik enerji kaynakları kullanılarak oluşturulmasına çalışılmıştır. Bu amaçla radyofrekans (RF), mikrodalga, lazer, bipolar koter, kriyoablasyon vb. yöntemler denenmiştir. Günümüzde en yaygın olarak radyofrekans ve kriyoablasyon kullanılmaktadır. 10 GENEL BİLGİLER 1. TARİHSEL GELİŞİM 1.1. Aritmilerin cerrahi tedavisi Aritmilerin tedavisi için ablasyon tedavisi kavramı, mekanizması ne olursa olsun tüm aritmilerin, kalp içinde başlaması ve yayılması için anatomik bir substrata bağımlı olduğu hipotezine dayanır. Klasik örnek, Wolf-Parkinson-White sendromudur. Bu aritmi mekanizmasının ilerleyen cerrahi tekniklerle birlikte tanınması, 1968’de Sealy tarafından yapılan ilk cerrahi ablasyon prosedürünün uygulanmasına yol açmıştır (9). 1982’de Scheinman ve arkadaşları (10) ve Gallagher ve arkadaşları (11) transvenöz elektrod kateterlerinden geçen yüksek enerjili direkt akım şoklarının, atriyal fibrilasyonu olan hastalarda, tam kalp bloku ve iyi kontrol edilemeyen ventriküler yanıt hızları oluşturabileceğini bildirmişlerdir. Son 20 yıl içinde kardiyak aritmilerin cerrahi tedavisinde önemli gelişmeler kaydedilmiştir. 1980 yılından 1990’lı yılların ortalarına kadar cerrahi, supraventriküler aritmilerin ve özellikle de WPW sendromunun tedavisinde ön plana çıkmış, ancak daha sonra yerini perkütan tekniklere bırakmıştır. Aritmilerin tedavisinde sadece farmakolojik ajanların yetersizliği, önemli yan etkilerinin ortaya çıkması ve buna paralel olarak elektrofizyoloji alanındaki ilerlemeler bu gelişmenin önemli nedenleri olarak kabul edilebilir. Elektrofizyoloji alanındaki ilerlemeler sayesinde bir çok aritminin mekanizması daha iyi anlaşılmış, özellikle operasyon sırasında kullanılan geliştirilmiş haritalama sistemleri cerrahi sonuçların iyileştirilmesine önemli katkıda bulunmuştur. Bu bağlamda AF’nin temel mekanizmasında yatan fokal 11 tetikleme ve makro re-entery mekanizmalarının ortaya çıkarılması ile AF’nin cerrahi tedavisinde yeni yaklaşımlar ortaya çıkmıştır. Günümüzde genel kabul edilen görüş, bir aritminin cerrahi tedavisi için 4 önemli endikasyon olduğu şeklindedir. 1. Aritminin medikal tedaviye yanıtsız olması 2. Aritminin hastanın yaşam kalitesini ciddi şekilde düşürmesi, hayati tehlike oluşturması 3. Ek kardiyak cerrahi girişimle beraber, ( örn. mitral kapak veya koroner bypass operasyonu ) eş zamanlı olarak aritmiye müdahale edilmesi 4. Daha önce denenmiş olan perkütan tekniklerin başarısız olması. 1.2 Atriyal fibrilasyonun cerrahi tedavisi İlk olarak 1980 yılında Cox ve arkadaşları ‘sol atriyal izolasyon prosedürü’ nü tarif etmişlerdir (12). Bu prosedürde AF sol atriyum içerisine hapsedilirken, kalbin diğer bölümleri sinüs ritmini sürdürmektedirler (şekil 1). Bu prosedür ile kalıcı pacemaker ihtiyacı olmadan düzenli bir ventriküler ritm sağlanmış, aynı zamanda kardiyak hemodinaminin de düzeldiği gözlenmiştir. Sol atriyum izole olmuştur ve sol ventrikül ile senkron çalışmamaktadır. Buna rağmen sol ventrikül sağdan gelen düzenli kardiyak debiye hemen adapte olur ve akımı buna senkron bir şekilde olur. Kalp ritminin daha düzenli olması ve hemodinamide iyileşme sağlanmasına rağmen, sol atriyum halen fibrile olduğu için sistemik emboli riski devam etmektedir. 1982 yılında Scheinman (10) ‘his düğümünün kateter ile ablasyonu’ yöntemini başlattı. Bu yöntemde supraventriküler aritmi atriyumlara hapsedilmekte, ventriküler ritim kalıcı pacemaker ile sağlanmaktadır (şekil 2). Kalp hızı kontrol altına alındığı bu yöntemde atriyoventriküler senkronizasyon kaybına bağlı hemodinamik bozukluk ve sistemik emboli riski devam etmektedir. 12 1985 yılında Guiraudon (13), AF cerrahi tedavisinde kalıcı pacemaker gerektirmeyen ‘koridor prosedürü’nü geliştirmiştir. Bu prosedürde, atriyal septum içerisinde sino-atriyal düğümü ve atriyo-ventriküler düğümü de bulunduran bir bant, yani koridor oluşturularak sino-atriyal düğümün ventrikülleri uyarmasına izin verilir (şekil 3). Bu prosedürde kalp kontrol altına alınsa da hemodinamik düzelme sağlanmamakta ve sistemik emboli riski devam etmektedir. Yapılan tüm bu çalışmalar AF’nin günümüz tedavi prosedürlerine ışık tutmuş ve gelişen teknolojinin de yardımıyla cerrahi tedavide bir çok yeni yöntem geliştirilmiştir. 13 2. Atriyal fibrilasyon ve cerrahi tedavi yöntemleri 2.1. Atriyal fibrilasyon tanım ve sınıflaması Atriyal fibrilasyon atriyumların normal sinüs ritminin kaybolmasına yol açacak şekilde hızlı ve düzensiz aktivasyonudur. AF’de, atriyum duvarı kendi içinde bölgesel değişimle birlikte ortalama 400-600 kez kasılır ve ventrikül hızı atriyal aktiviteyle olan etkileşimiyle ve atriyoventriküler nodun filtre fonksiyonuna göre 100 ila 160 atım/dakika arasında değişir. Elektrokardiyografik olarak, değişik yükseklik ve morfolojide, küçük ve düzensiz ‘f’ dalgaları ve düzensiz QRS kompleksiyle karakterizedir. Klinik görünümlerini sınıflamada; akut, paroksismal, intermitan, kalıcı ve sürekli gibi sıfatlar kullanılmış fakat bu tanımlamaların birbiriyle çelişen belirsiz ifadeler olması çalışmaların karşılaştırılmasını ve tedavinin değerlendirilmesini zorlaştırmıştır. Bu yüzden American College of Cardiology / American Heart Association / European Society of Cardiology topluluklarının ortak girişimi AF sınıflandırması için açık kesin bir terminoloji önermiştir (14). Sınıflama AF’nin ilk tespit atağı ile başlamaktadır. Eğer bir hasta iki veya daha fazla atağa sahipse, AF rekürren (tekrarlayan) olarak kabul edilmektedir. Rekürren AF; paroksismal, persistan (inatçı) ve permanent (kalıcı) olarak tanımlanmaktadır. Paroksismal AF yedi gün veya daha kısa sürmektedir ve kendiliğinden ortadan kalkmaktadır. Persistan AF kendiliğinden ortadan kalkmamaktadır ve normal sinüs ritmini yeniden kazanabilmek için elektrik veya farmakolojik kardiyoversiyon gerektirmektedir. Permanent AF ise, kardiyoversiyondan sonra bile sinüs ritminin sağlanamadığı veya hastanın ve doktorun sinüs ritmini geri kazanmak için daha fazla çaba göstermeye karar aldıkları bir rahatsızlıktır. 14 2.2. Atriyal fibrilasyonun epidemiyolojisi ve nedenleri Atriyal fibrilasyon, en sık görülen sürekli kardiyak ritim bozukluğudur ve yaşlı nüfusun artması ile birlikte sıklığı artmaktadır, (4). Framingham çalışmasında, 22 yaşın üzerindeki kişilerde, AF insidansı %2 olarak saptanmıştır. Genel popülasyonda görülme sıklığı %0.4 ila %2 iken bu oran 60 yaş üstünde %10’a ulaşmaktadır. Atriyal fibrilasyon, hem kardiyak, hem de nonkardiyak hastalıkta oluşabilir veya herhangi bir hastalık olmaksızın görülebilir. Gelişmiş ülkelerde, hipertansif kalp hastalığı, AF’si olan hastalarda altta yatan en sık hastalıktır ( bazı çalışmalarda, vakaların %50’sinden sorumludur) (18). Kapak hastalığı, atriyal fibrilasyonun önemli bir nedenidir çünkü kronik AF’lu hastalarda bunun varlığı, tromboemboli riskini önemli derecede arttırmaktadır. Mitral stenozu ve atriyal fibrilasyonu olan hastaların %20 kadarında, embolik olaylar gelişir ve bunlar en sık olarak ( vakaların %60-75’inde) serebral dolaşımı etkiler. Mitral stenozu olan hastalar arasında, felç ve tromboemboli riski, atriyal fibrilasyonlularda sinüs ritminde olanlara göre 3-7 kat fazladır. Atriyal fibrilasyon en sık romatizmal kalp hastalığı ile birliktedir. Romatizmal kalp hastalığı olan 1100 hastada yapılan çalışmada en yüksek atriyal fibrilasyon sıklığı (%70) mitral stenozu, mitral yetmezliği, ve triküspit yetmezliğinde görülmüş ve izole mitral stenozu olanların %29’unda, izole mitral yetmezliği olanların %16’sında ve her ikisinin birlikte olduğu hastaların %52’sinde tespit edilmiştir (19). Mitral kapak hastalığı ile kronik AF’nin birlikte olduğu durumlarda, sadece kapağa yönelik cerrahi girişim sonrası, olguların %80’inden fazlasında AF’nin sebat ettiği görülmüştür (20). Melo tarafından yapılan bir çalışmada ise ameliyat sonrası spontan sinüs ritmine dönüş %8 olarak bildirilmiştir (21). 15 Koroner kalp hastalığı olanlarda, kalp yetmezliği veya hipertansiyon gibi komplike edici faktörler olmadığında, AF gelişme riski oldukça düşüktür. Akut miyokard infarktüsü olan hastalarda AF genellikle ilk 24 saat içinde oluşur ve önceden AF hikayesi yoksa kendi kendini sınırlar. Geçici AF’nin nedenleri arasında; kalp cerrahisi, tiroid hastalığı, alkol, kardiyomiyopati, ailesel nedenler, KOAH, elektrolit dengesizliği sayılabilir. Bazen de AF için; EKG, fizik muayene, telekardiyografi ve ekokardiyografide tespit edilen yapısal bir kalp hastalığı yoktur. Bu durumda AF, ‘lone’(yalnız) olarak adlandırılır. Lone AF görülme sıklığı yaklaşık %2 ile %31 arasındadır (22). Lone AF sebebinin atriyumlar içerisinde bulunan fibrotik alanlar, kalbin otonomik sinirsel uyarılara aşırı duyarlılığı veya lokal atriyal miyokardit olabileceği öne sürülmüştür (23). Atriyal fibrilasyon mortalite ve morbiditeyi önemli oranda arttırmanın yanı sıra hastaların yaşam kalitesini önemli ölçüde bozmakta ve sosyoekonomik olarak önemli bir yük getirmektedir. Dolaşım sistemi ile ilgili hastaneye yatışların yaklaşık %10 aritmi nedeniyledir ve bunun büyük kısmını AF ve atriyal flatter oluşturmaktadır (24). AHA verilerine göre ABD’de yıllık ortalama 3.6 milyar dolar AF tedavisi için kullanılmaktadır (25). 2.3. Atriyal fibrilasyonun patofizyolojisi Atriyal fibrilasyonun klinik belirtileri, atriyal sistolik fonksiyonun kaybına ve düzensiz ventriküler yanıta bağlıdır. Atriyal sistolik fonksiyon kaybı, kalbin hemodinamik fonksiyonunda bozukluğa yol açar ve normal kişilerde kalbin atım hacminde %10 azalmaya neden olur (yüksek ventriküler hızlarda daha da fazla azalır). Artan yaş ile sol ventrikül sistolik ve diyastolik fonksiyonunda azalma meydana geldiğinden atım hacmindeki azalma %30 veya daha fazladır. Bunun 16 yanı sıra düzensiz ventrikül hızları ventrikülün suboptimal şekilde dolmasına neden olur ve kalp debisinin daha da azalmasına neden olur. İyi kontrol edilemeyen ventrikül hızları ile birlikte olan AF’nin kardiyoversiyonu, genellikle sol ventrikülün ejeksiyon fraksiyonunu ve egzersiz kapasitesini düzeltir fakat bu düzelme prosedür sonrası yavaş yavaş olur. Atriyal sistolik fonksiyon kaybı, sol atriyum içinde staza neden olur ve intra-atriyal trombüs oluşumuna ve bunun neticesinde felç ve tromboemboli riskinde artışa neden olur. Sol atriyum içinde staz oluşması, hiperkoagülasyon durumunu gösteren ve pıhtılaşma faktörleri ile endotel ve trombosit fonksiyonunu içeren hemostatik bozukluklarla ilişkili bulunmuştur (15). Atriyal fibrilasyonu olan hastalarda, atriyal natriüretik peptit düzeyleri de yüksektir ve bu durum, hemokonsantrasyon ve trombüs oluşumu riskinde artışa katkıda bulunabilir (16). Atriyal fibrilasyon, hastaların yaklaşık %20-50’sinde kalp yetmezliği ile ilişkilidir. AF, atriyal transport kaybı yoluyla kalp yetmezliğine yol açabilir. Sol ventrikül hipertrofisinde olduğu gibi, diyastolik disfonksiyon varsa, atriyal ‘kick’ kaybı ile birlikte AF gelişmesi, kalp yetmezliğine yol açabilir. Mitral stenozlu hastalarda AF, hem atriyal kontraksiyon kaybı, hem de diyastolik dolma süresinde kısalma ile kalp yetmezliğine katkıda bulunur. Kontrol edilemeyen yüksek kalp hızları da, uzun sürdüğünde, miyokardiyumda, ilerleyici sol ventrikül dilatasyonuna ve sol ventrikül sistolik fonksiyonunda azalmaya yol açabilen ultrastrüktürel ve mikroskopik değişiklikler oluşturur; buna taşikardinin indüklediği kardiyomiyopati denir (17). Kronik kalp yetmezliği olan ve sinüs ritminde olan bir hastada, intrakardiyak basınçların yükselmesi, atriyal gerilme ve dilatasyona yol açar, AF gelişmesine ve tekrarlamasına zemin hazırlar. 17 2.4. Atriyal fibrilasyon mekanizmaları ve cerrahi teknik ile ilişkisi Atriyal fibrilasyon patogenezi tam olarak anlaşılamamış bir aritmidir (26). Ektopik fokusun tekli dolaşım yeniden girişi ‘reentry’ ve çoklu dolaşım yeniden girişi rahatsızlığın başlamasında ve devam etmesinde rol oynamaktadır (27). Son zamanlarda karşı çıkılsa da çoklu dolaşım yeniden girişi 50 yıl boyunca AF’nin dominant kavramsal modeli olmuştur. Bilgisayar simulasyonu kullanarak Moe ve ark (28) AF sırasında çoklu gezinen dalgaların (multiple wandering wavelets) bulunduğunu ortaya koyan bir model geliştirdiler. Atriyal fibrilasyon, “elektriksel remodeling” ismi verilen bir süreç yoluyla kendi kendisini sürdürür. Hayvan modellerinde ve klinik deneylerde gösterilmiş olduğu gibi, atriyal fibrilasyon, ‘atriyal fibrilasyonun atriyal fibrilasyonu doğurduğu’ bir dizi elektrofizyolojik değişikliklere neden olur. Atriyal fibrilasyon periyotlarına yanıt olarak, atriyal refrakter süre kısalır (daha uzun sikluslarda orantılı olarak daha fazla etki görülür). Tek ekstra uyarı ile atriyal fibrilasyonun yeniden başlatılması kolaylaşır. Tekrarlayan ataklar, aritmi kalıcı olana kadar her atağın daha uzun sürmesi ile sonuçlanır. Sinüs düğümü fonksiyonu da baskılanır. Bütün bu değişiklikler, sinüs ritminin yerine konmasından sonra zaman içinde geri dönüşür. Cox Maze prosedürü, bu dalgaları içeren reentrant ‘yeniden girişli’ dolaşımları kesmek üzere tasarlanmıştır. Allessie (29), AF’nin atriyumda aritminin ‘ehlilleştirilmesi’ ile sonuçlanan bir elektrofizyolojik ve yapısal değişiklik döngüsü başlattığını gözlemleyerek AF’nin anlaşılmasını bir sonraki aşamaya taşımıştır. Yani AF, AF’nin devam ettirilmesini sağlayan elektriksel bir yeniden modellemeye neden 18 olmaktadır (29). Bu nedenle, AF’nin süresinin tedavinin seçimini ve başarısını etkilemesi muhtemeldir. AF’nin bir substrat ve tetikleyici gerektirdiği yönünde genel bir uzlaşma vardır (30). Substrat atriyal bir anomalidir (genellikle inflamasyon veya fibrozis) ve AF’nin gelişimini destekleyen atriyal elektriksel fonksiyon bozukluğuna yol açar (27). Tetikleyiciler arasında atriyal ektopik fokus, atriyum duvar tansiyonunda değişiklikler ve otonom tonusda değişiklikler bulunmaktadır. Substratın ve tetikleyicinin değişiklik göstermesine rağmen, deneysel ve klinik kanıtlar pulmoner venlerin ve sol atriyumun AF’yi başlatmadaki ve devam ettirmedeki önemini işaret etmektedir (31-32). Haissaguerre (33) paroksismal AF’nin vakaların %94’ünde pulmoner venlerdeki ektopik atımlardan kaynaklandığını ortaya koymuştur. Bu, pulmoner ven endotelyumundan sol atriyum endokardına doğru anatomik geçişle ilişkili olabilir. Bu noktada farklı elektrik (iyonik farklılıklar) özelliklerine sahip iki doku kesişmektedir ve bu da AF’nin gelişimine katkıda bulunabilir(33-34). Bu gözlem paroksismal AF görülen hastalarda pulmoner venlerin önemini gözler önüne sermesine rağmen, yine de aynı gözlem kalıcı ve sürekli AF’ye uygulanamaz. Kalıcı ve sürekli AF’ye gelince, doğrudan kanıtlar bulunmamaktadır ancak klinik tecrübeler patogenezlerinde ve devam etmelerinde posterior sol atriyumun ve muhtemelen de pulmoner venlerin rol oynadığını göstermektedir. Harada (35) kalıcı AF görülen 10 hastada intraoperatif atriyal aktivasyonu mapping (haritalama) ile gösterdi ve çoğu hastada sol atriyumun elektriksel olarak aktivatör bir rol oynadığını gösterdi. Bununla birlikte, bu hastalar ayrıca patolojik sağ atriyuma sahip olma eğiliminde idiler (36). Sürekli 19 AF ve mitral kapak hastalığı görülen hastaları tedavi eden Sueda (37-38); AF’yi yaklaşık olarak %78 oranında düzelten yeni bir sol atriyal prosedür geliştirdiler. Bu prosedür, dört pulmoner ven ağzını çevrelemeyi (izole etmeyi), sol atriyum apendiksini kesmeyi ve oluşturulan lezyonu mitral kapak anulusuna doğru ilerletmeyi içermektedir (Şekil 4). 20 2.5. Atriyal Fibrilasyonun Cerrahi Dışı Tedavisi 2.5.1 Farmakolojik Tedavi Atriyal fibrilasyonun farmakolojik tedavisinde üç ana hedef belirlenmiştir. İlk amaç normal sinüs ritminin tesisi (kardiyoversiyon) ve bunun sürdürülmesidir. Bu amaçla birçok famakolojik ajan (sınıf Ia ve sınıf Ic antiaritmik ilaçlar, digitalis, verapamil, diltiazem, beta-bloker, sotalol, amiodaron) kullanılmış fakat pek azı etkili bulunmuştur. Sınıf Ia antiaritmik ilaçlar (kinidin, disopiramid, prokainamid) akut atriyal fibrilasyonun kardiyoversiyonunda etkili bulunmuştur. Sınıf Ic antiaritmik ilaçlar (flekainid, propafenon) paroksizmal ve yeni başlangıçlı atriyal fibrilasyonda etkilidir, kronik atriyal fibrilasyonda ise yapısal kalp hastalığı olmayan hastalarda kardiyoversiyon amacıyla tercih edilebilir. Digoksin, betabloker ve kalsiyum kanal blokerleri ise kalp hızının kontrolü amacıyla tercih edilir. Amiodaron ve sotalol ise son zamanlarda özellikle postoperatif atriyal fibrilasyonun tedavisinde tercih edilmektedir. Farmakolojik kardiyoversiyonun başarısını etkileyen faktörler; altta yatan etyolojinin düzeltilmesi ve atriyal fibrilasyonun süresidir. Atriyal fibrilasyon süresi kısa olan hastalarda (3 aydan kısa), kardiyoversiyondan sonra sinüs ritminde kalma olasılığı, 12 aydan daha uzun süreli AF’na göre iki kat daha fazladır (39). İki yıldan daha uzun süreli kalıcı AF’nun çok azı sinüs ritmine döner. Genellikle paroksismal AF’de ve yeni başlangıçlı AF’de etkilidir. İkinci amaç ise ventrikül hızının kontrolüdür. Ventrikül yanıtını düzenleyerek hemodinamik düzelme sağlamak ve taşikardinin indüklediği kardiyomiyopatiyi önlemektir. Bu amaçda çoğu kez başarı elde edilir fakat atriyumlar halen fibrilasyondadır ve ventrikül doluşuna ve kardiyak debiye katkısı yoktur ayrıca tromboemboli riski devam etmektedir. Son olarak 21 tromboembolinin önlenmesi amaçlanmaktadır. Bu amaçla antikoagülan tedavi ömür boyu kullanılmalıdır. Farmakolojik tedavideki düşük başarı düzeyi, tedavinin uzun sürmesi, kullanılan ilaçların yan etkileri, hasta uyumsuzluğu ve artan tedavi maliyeti nedeniyle yeni tedavi stratejilerinin geliştirilmesi bir ihtiyaç olmuştur. 2.5.2. Elektriksel Kardiyoversiyon Elektriksel kardiyoversiyon, atriyal fibrilasyonu olan hastalarda, atriyal miyokardiyumu repolarize ederek ve böylece organize iletiyi yerine koyarak sinüs ritmini geri getirir. Başlangıçta asistolik bir periyottan sonra, sinoatriyal düğüm, kardiyak bir pace-maker olarak rolünü devam ettirir. Eksternal elektriksel kardiyoversiyon, sinüs ritmini tesis etmek açısından etkilidir, ama etkinliği %2090 arasında değişir (başarı oranı altta yatan etyolojiye göre). İnternal kardiyoversiyon hem farmakolojik hem de eksternal kardiyoversiyonun başarısız olduğu hastalarda denebilir. İnternal kardiyoversiyonun düşük ve yüksek enerjili iki formu vardır. Yüksek enerjili kardiyoversiyonda, sağ atriyal kavite içine yerleştirilen kateter elektrod ile sırtta bulunan dağıtıcı elektrod arasına 200300J’lük bir şok verilir (40). Düşük enerjili kardiyoversiyonda ise, sağ atriyum veya koroner sinüse ve pulmoner artere yerleştirilen kateter elektrodlar ile uygulanır (41). Bu iki yaklaşım, özellikle obez hastalarda, akciğer hastalığı olanlarda ve standart transtorasik yaklaşımın başarısız olduğu hastalarda yararlıdır. 22 2.5.3. Pacemaker Tedavisi ve Kateter Ablasyonu Atriyal fibrilasyonu olan hastalarda, pacemaker tedavisinin geleneksel endikasyonları, bradikardi-taşikardi sendromu ile birlikte sinüs düğümü disfonksiyonu ve AV tam bloktur. AV iletinin kalıcı bir pacemaker yoluyla kateter ablasyonu, AF’li hastalarda, ventriküler hız kontrolünü sağlamak için etkili ve yüksek düzeyde güvenilir bir yöntemdir. Fakat antikoagülan tedavi gereksinimi devam etmektedir ve hemodinamik düzelmeye katkısı yoktur (42). Kateter ablasyonu kullarak AF’nin ortadan kaldırılması zor bir stratejidir ve oldukça deneyim gerektirmektedir. 2.6. Cerrahi Tedavi Teknikleri ve Değişik Enerji Kaynakları ile Ablasyon 2.6.1. COX MAZE III Prosedürü ve Modifikasyonları Cox maze III ameliyatı AF’nin tedavisinde altın standarttır. Cox ve ark.(43 44) AF’nin patofizyolojisi ile ilgili deneysel ve klinik kanıtlara dayanan bir prosedür tasarlamışlardır. Temel prensip fibrositlerin elektrik akımını iletmediğidir. Sonuçları geliştirmek ve ameliyatı basitleştirmek üzere prosedürü iki kez modifiye etmişlerdir ve ortaya Cox Maze III yöntemi çıkmıştır (45). Cox Maze III ameliyatında, insizyonlar ve kriyolezyonlar, AF’nin çoklu reentrant dolaşımlarını kesmek üzere stratejik şekilde gerçekleştirilir (Şekil 5 A, B). Standart kardiyopulmoner bypass başladıktan sonra çalışan kalpte ilk olarak sağ insizyonlar yapılır. Önce sağ atriyal apendiks ampüte edilir. Sağ atriyotomi, apendiks anterior yüzünden inferior vena kavaya doğru atriyum ortasına dek, posterior yüzünde ise triküspit kapağa dek ilerletilir. Diğer taraftan, yine sağ atriyumda süperior vena kava ile inferior vena kava arasında krista terminalisin 23 arkasından giden, düz ikinci bir insizyon yapılır. Bu insizyonun tam ortasından başlayan ilave bir insizyon triküspit kapak anülüsüne doğru yönlendirilir ve anülüse kadar olan mesafe kriyoablasyon ile tamamlanır. Kardiyopleji ile kardiyak arrest sağlandıktan sonra mitral kapak ameliyatlarında olduğu gibi sağ pulmoner venlerin hemen önünden (Waterson Oluğu) sol atriyotomi yapılır. Sol atriyotomi alt ve üst pulmoner venlere uzatıldıktan sonra venlerin sol tarafı da kriyoablasyon yapılarak dört pulmoner venin birlikte etrafında dairesel ileti bloğu oluşturulmuş olur. Buradan bu çember kriyoablasyon ile mitral kapak anülüsüne birleştirilir. Ardından sol atriyum apendiksi ampüte edilir ve apendiks ile dairesel atriyotomi arasındaki atriyum dokusuna kriyoablasyon uygulanır. Daha sonra süperior ile inferior vena kava arasının tam ortasından, atriyal septumda, fossa ovalise kadar bir insizyon yapılır. Buradan da triküspit kapak anülüsüne kadar kriyoablasyon uygulanır. Tüm sol atriyal insizyonlar içeriden tek kat devamlı dikiş ile kapatılır. Sol tarafın havası tahliye edildikten sonra aort klempi kaldırılır ve kalp reperfüze olurken sağ atriyotomi kapatılır. Kalp ritmi geri döndükten sonra kardiyopulmoner bypassa son verilir. Sağ ve sol insizyonlar en yaygın reentrant dolaşımları keser ve sinüs uyarısını sinoatriyal noddan atriyoventriküler noda belirli bir yol boyunca yönlendirir. Bu ana geçiş yolunun dışındaki “çoklu çıkmaz sokaklar” tüm atriyal miyokardiyumunun elektriksel aktivasyonuna izin verir. Cox Maze III, pulmoner damarları çevrelemeyi ve izole etmeyi ve sol atriyal apendiksi kesmeyi içermektedir. Bu özellikler, AF’yi düzeltmek için diğer araştırmacılar tarafından tasarlanan çoğu ameliyatta kullanılmaktadır. Bir çok merkezde (37,38,46,47), Cox Maze III ameliyatındaki insizyonların ve kriyolezyonların bazılarını içeren prosedürler uygulanmış ve rapor edilmiştir. 24 Bunlar parsiyel Maze prosedürleri olarak sınıflandırılır. Bu prosedürler, pulmoner venlerin izolasyonu veya sol atriyal apendiksin eksizyonu da dahil olmak üzere sol atriyum üzerine yoğunlaşmıştır (Şekil 6). Genellikle koroner sinüs, atrial flutter riskini arttırmasına rağmen göz ardı edilmiştir (48). Kress ve ark. (49) AF’nin intraoperatif ablasyonu için bir sol atriyal izolasyon paterni ortaya koymuşlardır. Bu lezyon paterni sol ve sağ pulmoner venleri çiftler halinde izole etmeyi, izole edilen bu bölümler arasında bağlantı oluşturmayı ve buradan da sol atriyal apendikse doğru lezyon oluşturmayı endokardiyal hem de epikardiyal olarak içermektedir. Bu prosedür hem uygulanabilir. Genellikle bu basitleştirilmiş lezyonların oluşturulması için alternatif enerji kaynakları kullanılır. Bu nedenle parsiyel Maze prosedürleri daha az zaman almaktadır (46, 50). Cox ve ark. (44) , her türden Cox-Maze prosedürünü içeren en büyük hasta serisini rapor etmiştir. Toplam 346 hastada operatif mortalite %2 idi. AF hastaların %99’unda tedavi edilmiştir ve hastaların sadece %2’si uzun vadeli postoperatif antiaritmik ilaç tedavisine ihtiyaç duymuştur. AF’nin başarılı bir şekilde düzeltilmesini mitral kapak hastalığının varlığı, sol atriyal büyüklük ve AF türü (paroksismal / persistan) etkilememiştir. Geçici postoperatif AF yaygındı ve hastaların %38’inde görüldü. Bu sorun, peroperatif dönemdeki kısa atriyal refrakter döneme atfedildi ve uzun vadeli sonuçları ortadan kaldırmadı (56). Hastaların %15’inde cerrahi operasyon sonrası pacemaker ihtiyacı duyuldu. Sağ atriyal transport fonksiyonu hastaların %98’inde görüldü ve sol atriyal transport fonksiyonunun görülme oranı da %93’tü (44). İnme yaygın değildi (57,58). Diğer merkezler de Cox Maze III prosedürü ile ilgili sonuçlar yayınlamıştır (59, 60). Genel olarak, etkinlikleri Cox Maze ve ark. tarafından rapor edilenlerden 25 daha düşük olmuştur. Cleveland Kliniği’nde ve Mayo Klinik’te AF’yi iyileştirme oranı %90 civarında rapor edilmiştir (59,61). Ek organik kalp hastalığının varlığı Cox ve arkadaşlarının çalışmalarında Cox Maze III prosedürünün etkinliğini ortadan kaldırmamasına rağmen, diğer araştırmacılar düşük oranda başarı rapor etmişlerdir. Çoğu seride, mitral kapak cerrahisinin Cox Maze III ile kombine edilmesi hastaların % 75- 82’sinde AF’yi tedavi etmiştir (62,63,64,65). Kamata ve arkadaşları (64,66) atriyal fibrilasyon dalgasındaki oynama genişliğinin (amplitüd) ve sol atriyum çapının bu hastalarda yürütülen Cox Maze prosedüründen sonraki sinüs ritmi tesisinin bağımsız prediktörleri olduğunu bulmuşlardır. Neden diğer araştırmacıların sonuçlarının Cox ve arkadaşlarınınkinden düşük olduğu belirsizdir. Çeşitli gruplar parsiyel Maze prosedürlerinin sonuçlarını yayınlamışlardır (36,37,46,47). Bu araştırmacılar hastaların %80’inde sinüs ritmini tesis etmişlerdir (46,50). İnsizyon ve kriyolezyon paternindeki küçük varyasyonlar sonucu etkilememiştir. Parsiyel maze prosedürleri sol atriyum kaynaklı AF’yi ortadan kaldırabilmesine rağmen, sağ atriyum kaynaklı atriyal flatter riski halen devam etmektedir (67,68,69). Bu prosedürlerden sonra atriyal flatterin ortaya çıkma olasılığı %5-10’dur ve bunun kateter ile ablasyonu kolaydır. 2.6.2. Mikrodalga ablasyon Termal zarar ve sonrasındaki skar formasyonu yolu ile iletim bloklarından oluşan hatlar yaratmak için mikrodalga enerjisinden yararlanılmaktadır. Yüksek frekanslı elektromanyetik (mikrodalga) enerji dokudaki su moleküllerinin osilasyonuna neden olur ve elekromanyetik enerji kinetik enerjiye (ısı) dönüştürür. 26 Dokuda hasar oluşturma mekanizması radyofrekansta olduğu gibi ısı temellidir (51). Mikrodalga ısıtma radyofrekansla ısıtmaya göre daha avantajlıdır çünkü ısıtılan dokunun derinliği ve hacmi çok daha fazladır ve bu da transmural lezyonlar için daha yüksek oluşum ihtimali anlamına gelir. Mikrodalga ısıtma endokardiyal yüzeylerde yanıklar oluşturmaz ve bu da tromboembolizm riskini azaltabilir (52). Mikrodalga sondalar koruyuculudur ve bu özellik epikardiyal ablasyon sırasında önem arz etmektedir. Günümüzde mikrodalga tabanlı AF ablasyonu için 2-, 4-, ve 10 cm’lik sondalar bulunmaktadır (53). Mikrodalga enerjisi ile yaratılan lezyon tipleri radyofrekans ile yaratılanlar ile benzerdir ve genellikle pulmoner damar izolasyonunu içerir. Mikrodalga ablasyonu yapılan hastaların %80’inde sinüs ritmi tesis edilmiştir (53). Dünya çapında, bu türden 500’den fazla prosedür gerçekleştirilmiştir ve bunların yaklaşık %30‘u “off pump”dır. Mikrodalga kateterin AF’nin intraoperatif zamanlarda kullanılmaya başlaması nedeniyle, tedavisinde ancak son uzun vadeli sonuçlar bulunmamaktadır. 2.6.3. Kriyoablasyon Kriyoablasyon, aritmi cerrahisinde yerleşik yöntemlerden birisidir ve Cox Maze III prosedürünün önemli bileşenlerinden birisini oluşturur (43, 45). Diazot monoksit tabanlı bir kriyosondanın atrial dokuya -60 derece 2 dakika süreyle uygulanması transmural lezyon üretir ve bu da görsel olarak teyit edilebilir. Doku bütünlüğü korunur ve böylece geride düz endokardiyal bir yüzey bırakır. Uyguladıkları parsiyel Maze prosedüründe Sueda ve ark. (37, 38) lezyon setini tamamlamak için kriyo-lezyonlar kullanmışlardır ve % 78 oranında başarı 27 bildirmişlerdir. Diğer araştırmacılar AF’yi tedavi etmek üzere pulmoner ven izolasyonundan oluşan sınırlı sol atriyal kriyoablasyon uygulamışlardır ve %70 başarı elde etmişlerdir (70). Cox ve ark. (34,45) son zamanlarda yayınladıkları bir raporda, Cox Maze III standart lezyon setinin kriyoproblar kullanılarak yeniden üretildiği minimal invaziv bir yönteme yer vermişlerdir. Bu prosedür zorlayıcı ve teknik açıdan zordur. En belirgin dezavantajları çok büyük donanım gerektirmeleri, epikardiyal yüzeylere uygulanmasının zor olması ve uygulama süresinin çok uzun olmasıdır. Bu probların zorluklarından birisi de sertliğidir; bunula birlikte, gelecekte geliştirilecek esnek problar ve farklı şekillerdeki problar bu sınırlamayı ortadan kaldıracaktır. 2.6.4. Lazer ablasyon Lazer enerjisi yüksek enerjili optik dalgalardan oluşur. Dokular üzerindeki etkisi direkt ısınma ile şok dalgalarının sebep olduğu hızlı hücresel patlamaların oluşturduğu mekanik hasarın bir bileşimidir. Lazer tekniği ile keskin ve dar ablasyon hatları oluşturulabilmektedir. Çünkü lazer ışınları dokuya direkt olarak penetre olur ve ışının sınırları dahilindeki dokuyu ısıtırken lezyon minimal lateral yayılım gösterir (54). Bu enerji kaynağının çok kuvvetli olması nedeniyle klinik olarak çok yaygın kullanılmamaktadır. 2.6.5. Ultrason ablasyon Titreşimsel bir enerji türüdür. Hücre zarlarını parçalar, fiziksel özelliklerini değiştirir veya termal ısınmaya neden olur. Kardiyak jeneratörlerde, kullanılan frekans aralığında oluşturduğu doku hasarı termal ısınma sonucudur. Oluşan 28 lezyonların sınırları belirli ve teorik olarak radyofrekans ile oluşanlardan daha geniştir. Transdüserin kırılgan olması ve 100 dereceyi aşan sıcaklıklarda zarar görebilmesi bir dezavantajıdır. Nekrotik doku varlığında ultrason emilim katsayısı değişeceğinden lezyonun genişlik ve derinliği değişecektir (55). 2.7. RADYOFREKANS ABLASYON Radyofrekans, frekansı radyo bandında yer alan ve alterne eden elektrik akımıdır. Radyofrekans yönteminde radyo bandında yer alan; 350kHz’den 1 MHz’e kadar alterne edilen ve dokuda ısı artışı meydana getiren radyofrekans enerjisi kullanılır. Elektrik akımı kateter ucundaki verici kutup ile hastanın sırtına yerleştirilmiş veya bipolar sistemde yine kateter üzerinde yer alan diğer alıcı kutup arasında hareket eder. Geçen enerjinin büyük bölümü kateter ile miyokardiyal dokunun temasta bulunduğu yüzeye iletildiğinden vücudun diğer bölümleri etkilenmez. Bu etkileşim sonucu dokularda titreşim ısı enerjisine dönüşür ve koagulasyon nekrozu oluşur (72). Yapılan çalışmalarda dokuyu 70 ila 80 derecede yaklaşık 1 dakika ısıtmanın 3 ila 6 mm derinlikte lezyon oluşturduğu gözlenmiştir ki bu da bir transmural geçiş bloğu hattı oluşturmak için yeterlidir (71). Radyofrekans ablasyon uygulaması için bir enerji jeneratörü ve probu olan çeşitli sistemler geliştirilmiştir. Radyofrekans ablasyon 1980’lerin ortalarından bu yana perkütan kateter aracılığıyla özellikle supraventriküler taşikardilerin tedavisinde kullanılmaktadır. Ucu serum irrigasyonlu radyofrekans ablasyonu ilk olarak 1988 yılında Wittkampf ve arkadaşları (73) tarafından kullanılmıştır. Bu kateterin kronik AF’de intraoperatif olarak kullanımı ilk olarak 1995 yılında Sie ve arkadaşları (74), daha sonra ise Melo ve arkadaşları (75) tarafından 29 gerçekleştirilmiştir. Monopolar sistemlerde, hasta deriye yerleştirilen (genellikle sırt bölgesine) elektrik yüksüz bir elektrod ile topraklanır ve akım radyofrekanslı kateterin ucundan akar ve dokuya temas noktasında ısıtır. Lokal olarak 100 derecenin üzerinde sıcaklıklar ortaya çıkarabilir ve bu da doku buharlaşmasına ve yüzeyel yanmalara neden olabilir. Dokunun diğer kısımları temas bölgesi ısındıktan sonra ısının diğer bölgelere aktarılmasıyla ısınır. Bu mekanizma lezyon derinliğini sınırlayabilir, transmural lezyon oluşturmak için aşırı enerji uygulamasına gerek duyulabilir. Serum soğutmalı sistemler ise yüzeyel yanmaların etkisini azaltırken lezyon derinliğini arttırabilir. Değişik ablasyon kateterlerinin etkinliğini araştıran Nagakawa ve arkadaşları (80), kuru ve serum irrigasyonlu kateterleri karşılaştırdılar ve sonuç olarak kuru sistemde istenen lezyon derinliğine ulaşmak için verilen enerji düzeyinde dokuda karbonizasyon oluştuğunu, karbonize yüzeyin ısıyı diğer katmanlara iletmede dirençli olduğunu ve bunun neticesinde tam kat lezyon oluşturmanın güç olduğunu ayrıca bu karbonize yüzeyin tromboemboli için odak oluşturduğunu ve en geniş ve en derin lezyonların serum irrigasyonlu kateter ile gerçekleştiğini gözlemlediler. Son zamanlarda geliştirilen bipolar sistemde kontrollü ve kesin transmural lezyon oluşturularak bu dezavantaj ortadan kaldırılır. Cerrahi uygulamalar için çeşitli kateter tipleri geliştirilmiştir. Bunlar arasında, esnek problar, rijit problar, kalem benzeri problar (serum ilaveli) ve bipolar klemp gibi problardır. Problar endokardiyal veya epikardiyal uygulanabilir. Her iki teknik de sürekli ve transmural lezyon oluşturabilir (71, 76). Epikardiyal uygulama çalışan kalpte de yapılabilmektedir (77). 30 Radyofrekans ablasyon amacıyla çeşitli lezyon tipleri oluşturulmuştur (62, 71, 78). Bu lezyon tiplerinin tamamı pulmoner venlerin tamamen veya tama yakın izolasyonunu, sol atriyum apendiksinin eksizyonunu veya dışlanmasını içerir. Ayrıca sol pulmoner venler ile sol atriyum apendiksi arasında ve yine sol pulmoner venler ile mitral kapak anulusu arasında lezyon oluşturarak iletinin engellenmesini içerir. Sağ atriyal uygulamalar ise Cox Maze III prosedürüne benzer şekilde yapılır (78,79) (Şekil 7). Sol atriyal uygulama ortalama 10-20 dakika sürmektedir. Bu süre Cox Maze III prosedürünü gerçekleştirmek için gerekli 1 saatlik süreden oldukça kısadır (62, 71, 77, 81, 85). Bu lezyon tiplerinin çeşitli olmasına rağmen AF’nin tedavi oranı %70 ila %80 arasında bildirilmiştir (71,78, 81, 82, 83, 84). Tedavi edilen hastaların çoğu organik kalp hastalığına sahipti ve ek olarak mitral kapak ameliyatı geçirmişlerdir. Bu hastalarda elde edilen başarı hemen hemen Cox Maze prosedürüne yakındır ve sağ atriyumun prosedüre dahil edilip edilmemesinden bağımsızdır (44, 59, 60). Peroperatif AF yaygındır ve vakaların yaklaşık üçte ikisinde görülür (71, 84, 85). Hastaların %30-40’nın AF ile hastaneden ayrılmasına rağmen, bir çoğu takip eden 3 ay içinde sinüs ritmine dönmektedir. Bu nedenle AF ile taburcu, prosedürdeki başarısızlığın endikasyonu değildir. Bazı araştırmacılar atriyal büyüklüğün başarıyı etkilediğini bildirmelerine rağmen, bu bulgu diğer araştırmacılar tarafından teyit edilmemiştir (62, 78). Atriyal transport fonksiyonu, sinüs ritmine dönen hastaların %80-100’ünde görülmektedir (86, 87). Elde edilen bu başarı radyofrekans ablasyona olan ilgiyi arttırmaktadır ancak oluşturulan lezyon tipi ve prosedürün sadece sol atriyumu içermesi konusunda halen tartışmalar devam 31 etmektedir. Uygulamalar arttıkça ve bu konuda yeni veriler yayınlandıkça prosedür daha yaygın hale gelecektir. 32 MATERYAL ve METOD 1. Amaç Bu çalışmamızda amacımız; kronik atriyal fibrilasyonu olan ve açık kalp ameliyatına aday hastalarda, intraoperatif olarak radyofrekans ablasyon uygulayarak, hastaları atriyal fibrilasyonun komplikasyonlarından korumak ve aynı zamanda radyofrekans enerjisinin bu konudaki etkinliğini ve güvenilirliğini denetleyerek tekniğin klinik uygulamalarda yaygın olarak kullanımını sağlamaktı. 2. Hasta Seçimi ve Endikasyonlar Hasta seçim kriterleri; kalıcı atriyal fibrilasyonu olması (en az 6 aydır AF mevcudiyeti) ve romatizmal mitral kapak hastalığı nedeniyle ameliyat endikasyonu bulunması idi. Bunun yanısıra endokarditi olan, öncesinde bilinen hasta sinüs sendromuna sahip, sol atriyum duvarında kalsifikasyon olan, kardiyak fonksiyonları uygun olmayan (EF <%25), bipolar uygulama için engel oluşturabilecek reoperasyon ve ileri adhezyon olan hastalar çalışma dışında bırakıldı. Atriyum çaplarının ileri derecede büyümesi ( sol atriyum > 7.2 cm); hem atriyum duvarının ince olması hem de sinüs ritmine dönme olasılığının az olması nedeniyle diğer bir kısıtlayıcı faktördü. 33 Tablo-1. Hastaların preoperatif demografik ve ekokardiyografik verileri. Preoperatif değişken Erkek : Kadın 7:18 (% 28 / % 72) Ortalama yaş (yıl) 46.2 ± 10.6 (20-67) Ortalama fonksiyonel kapasite (NYHA Sınıfı) 3.4 ± 0.64 (2-4) Ortalama AF süresi (yıl) 3.7 ± 2.01 (1-8) Hipertansiyon 6 (% 24) Kronik obstrüktif akciğer hastalığı 4 (% 16) Geçirilmiş mitral rekonstrüksiyon operasyonu 3 (% 12) Situs İnversus Totalis 1 (% 4) Şikayeti Çarpıntı 14 ( %56) Nefes darlığı 11 (% 44) Ejeksiyon Fraksiyonu (%) 59.3 ± 8.4 (30-70) Mitral kapak lezyonu Mitral darlığı 13 (% 52) Mitral yetmezliği 1 (% 4) Miks hastalık 11 (%44) Sol ventrikül diyastol sonu çapı (cm) 5.3 ± 0.7 (4.2-6.7) Sol ventrikül sistol sonu çapı (cm) 3.5 ± 0.7 (2.3-5) Mitral kapak alanı (cm2) 1.1 ± 0.1 (0.7-1.5) Sol atriyum çapı (cm) 5.7 ± 0.9 (4.1-7.2) Pulmoner arter basıncı (mmHg) 54.5 ± 12.2 (30-80) 34 Çalışmamızda 18 bayan ve 7’si erkek, toplam 25 hastaya radyofrekans ablasyon yapıldı. Olguların tamamı kardiyoloji ve kalp-damar cerrahisi ortak konseyi kararına göre operasyonuna karar verilmiş hastalardı. Çalışmaya alınan hastaların preoperatif demografik verileri Tablo 1’de özetlenmiştir. Hastaların tamamında romatizmal mitral kapak hastalığı mevcuttu. Üç hastaya daha önce açık mitral komussürotomi ameliyatı uygulanmıştı. Operasyonlarda 19 hastaya mital kapak replasmanı, 6 hastaya mitral kapak rekonstrüksiyon teknikleri uygulandı. Ek prosedür olarak 10 hastaya triküspit kapak rekonstriksiyon teknikleri uygulanırken bir hastaya aort kapak replasmanı, bir hastaya aortik rekonstriksiyon yapıldı. Dört hastada sol atriyal trombüs mevcuttu. Hastaların tamamında kalıcı atriyal fibrilasyon mevcuttu. Onbir hastaya bipolar, 14 hastaya ise unipolar radyofrekans ablasyon yapıldı. Hastaların 20 tanesine sadece sol atriyal ablasyon uygulanırken 5 hastaya hem sol hem de sağ atriyal prosedür uygulandı. 5. Unipolar ablasyon uygulaması Median sternotomiyi takiben, standart kardiyopulmoner bypass tesis edildi. Kross klemp sonrası sol atriyotomi yapıldı. Endokardiyal ablasyon uygulamak için serum irrigasyonlu Cardioblate ® Surgical Ablation Pen (Medtronic model 60813) kullanıldı. Ortalama 10-15 saniye süreyle 25-30 Watt radyofrekans enerjisi kullanıldı (Şekil 8). Sol atriyumda trombüs bulunan vakalarda trombektomi yapıldı. İlk önce sağ pulmoner venler yarımay şeklinde lezyon oluşturarak her iki uçtan sol atriyotomi insizyonuyla birleşecek şekilde izole edildi. (Şekil 9). Daha sonra sol pulmoner venler elips şeklinde lezyon oluşturarak izole edildi. İzole edilen bu iki adacık düz bir hat ile birleştirildi (Şekil 9). Daha sonra sol atriyum apendiksine ve mitral kapak posterior anulusuna sol ven pulmoner adacığından düz bir hatla lezyon oluşturularak prosedür tamamlandı (Şekil 9). Daha sonra sol atriyal apendiksine internal ligasyon yapıldı. Ablasyon işleminden 35 önce dikiş materyali termal hasar görebileceği için işlem tamamlandıktan sonra mitral kapakla ilgili prosedüre geçildi. Ablasyon öncesi çevre dokuların termal hasara uğramaması için sol atriyum arka duvarı ile posterior perikard arasına kuru gazlı bez kondu. Kaşektik hastalar ve sol atriyum duvarı ileri derecede ince olan hastalara prosedür uygulanmadı. Sağ atriyal uygulamada ise (Şekil 10 A) sağ atriyotomiyi takiben insizyonun her iki ucundan vena kava inferior ve vena kava superiora doğru lezyon oluşturuldu. Daha sonra sağ atriyum apendiksinden septal liflete doğru lezyon oluşturuldu. Posterior lifletten sağ atriyum tavanına insizyonla birleşecek şekilde lezyon oluşturuldu (Şekil 10 B). Sağ atriyotomi alt ucundan, fossa ovalisden geçecek şekilde koroner sinüs ostiumuna doğru lezyon oluşturuldu, buradan da posterior liflete ve vena cava inferiora birer lezyon oluşturularak ablasyon işlemi tamamlandı (Şekil 10 C). Apendiks ligatüre edildi ve triküspid kapakla ilgili cerrahi prosedüre geçildi. Kros klemp sonrası her hastaya 600-800mg/gün yükleme dozunda amiodaron infüzyonu başlandı. Her hastaya geçici epikardiyal pacemaker teli yerleştirildi. Dekanülasyonu takiben AF’ye giren hastalara internal elektromekanik kardiyoversiyon uygulandı. 4. Bipolar ablasyon uygulaması Bipolar uygulama için serum irrigasyonlu Cardioblate® BP2 Surgical Ablation Device (medtronic model 60831) kullanıldı. Median sternotomiyi takiben standart kardiyopulmoner bypass tesis edildi yapıldı, sol atriyum değerlendi. Trombüs bulunan vakalarda önce trombektomi yapıldı. Sol pulmoner venler eksplore edildi ve 36 serbestleştirildi, epikardiyal olarak bipolar ablasyon uygulanarak her iki pulmoner ven ada şeklinde izole edildi (Şekil 11 A). Daha sonra sol atriyum apendiksine epikardiyal ablasyon uygulanarak lezyon oluşturuldu. Bipolar kateterin bir ayağı epikardiyal yüzeyde diğeri sol atriyum endokardiyal yüzünde olacak şekilde her iki sağ pulmoner venlerin etrafında lezyon oluşturarak sol atriyotomi insizyonuyla birleştirildi (Şekil 11 B). Ablasyon işlemi tamamlandıktan sonra sol atriyal internal ligasyon yapıldı. Daha sonra mitral kapakla ilgili prosedür tamamlandı. Kros klemp sonrası her hastaya 600800mg/gün yükleme dozunda amiodaron infüzyonu başlandı. Her hastaya geçici epikardiyal pacemaker teli yerleştirildi. Dekanülasyonu takiben AF’ye giren hastalara internal elektromekanik kardiyoversiyon uygulandı. Tablo 2. Operatif veriler Uygulanan Prosedür Mitral kapak replasmanı 19 (% 76) Mitral rekonstrüksiyon 6 (% 24) Ek Prosedür Aort kapak replasmanı 1 (% 4) Aort kapak rekonstrüksiyon 1 (% 4) 37 Trikuspid kapak rekonstrüksiyonu 10 (% 40) Sol atriyum trombektomi 4 (% 16) Ablasyon Bipolar (yalnız sol atriyal prosedür) 11 (% 44) Unipolar 14 (% 56) Yalnız sol atriyum 9 (% 64.2) Sol/ Sağ atriyum 5 (% 35.8) . ____________ AKK (dak) 75.2 ± 20.1 (38-110) TPZ (dak) 101 ± 24.8 (62-150) Hipotermi (C°) 29.6 ± 1.2 (27-32) KPB çıkışı ritm Sinüs 21 ( % 84) AF 2 (% 8 ) Nodal 1 (% 4) Fibroflutter 1 (% 4) KPB çıkışı inotrop 5. 5 (% 20) Postoperatif takip Hasta yoğun bakım ünitesinde tam monitorize olarak izlendi. Ritim takibi 12 derivasyonlu elektrokardiyografi ile yapıldı. Her hastaya postoperatif amiodaron infüzyonu başlandı ve yoğun bakım ünitesinde hastalar ritim açısından tekrar değerlendirildi. Bradikardi gelişen iki hastada amiodaron infüzyonu sonlandırıldı ve geçici pacemaker desteği sağlandı. Elektrokardiyografide PR mesafesi uzayan hastalarda 38 amiodaron infüzyon dozu azaltıldı ve daha sık takip yapıldı. Postoperatif sinüs ritminde olan ve yoğun bakımda AF ritmine dönen hastalara sedatize edilerek elektromekanik kardiyoversiyon uygulandı. Hemodinamik problemi olmayan hastalar servis izlemine alındı. Hastalar antikogulan ve antiaritmik tedavisi planlanarak taburcu edildi. Antiaritmik olarak amiodaron tedavisinin en az üç ay süreyle kullanlması önerildi. Taburcu sonrası ilk hafta ve ilk ay elektrokardiyografi ile takip edildi. Post operatif 3. ayda ekokardiyografi ve elektrokardiyografi takipleri yapıldı. Tablo 3. Postoperatif veriler Yoğun bakımda kalma süresi (gün) 3.2 ±1.4 (1-7) Hastanede kalma süresi (gün) 7.3±2.6 (4-15) Drenaj miktarı (ml) 584±259 EKOKARDİYOGRAFİ Ejeksiyon Fraksiyonu (%) 54.5 ± 10.1 (30-70) Mitral kapak Mak gradiyent (mmHg) 13.28±7.6 (0-34) Mean gradiyent (mmHg ) 5.32±2.9 (0-12) Sol ventrikül diyastol sonu çapı (cm) 5.24± 0.7 (4-7.1) Sol ventrikül sistol sonu çapı (cm) 3.63 ±0.5 (2.4-4.4) Sol atriyum çapı (cm) 5.01 ±0.7 (3.9-6.5) Pulmoner arter basıncı (mmHg) 38.8 ±11.3 (28-60) 39 6. İstatistik Karşılaştırmalar İstatistik analizler SPSS “13.0 for Windows®” programı (SPSS Inc., Chicago, III) kullanılarak gerçekleştirildi. Devamlı değişkenler için ortalama ± standart sapma, kategorik değişkenler için yüzdesel rakamlar verildi. Kategorik değişkenler arasındaki farklar χ2 ve Fisher Exact testi ile; devamlı değişkenler arasındaki testler one-way Anova testi ile değerlendirildi. Paired t test, sol atriyum çaplarındaki pre- ve postoperatif değişiklikler için kullanıldı. P değeri < 0.05 ise anlamlı kabul edildi. 40 SONUÇLAR Onbir hastaya bipolar, 14 hastaya monopolar ablasyon uygulandı. Kardiyopulmoner bypass (KPB) çıkışında 21 hasta normal sinüs ritmine dönmüşken, 2 hasta AF’de, 1 hasta atriyal fibroflatter ritminde, 1 hasta nodal ritimde idi. Yoğun bakım izleminde hastalar tam monitorize edildi ve ritm takibi 12 derivasyonlu elektrokardiyografi (EKG) ile yapıldı. Postoperatif yoğun bakım takibinde KPB çıkışı sinüs ritminde olan 21 hastadan 9 hasta AF’ye girdi. Bu hastalardan 5’ine elektromekanik kardiyoversiyon uygulandı ve 4 hasta tekrar sinüs ritmine dönerken 1 hastada başarılı olunamadı. Dört hastaya farmakolojik kardiyoversiyon denendi fakat başarılı olunamadı. Taburcu olurken 16 hasta (% 64) sinüs ritminde, 8 hasta (% 32) AF’de ve 1 hasta da (% 4) nodal ritimdeydi. Kardiyoversiyon denenen ve başarılı olunamayan hastanın postoperatif 3. aydaki kontrolünde normal sinüs ritmine döndüğü gözlendi. Farmakolojik kardiyoversiyon denenen dört hastadan ikisi postoperatif üçüncü aydaki kontrolde normal sinüs ritminde idi. Sonuç olarak elektromekanik kardiyoversiyon uygulanan beş hastanın tamamı, farmakolojik kardiyoversiyon denenen 4 hastanın 2’si postoperatif 3. ayda sinüs ritminde idi. Postoperatif 3. ayda EKG ve ekokardiyografi takibi yapıldı. Üçüncü ayda yapılan kontrolde toplam 19 hasta (% 76) normal sinüs ritmine dönmüştü. 4 hasta (% 16) halen AF’de, 1 hasta (% 4) fibroflutter ritminde, 1 hasta da (% 4) nodal ritimde idi. Yapılan istatiski değerlendirmede postoperatif 3. aydaki ritim ile sol atriyum çapı, mitral kapak patolojisi, unipolar ve bipolar uygulama, sağ atriyal uygulama karşılaştırıldı (Tablo 1, 2, 3, 4). Sonuçlar arasındaki farklar istatistiki olarak anlamlı değildi. Sol atriyum çapı 5 cm’nin altında olan hastalarda sinüs ritmine dönüş 5 cm’nin üzerinde olanlara göre daha fazla idi, fakat 41 toplam hasta sayısının yetersizliği nedeniyle sonuç istatistiki olarak anlamlı bulunmadı. Hem sağ hem de sol atriyal uygulama yapılan hastalarda yalnızca sol atriyal uygulama yapılanlara göre daha fazla sinüs ritmi elde edildi fakat hasta sayısı yetersiz olduğu için istatistiki olarak anlamlı sonuç elde edilemedi. Preoperatif ve postoperatif diğer verilerle yapılan değerlendirmede sinüs ritmine dönme oranına etkili faktör bulunamadı. Erken dönemde bipolar ve monopolar uygulamaya bağlı komplikasyon görülmedi. Mortalite ve morbidite izlenmedi. Kalıcı pacemaker ihtiyacı toplam bir hastada görüldü (%4). Bir hastada postoperatif atrial fibroflatter gelişti (%4). Bu hastaya sadece sol atriyal prosedür uygulanmıştı. AF ritminde taburcu edilen bu hasta postoperatif 8. ayda presenkopa yol açan ve multiple pause atakları olan yavaş geçişli fibroflatter ritminde başvurdu ve Holter tetkiki sonucunda kalıcı pacemaker implantasyonu uygulandı. Geç dönemde meydana gelen bu komplikasyon bu prosedürün uygulandığı diğer kliniklerde görülen kalıcı pacemaker gereksinim oranına yakındı. Atriyal fibrilasyonla taburcu edilen bir hastada post operatif 2. ayda serebrovasküler olay gelişti ve bu hasta sağ hemiparezi ile takip edilmektedir. Sosyokültürel düzeyi düşük olan bu hastada serebrovasküler olayın muhtemel nedeni antikoagülan kullanımındaki düzensizliktir. Postoperatif sinüs ritminde takip edilen bir hasta postoperatif 3. ayda mitral mekanik kapakta ileri dehissens ve mitral yetmezliği nedeniyle reoperasyona alındı. Bu operasyon sonrası kalıcı tam blok gelişerek kalıcı pacemaker implantasyonu uygulandı. Bu hastada kalıcı pacemaker gereksinimin nedeni uygulanan prosedüre bağlı değildir. Reoperasyonda yapışıklıklar nedeniyle mitral kapağa transeptal olarak yaklaşılmak zorunda kalınmıştır ve kalıcı blok gelişmesinin muhtemel nedeni atriyal septuma yapılan insizyondur. Mitral rekonstriksiyon yapılan ve sinüs ritminde takip edilen bir hasta postoperatif 4. ayda mitral yetmezliği ve akciğer ödemi ile reoperasyon planlanarak interne edildi. Hasta 42 yoğun bakım izleminde serebrovasküler olay geçirerek reoperasyona alınmadan kaybedildi. Romatizmal mitral kapak hastalığı olan hastalarda mitral kapak cerrahisi ile eşzamanlı yapılan radyofrekans ablasyon yöntemi ile elde edilen kardiyoversiyon oranı erken postoperatif dönemde tatmin edici düzeyde bulundu. Bu yöntem, uygun hasta profili seçildiğinde ve titiz bir uygulamayla hastalar bir protokole göre takip edildiğinde özellikle mitral kapak tamir operasyonları ile birlikte uygulandığında başarılı, Cox Maze III prosedürüne göre komplikasyon oranı düşük, tedavi maliyetini azaltan, etkili ve kolay uygulanabilir bir yöntemdir. 43 Tablo 1. Mitral kapak hastalığı ile postoperatif III. aydaki ritmin karşılaştırılması TOPLAM 3. ay sonunda ritim MİTRAL KAPAK md my PATOLOJİSİ miks TOPLAM NSR AFR FiBROFLATTER 9 3 1 13 1 0 0 1 9 2 0 11 19 5 1 25 P=0.843 Tablo 2.Unipolar ve bipolar uygulama ile postoperatif III. aydaki ritmin karşılaştırılması 3. ay sonunda ritim AFR FiBROFLATTER 12 2 0 14 7 3 1 11 19 5 1 25 NSR UNİPOLAR-BİPOLAR unipolar bipolar TOPLAM TOPLAM P=0.335 44 Tablo 3. Sağ atriyal uygulama ile postoperatif III. aydaki ritmin karşılaştırılması TOPLAM 3.ay sonunda ritim NSR AFR FiBROFLATTER 14 5 1 20 5 0 0 5 19 5 1 25 YAPILMADI SAĞ ATRİYAL ABLASYON YAPILDI TOPLAM P=0.373 Tablo 4. Sol atriyum çapı ile postoperatif III. aydaki ritmin karşılaştırılması 3. ay sonunda ritim SOL ATRİYUM ÇAPI TOPLAM TOPLAM NSR AFR FiBROFLATTER >5cm 9 4 0 13 <5cm 10 1 1 12 19 5 1 25 P=0.244 45 TARTIŞMA Atriyal fibrilasyon mortalite ve morbiditeyi önemli oranda arttırmanın yanı sıra hastaların yaşam kalitesini önemli ölçüde bozmakta ve sosyoekonomik olarak önemli bir yük getirmektedir. Dolaşım sistemi ile ilgili hastaneye yatışların yaklaşık %10 aritmi nedeniyledir ve bunun büyük kısmını AF ve atriyal flatter oluşturmaktadır (24). Mitral kapak hastalığı nedeniyle ameliyat olan hastaların büyük kısmı atriyal fibrilasyon ritmindedir. İntermitan veya bir yıldan kısa süreli AF’u hastalarda mitral kapak ameliyatı sonrası ritim genellikle sinüse dönmektedir fakat kronik atriyal fibrilasyonda bu oran oldukça düşüktür (19, 20). Mitral kapak hastalığı ile kronik AF’nin birlikte olduğu durumlarda, sadece kapağa yönelik cerrahi girişim sonrası, olguların %80’inden fazlasında AF’nin sebat ettiği görülmüştür (20). Melo tarafından yapılan bir çalışmada ise ameliyat sonrası spontan sinüs ritmine dönüş %8 olarak bildirilmiştir (21). Cox Maze Prosedürü yapısal kalp hastalığı ve atriyal fibrilasyonu olan hastalarda sinüs ritminin tesisinde oldukça efektif ve yaygın kabul görmüş bir yöntemdir (8). Toplam 346 hastayı içeren ve tüm olguları kapsayan Cox (44) tarafından yayınlanan en büyük seride operatif mortalite %2 idi. AF hastaların %99’unda tedavi edilmiştir ve hastaların sadece %2’si uzun vadeli post-operatif antiaritmik ilaç tedavisine ihtiyaç duymuştur. Geçici postoperatif AF hastaların %38’inde görüldü. Bu sorun, peroperatif dönemdeki kısa atriyal refrakter döneme atfedildi ve uzun vadeli sonuçları etkilemedi (56). Hastaların %15’inde operasyon sonrası kalıcı pacemaker ihtiyacı duyuldu. Sağ atriyal transport fonksiyonu 46 hastaların %98’inde görüldü ve sol atriyal transport fonksiyonunun görülme oranı da %93’tü (44). Diğer merkezlerin Cox Maze III prosedürü ile ilgili sonuçları (59, 60) Cox Maze ve ark. tarafından rapor edilenlerden daha düşük olmuştur. Cleveland Kliniği’nde ve Mayo Klinik’te AF’yi iyileştirme oranı %90 civarında rapor edilmiştir (59,61). Ek organik kalp hastalığının varlığı Cox ve arkadaşlarının çalışmalarında Cox Maze III prosedürünün etkinliğini ortadan kaldırmamasına rağmen, diğer araştırmacılar düşük oranda başarı rapor etmişlerdir. Çoğu seride, mitral kapak cerrahisinin Cox Maze III ile kombine edilmesi hastaların % 7582’sinde AF’yi tedavi etmiştir (62,63,64,65). Kamata ve arkadaşları (64,66) atriyal fibrilasyon dalgasındaki oynama genişliğinin (amplitüd) ve sol atriyum çapının bu hastalarda yürütülen Cox Maze prosedüründen sonraki sinüs ritmi tesisinin bağımsız prediktörleri araştırmacıların sonuçlarının olduğunu bulmuşlardır. Neden diğer Cox ve arkadaşlarınınkinden düşük olduğu belirsizdir. Cox ve arkadaşları maze prosedürünü çoğunlukla lone uygulamışlardır, fakat diğer araştırmacılar maze prosedürünü ilaç AF’de tedavisine dirençli ve açık kalp cerrahisi gerektiren ek kardiyak patolojisi olan hastalarda tercih etmektedirler. Bununla birlikte bu yöntemin oldukça komplike olması, uygulamanın uzun sürmesi, uygulamanın tecrübe gerektirmesi bu konuda calışan araştırmacıları daha basit ve minimal invaziv yöntemler konusunda arayışa itmiştir. Parsiyel maze prosedürleri olarak adlandırılan bu yöntemlerde birçok lezyon setleri oluşturulmuştur (36,37,46,47). Çeşitli gruplar parsiyel Maze prosedürlerinin sonuçlarını yayınlamışlardır (36,37,46,47). Bu araştırmacılar 47 hastaların %80’inde sinüs ritmini tesis etmişlerdir (46,50). İnsizyon ve kriyolezyon paternindeki küçük varyasyonlar sonucu etkilememiştir. Parsiyel maze prosedürleri sol atriyum kaynaklı AF’yi ortadan kaldırabilmesine rağmen, sağ atriyum kaynaklı atriyal flatter riski halen devam etmektedir (67,68,69). Bu prosedürlerden sonra atriyal flatterin ortaya çıkma olasılığı %5-10’dur ve bunun kateter ile ablasyonu kolaydır. Bu yöntemler Cox maze prosedürüne göre daha az invazivdir. Haissaguerre ve ark.(33) paroksismal AF’nin vakaların %94’ünde pulmoner venlerdeki ektopik atımlardan kaynaklandığını ortaya koyduğu çalışma ve sol atriyuma yönelik bu işlemlerin başarılı olması aynı lezyon setlerinin farklı enerji kaynakları kullanılarak elde edilebileceği fikrini doğurmuştur. Radyofrekans ablasyon 1980’lerin ortalarından bu yana perkütan kateter aracılığıyla özellikle supraventriküler taşikardilerin tedavisinde kullanılmaktadır. Ucu serum irrigasyonlu radyofrekans ablasyonu ilk olarak 1988 yılında Wittkampf ve arkadaşları (73) tarafından kullanılmıştır. Bu kateterin kronik AF’de intraoperatif olarak kullanımı ilk olarak 1995 yılında Sie ve arkadaşları (74), daha sonra ise Melo ve arkadaşları (75) tarafından gerçekleştirilmiştir. Radyofrekans ablasyon amacıyla çeşitli lezyon tipleri oluşturulmuştur (62, 71, 78). Bu lezyon tiplerinin tamamı pulmoner venlerin tamamen veya tama yakın izolasyonunu, sol atriyum apendiksinin eksizyonunu veya dışlanmasını içerir. Ayrıca sol pulmoner venler ile sol atriyum apendiksi arasında ve yine sol pulmoner venler ile mitral kapak anulusu arasında lezyon oluşturarak iletinin engellenmesini içerir. Sağ atriyal uygulamalar ise Cox Maze III prosedürüne benzer şekilde yapılır (78,79) (Şekil 7). Sol atriyal uygulama ortalama 10-20 48 dakika sürmektedir. Bu süre Cox Maze III prosedürünü gerçekleştirmek için gerekli 1 saatlik süreden oldukça kısadır (62, 71, 77, 81, 85). Bu lezyon tiplerinin çeşitli olmasına rağmen AF’nin tedavi oranı %70 ile %80 arasında bildirilmiştir (71,78, 81, 82, 83, 84). Bu yeni teknikler AF’yi efektif bir şekilde tedavi etmenin yanı sıra. kardiyopulmoner bypass süresi kısalttığından ve komplikasyon görülme sıklığı azalttığından oldukça düşük morbidite ve mortaliteye sahiptir. Bu prosedürlerin en önemli başarısı Cox maze prosedüründeki gibi tam lezyon seti oluşturmadan, kısmi lezyon oluşturularak AF’nin başarılı bir şekilde tedavi edilebileceğini göstermeleridir. Tedavi edilen hastaların çoğu organik kalp hastalığına sahipti ve ek olarak mitral kapak ameliyatı geçirmişlerdir. Bu hastalarda elde edilen başarı hemen hemen Cox Maze prosedürüne yakındır ve sağ atriyumun prosedüre dahil edilip edilmemesinden bağımsızdır (44, 59, 60). Peroperatif AF yaygındır ve vakaların yaklaşık üçte ikisinde görülür (71, 84, 85). Hastaların %30-40’nın AF ile hastaneden ayrılmasına rağmen, bir çoğu takip eden 3 ay içinde sinüs ritmine dönmektedir. Bu nedenle AF ile taburcu, prosedürdeki başarısızlığın göstergesi değildir. Ablasyon sonrası elektromekanik veya farmakolojik kardiyoversiyon önem taşımaktadır, sinüs ritmi tesis edildikten sonra farmakolojik olarak desteklenmeli ve hastanın sinüs ritminde kalması sağlanmalıdır. Amiodaron ve sotalol tedavisi postoperatif artiyal fibrilasyonun profilaksisinde tercih edilmektedir. Mitral kapak replasmanı gereken hastalarda maze prosedürünün uygulanması halen tartışmalı bir konudur çünkü mekanik kapak replasmanı yapılan hastalarda sinüs ritmi tesis edilse dahi antikoagülan tedavi ihtiyacı ömür boyu devam etmektedir. Fakat mitral rekonstrüksiyon yapılan hastalarda sinüs ritminin tesisi antikoagülan tedavi gereksinimini ortadan 49 kaldıracağından maze önerilmektedir. Bununla prosedürünün birlikte bu AF’nin hasta gurubuna antikoagülan uygulanması tedaviye rağmen tromboemboli riskini arttırdığını düşünen cerrahlar ise maze prosedürünün rutin uygulanmasını savunmaktadırlar. Bu konuda daha fazla randomize çalışmaya ihtiyaç duyulmaktadır. Epikardiyal ve bipolar ablasyon prosedürü endokardiyal yaklaşıma göre daha yeni bir uygulamadır ve literatürde şu ana kadar bildirilen komplikasyonlar endokardiyal uygulamalardan oluşmuştur. Kullanılan prob ne olursa olsun, özellikle sol atriyal ablasyon esnasında; özofagus, sirkumfleks koroner arter ve sol ana bronş yaralanmaları veya sol atriyum perforasyonuna bağlı kanamalar gelişebilir. Endokardiyal uygulamada karşılaşılan en fatal komplikasyon özofagus yaralanmasıdır (88). Sağ ve sol pulmoner ven ağızlarının iki ayrı ada halinde çevrelenmesi ve bu ikisinin birleştirilmesi esnasında sol atriyum arka duvarına yakın komşuluğundan dolayı özofagus hasar görebilir. Sol atriyum ile özofagus arasında bazen hiç bağ dokusu bulunmayabilir (özellikle kaşektik hastalarda). Bu yüzden, işlem esnasında eğer varsa TEE probu ve nazogastrik sonda çıkarılmalıdır. Oblik sinüse gazlı bez yerleştirilmesi de hasar oluşma olasılığını en aza indirecektir. Ayrıca sol atriyal dairelerin kesişmemesine özen gösterilmelidir çünki aynı dokuya ikinci kez enerji uygulamak perforasyon riskini arttırmaktadır (89). Doll ve Mohr (88 ), 387 hastaya radyofrekans ablasyon uygulamışlar ve dört hastada ( %1 ) özofagus perforasyonu geliştiğini bildirmişlerdir. Sol atriyal endokardiyal uygulamada pulmoner adacıklar mitral kapak anulusu ile birleştirilirken, anatomik varyasyona göre, termal hasara maruz kalabilir. Bu etkiyi en aza indirmek için işlem esnasında retrograd soğuk 50 kardiyopleji verilmesi önerilmektedir (90). Sirkumfleks arter yaralanmasına kriyoablasyon ile kombine Maze operasyonu sırasında da rastlanılmıştır (91). Endokardiyal radyofrekans uygulamada karşılaşılan diğer komplikasyon ise, sol atriyum arka duvarına yakın komşuluğundan dolayı sol ana bronş yaralanmasıdır. Bu yüzen ablasyon işlemine başlamadan önce elle palpasyon yapılmalı ve sol ana bronşa ait çıkıntı hissedilerek ablasyon buna göre şekillenmelidir (92). Ablasyon işlemi sol atriyum apendiksinin internal ligasyonundan sonra yapıldığında, dikiş materyeli hasar görebilir ve buna bağlı kanama görülebilir (93). Bu yüzden ablasyon işlemi her zaman diğer tüm cerrahi işlemlerden (kapak replasmanı, rekonstrüksiyon..) önce yapılmalıdır. Atriyum çapları ileri genişlemiş ve duvar yapısı ince olan hastalarda ablasyon süresi kısa tutulmalı ve uygulanan enerji miktarı az olmalıdır. Pulmoner ven stenozuna perkütan uygulamalarda rastlanmakla birlikte, pulmoner ostiumlara en az 3-4 mm uzaklıkta yapılacak uygulamanın güvenli olacağı bildirilmiştir (94). Diğer bir komplikasyon ise kalıcı pacemaker gereksinimi duyulan ritim ( nodal ritim, a-v tam blok..) bozukluğudur. Mohr ve arkadaşlarının (90) 243 hastada yaptıkları uygulamada 23 (%9.8) hastaya pacemaker takılmıştır. Maze III prosedürü uygulanan hastalarda ise bu oran %2-24 olarak bildirilmiştir (8, 94). Öncesinde hasta sinüs sendromu olduğu bilinen hastalara bu prosedür uygulanmamalıdır. Bazı araştırmacılar atriyal büyüklüğün başarıyı etkilediğini bildirmelerine rağmen, bu bulgu diğer araştırmacılar tarafından teyit edilmemiştir (62, 78). Sol atriyum çaplarının ileri derecede büyümesi, atriyum duvarının incelmesi, fibrozis ve kalsifikasyon rüptür riski nedeniyle tercih edilmemektedir. Atriyal transport 51 fonksiyonu, sinüs ritmine dönen hastaların %80-100’ünde görülmektedir (86, 87). Elde edilen bu başarı radyofrekans ablasyona olan ilgiyi arttırmaktadır ancak oluşturulan lezyon tipi ve prosedürün sadece sol atriyumu içermesi konusunda halen tartışmalar devam etmektedir. Yakın gelecekte AF için cerrahi uygulamanın yaygın şekilde kullanımını ve enerji kaynaklarında, lezyon setlerinde ve cerrahi yöntemlerde iyileşmeyi göreceğiz. Radyofrekans ve mikrodalga enerjilerinin uygulanması için basit ve daha hızlı teknikler halen gelişim halindedir. Lazer ve ultrason da lezyon yaratmak için alternatif enerji kaynakları olabilir. AF’nin minimal invaziv, offpump ablasyonu ufukta görünmektedir. Cox sağ torakotomi yoluyla bir kriyomaze prosedürünün gerçekleşebileceğini göstermiştir (87). Sol atriyum apendiksi stapler kullanılarak eksize ve eksklude edilebilir (95). Yakın gelecekte, AF’nin torakoskopik stapler ve geliştirilecek kateterler ile off-pump epikardiyal ablasyonu mümkün olacaktır. 52 ŞEKİLLER ŞEKİL 1: SOL ATRİYAL İZOLASYON PROSEDÜRÜ 53 ŞEKİL 2: HİS DÜĞÜMÜ ABLASYON ŞEKİL 3 : KORİDOR PROSEDÜRÜ 54 ŞEKİL 4: Sueda prosedüründeki sol atriyal insizyon paterni. Pulmoner venlere dairesel bir şekilde insizyon yapılır ve sol atriyum apendiksine ve mitral anulusuna doğru birleştirici insizyon yapılır. 55 ŞEKİL 5: COX MAZE III PROSEDÜRÜ A) B) 56 ŞEKİL 6: MİNİ-MAZE PROSEDÜRÜ ŞEKİL 7: RADYOFREKANS ABLASYONDA LEZYON SETLERİ 57 ŞEKİL 8: ORTALAMA LEZYON DERİNLİĞİ VE ABLASYON ZAMANI Ortalama lezyon derinliği ve ablasyon zamanı *95%güvenilirlik Ortalama derinlik(mm) 8 7 --- 30 watts 5cc/dak 6 --- 25 watts 5cc/dak 5 --- 20watts 5cc/dak 4 3 2 1 0 0 5 10 15 20 25 30 35 40 (zaman (sn/1cm²) ŞEKİL 9: UNİPOLAR ABLASYON SOL ATRİYAL UYGULAMA mitral kapak ve anulus kırmızı: cerrahi insizyon hattı mavi: radyofrekans ablasyon hattı 58 ŞEKİL 10 : UNİPOLAR RF SAĞ ATRİYAL UYGULAMA ŞEMASI kırmızı: cerrahi insizyon hattı mavi: radyofrekans ablasyon hattı A) vcs vcı B) triküspid kapak 59 C) koroner sinüs ŞEKİL 11. BİPOLAR RF ABLASYON UYGULAMA ŞEMASI A) 60 B) 61 KAYNAKLAR 1. Silverman ME. From rebellious palpitations to the discovery of auricular fibrillation: contributions of Mackenzie, Lewis and Eindhoven. Am J Cardiol 1994;73:384-9. 2. Martin A, Schwartz MJ, Kronmal RA, Kosinski AS. Prevalence and significance of atrial fibrillation in coronary artery disease (CASS Registry) . Am J Cardiol 1988;61:7147-71. 3. Kannel WB, Abbott RD, Savage DD, McNamara PM. Epidemiologic features of chronic atrial fibrillation: the Framingham study. N Engl J Med 1982; 306:1018-22 4. Benjamin EJ, Wolf PA, D’Agostino RB, Silbershatz H, Kannel WB, Lewy D . Impact of atrial fibrillation on the risk of death: the Framingham Heart Study. Final results. Circulation 1991;84:527-39. 5. . Ezekowitz M.D and Netrebko P.I. Anticoagulation in management of atrial fbrillation. Current Opinion in Cardiology 2003;18:26-31 6. Lundstrom T. and Ryden L. Chronic atrial fibrillation. Long-term results of direct current conversion. Acta Medica Scandinavica 1988;223:53-9. 7. Graffigna A, Pagani F, Minzioni G , Salerno J, Vigano M. Left atrial isolation associated with mitral valve operations. Ann Thorac Surg. 1992;54:1093-1097; discussion 1098. 8. Cox JL , Schuessler RB, Lappas DG, Boieneau JP. An 8 ½ -year clinical experience with surgery for atrial fibrillation . Ann Surg. 1996; 224:267273;discussion 273-275. 62 9. Sealy WC, Hattler BG jr, Blumenshein SD, Cobb FR. Surgical treatment of Wolf-Parkinson-White syndrome. Ann Thorac Surg 1969;81-11. 10. Scheinman MM, Morady F, Hess DS, Gonzales R. Catheter-induced ablation of the atrioventricular junction to control refractory supraventricular arrhythmias. JAMA 1982;248:851-5. 11. Gallagher JJ, Svenson RH, Kasell JH, et al. Catheter technique for closedchest ablation of the atrioventricular conduction system. N engl J Med 1982;306:194-200. 12. Williams JM, Ungerleider RM, Lofland GK, Cox JL. Left atrial isolation: new technique for the treatment of supraventricular arrhythmias. J Thorac Cardiovasc Surg. 1980;80:373-380. 13. Guiraudon GM, Campell CS, Jones DL, et al. Combined sino-atrial node atrio-ventricular node isolation: A surgical alternative to His Bundle ablation in patients with atrial fibrillation. (Abs.) Circulation 1985;72:III220. 14. Fuster V, Ryden LE, Asinger RW, et al. ACC/AHA/ESC guidelines for the management of the patients with atrial fibrillation. Eur Heart J 2001;22:1985-923. 15. Lip GYH. Does atrial fibrillation confer a hypercoagulable state? Lancet 1995;346:1313-4. 16. Peterson P, Kastrup J, Wilhelmsen R, Schutten HJ. Atrial natriuretic peptide in atrial fibrillation before and after electrical cardioversion therapy. Eur Heart J 1988;9:639-41. 63 17. Shinbane JS, Wood MA, Jensen DN, Ellenbogen KA, Sheinman MM, Tachycardia-induced cardiomyopathy: a rewiev of animal models and clinical studies. J Am Coll Cardiol 1997;29:709-15. 18. Pasty BM, Manolio TA, Kuller LH, et al. Incidence of the risk factors for the atrial fibrillation in older adults. Circulation 1997;96:2555-61. 19. Diker E, Aydogdu S, Ozdemir M, et al. Prevalence and predictors of the atrial fibrillation in rheumatic heart disease. Am J Cardiol 1996;77:96-8. 20. Handa N, Schaff HV, Morris JJ, Anderson BJ, et al. Outcome of mitral valve repair and the Cox Maze procedure for mitral regurgitation and associated atrial fibrillation. J Thorac Cardiovasc Surg 1999;118;628-635. 21. Melo J, Adrago P, Neves J, et al. Surgery for atrial fibrillation using radiofrequency catheter ablation: assessment of results at one year. Eur J Cardio-thorac Surg 1999;155:851-855. 22. Brand FN, Abbott RD, Kannel WB, Wolf PA. Characteristics and prognosis of lone atrial fibrillation: 30-year follow-upin the Framingham study. J Am Med Assoc. 1985;254:3449-53. 23. Frustaci A, Chimenti C, Belloci F, Morgante E, Russo MA, Maseri A. Histological substrate of atrial biopsies in patients with lone atrial fibrillation. Circulation 1997;96:1180-1184. 24. Bialy D, Lehmann MH, Schumacher DN, Steinman RT, Meissner MD. Hospitalization for arrhythmias in the United States: Importance of Atrial Fibrillation. JACC 1992;19:716-724. 25. American Heart Association policy document on the atial fibrillation.1988. http:www.americanheart.org/arrhythmia/patient/about-atria.html. 64 26. Chen PS, Athill CA, Wu TJ, Ikeda T, Ong JJ, Karagueuzian HS. Mechanisms of atrial fibrillation and flutter and implication for management. Am J Cardiol 1999;84:125R-30R. 27. Nattel S. New ideas about atrial fibrillation 50 years on. Nature 2002;415:219-26. 28. Moe GK. On the multiple wavelet hypothesis of atrial fibrillation. Arch Int Pharmacodyn 1962;140:183-8. 29. Allessie MA. Atrial electrophysiologic remodeling: another vicious circle? J Cardiovasc Electrophysiol 1998;9:1378-93. 30. Falk RH. Atrial fibrillation. N Engl J Med 2001;344:1067-78. 31. Epstein AE, Kay GN. Finding our way through the maze. J Cardiovasc Electrophysiol 1999;10:1575-7. 32. Roithinger FX, Steiner PR, Goseki Y, Sparks PB, Lesh MD. Electrophysiologic effects of selective right versus left atrial linear lesions in a canine model of chronic atrial fibrillation. Cardiovasc Electrophysiol 1999;10:1564-74. 33. Haissaguerre M, Jais P, Shah DC, et al. Spontaneous initiation of atrial fibrillation by ectopic beats originating in the pulmonary veins. N Engl J Med 1998;339:659-66. 34. Nathan H, Eliakim M. The junction between the left atrium and the pulmonary veins. An anatomic study of human hearts. Circulation 1966;34:412-22. 65 35. Harada A, Sasaki K, Fukushima T, et al. Atrial activation during chronic atrial fibrillation in patients with isolated mitral valve disease. Ann Thorac Surg 1996;61:104-12. 36. Nitta T, Imura H, Bessho R, Hosaka H, Yamauchi S, Tanaka S. Wavelength and conduction inhomogeneity in each atrium in patients with isolated mitral valve disease and atrial fibrillation. J Cardiovasc Electrophysiol 1999;10:521-8. 37. Sueda T, Nagata H, Orihashi K, et al. Efficacy of a simple left atrial procedure for chronic atrial fibrillation in mitral valve operations. Ann Thorac Surg 1997;63:1070-5. 38. Sueda T, Nagata H, Shikata H, et al. Simple left atrial procedure for chronic atrial fibrillation associated with mitral valve disease. Ann Thorac Surg 1996;62:1796-800. 39. Dittrich HC, Erickson JS, Schneiderman T, Blacky AR, Savides T, Nicod PH. Echocardiographic and clinical predictors for outcome of elective cardioversion of atrial fibrillation. Am J Cardiol 1989;63:193-7. 40. Levy S, Lauribe P, Dolla E, et al. A randomized comparison of external and internal cardioversion of chronic atrial fibrillation. Circulation 1992;86:1415-20. 41. Lau CP, Log NS. A comparison of transvenous atrial defibrillation of acute and chronic atrial fibrillation and the effect of intravenous sotalol on human atrial defibrillation threshold. PACE 1997;20:2442-52. 42. Brignole M, Menozzi C, Gianfrancho L, et al. Assessment atrioventricular junction ablation 66 and VVIR pacemaker of versus pharmacological treatment in patients with heart failure and chronic atrial fibrillation. Circulation 1998;98:953-60. 43. Cox JL, Schuessler RB, D’Agostino HJ Jr, et al. The surgical treatment of atrial fibrillation. III. Development of a definitive surgical procedure. J Thorac Cardiovasc Surg 1991;101:569-83. 44. Cox JL, Ad N, Palazzo T, et al. Currrent status of the Maze procedure for the treatment of atrial fibrillation. Semin Thorac Cardiovasc Surg 2000;12:15-9. 45. Cox JL, Schuessler RB, Boineau JP. The development of the Maze procedure for treatment of atrial fibrillation. Semin Thorac Cardiovasc Surg 2000;12:2-14. 46. Takami Y, Yasuura K, Takagi Y, at al. Partial maze procedure is effective treatment for chronic atrial fibrillation associated with valve disease. J Card Surg 1999;14.103-8. 47. Bauer EP, Szalay ZA, Brandt RR, at al. Predictors for atrial transport function after Mini-Maze operation. Ann Thorac Surg 2001;72:1251-5. 48. Cox JL,Ad N.The importance of cryoablation of the coronary sinus during the Maze procedure.Semin Thorac Cardiovasc Surg 2000;12:20-4. 49. Kress DC, Krum D, Chekanov V, at al. Validation of a left atrial lesion pattern for intraoperative ablation of atrial fibrillation. Ann Thorac Surg 2002;73:1160-8. 50. Szalay ZA, Skwara W, Pitschner HF, Faude I, Klovekorn WP, Bauer EP. Midterm results after the Mini-Maze procedure. Eur J Cardiothorac Surg 1999;16:306-11. 67 51. Wonnell TL, Stauffer PR, Langberg JJ.Evaluation of microwave and radio frequency catheter ablation in a myocardium-equivalent phantom model.IEEE Trans Biomed Eng 1992;39:1086-95. 52. Spitzer SG, Richter P, Knaut M, Schuler S. Treatment of atrial fibrillation in open heart surgery-the potential role of microwave energy. Thorac Cardiovasc Surg 1999;47(Suppl 3):374-8. 53. Knaut M, Spitzer SG, Karolyi L, at al. Intraoperative microwave ablation for curative treatment of atrial fibrillation in open heart surgery-the MICROSTAF and MICRO-PASS pilot trial. MICROwave Application in Surgical treatment Atrial Fibrillation in Bypass-Surgery. Thorac Cardiovasc Surg 1999;47(Suppl 3):379-84. 54. Dorschler K, Muller G. The role of laser in cardiac surgery. Thorac Cardiovasc Surg.1999;47:385-387. 55. Viola N, Williams MR, Oz MC, Ad N. The technology in use for the surgical ablation of atrial fibrillation. Semin Thorac Cardiovasc Surg. 2002;14:198-205. 56. Cox JL, Schuessler RB, Boineau JP. The development of the Maze procedure for atrial flutter and atrial fibrillation. Adv Card Surg 1995;6:1-67. 57. Cox JL, Ad N, Palazzo T. Impact of the maze procedure on the stroke rate in patients with atrial fibrillation. J Thorac Cardiovasc Surg 1999;118:833-40. 58. Ad N, Cox JL. Stroke prevention as an indication for the Maze procedure in the treatment of atrial fibrillation. Semin Thorac Cardiovasc Surg 2000;12:56-62. 68 59. McCarthy PM, Gillinov AM, Castle L, Chung M, Cosgrove D 3rd. The Cox-Maze procedure: the Cleveland Clinic experience. Semin Thorac Cardiovasc Surg 2000;12:25-9. 60. Arcidi JM Jr, Doty DB, Millar RC.The Maze procedure:the LDS Hospital experience. Semin Thorac Cardiovasc Surg 2000;12:38-43. 61. McCarthy PM, Castle LW, Maloney JD, et al.Initial experience with the maze procedure for atrial fibrillation. J Thorac Cardiovasc Surg 1993;107787. 62. Chen MC, Chang JP, Guo GB, Chang HW. Atrial size reduction as a predictor of the success of radiofrequency maze procedure for chronic atrial fibrillation in patients undergoing concomitant valvular surgery. J Cardiovasc Electrophysiol 2001;12:867-74. 63. Raanani E, Albage A, David TE, Yau TM, Armstrong S. The efficacy of the Cox/maze procedure combined with mitral valve surgery: a matched control study. Eur J Cardiothorac Surg 2001;19:438-42. 64. Kamata J, Kawazoe K, Izumoto H, et al. Predictors of sinus rhythm restoration after Cox maze procedure concomitant with other cardiac operations. Ann Thorac Surg 1997;64:394-8. 65. Izumoto H, Kawazoe K, Kitahara H, Kamata J. Operative results after the Cox/maze procedure combined with a mitral valve operation. Ann Thorac Surg 1998;66:800-4. 66. Ueshima K, Hashimoto K, Chiba M, et al. What are the predictors of restoration of sinus rhythm after combined treatment with surgical repair for 69 organic heart disease and the Maze procedure for atrial fibrillation? J Cardiovasc Surg (Torino) 1999;40:793-6. 67. Mohr FW, Fabricus AM, Falk V, et al. Curative treatment of atrial fibrillation with intraoperative radiofrequency ablation: short-term and midterm results. J Thorac Cardiovasc Surg 2002;123:919-27. 68. Usui A, Inden Y, Mizutani S, Takagi Y, Akita T, Ueda Y. Repetetive atrial flutter as a complication of the left-sided simple maze procedure. Ann Thorac Surg 2002;73:1457-9. 69. Deneke T, Khargi K, Grewe PH, et al. Left atrial versus bi-atrial Maze operation using intraoperatively cooled-tip radiofrequency ablation in patients undergoing open-heart surgery: safety and efficacy. J Am Coll Cardiol 2002;39:1644-50. 70. Gaita F, Gallotti R, Calo L, et al. Limited posterior left atrial cryoablation in patients with chronic atrial fibrillation undergoing valvular heart surgery. J Am Coll Cardiol 2000;36:159-66. 71. Williams MR, Stewart JR, Bolling SF, et al. Surgical treatment of atrial fibrillation using radiofrequency energy. Ann Thorac Surg 2001;71:1939-44. 72. Haissaguerre M, Jais P, Shah DC, et al. Right and left atrial radiofrequency catheter therapy of paroxysmal atrial fibrillation. J Cardiovasc Electrophysiol. 1996;7:1132-1144. 73. Wittkampf FH, Hauer RN, Robles de Medina EO. Radiofrequency ablation with a coolet porous electrode catheter. J Am Coll Cardiol 1988;11:17. 70 74. Sie HT, Ramdal Misier R, Beukema WP. Radiofrequency ablation of atrial fibrillation in patients undergoing mitral valve surgery: first experience. Circulation 1996;94:1-675. 75. Melo J, Adragao P, Neves J, et al. Surgery for atrial fibrillation using radiofrequency catheter ablation: assessment of results at one year. Eur J Cardio-thorac Surg 1999;155:851-855. 76. Shimoike E, Kaji Y, Ueda N, Maruyama T, Kanaya S, Niho Y. In vivo and in vitro study of radiofrequency application with a new long linear probe: implication for the maze operation. J Thorac Cardiovasc Surg 2000;120:164-72. 77. Gaita F, Riccardi R, Calo L, et al. Atrial mapping and radiofrequency catheter ablation Electrophysiological in patients findings with and idiopathic ablation atrial fibrillation. results. Circulation 1998;97:2136-45. 78. Sie HT, Beukema WP, Misier AR, et al. Radiofrequency modified maze in patients with atrial fibrillation undergoing concomitant cardiac surgery. J Thorac Cardiovasc Surg 2001;122:249-56. 79. Chen MC, Guo GB, Chang JP, Yeh KH, Fu M. Radiofrequency and cryablation of atrial fibrillation in patients undergoing valvular operations. Ann Thorac Surg 1998;65:1666-72. 80. Nakagawa H, Yamanashi WS, Pitha JV, et al. Comparasion of in vivo tissue temperature profile and lesion geometry for radiofrequency ablation with a saline-irrigated electrode versus temperature control in a canine thigh muscle preparation. Circulation. 1995;91:2264-2273. 71 81. Hindricks G, Mhor FW, Autschbach R, Kottkamp H. Antiarrhythmic surgery for treatment of atrial fibrillation-new concepts. Thorac Cardiovasc Surg 1999;47(Suppl 3):365-9. 82. Sie HT, Beukema WP, Ramdat Misier AR, Elvan A, Ennema JJ, Wellens HJ. The radiofrequency modified maze procedure. A less invasive surgical approach to atrial fibrillation during open-heart surgery. Eur Cardiothorac Surg 2001;19:443-7. 83. Nitta T, Lee R, Schuessler RB, Boineau JP, Cox JL. Radial approach: a new consept in surgical treatment for atrial fibrillation I. Consept, anatomic and physiologic basis and development of a procedure. Ann Thorac Surg 1999;67:27-35 84. Pasic M, Bergs P, Muller P, et al. İntraoperative radiofrequency maze ablation for atrial fibrillation: the Berlin modification. Ann Thorac Surg 2001;72:1484-91. 85. Benussi S, Pappone C, Nascimbebe S, et al. A simple way to treat chronic atrial fibrillation during mitral valve surgery: the epicardial radiofrequency approac. Eur J Cardiothorac Surg 2000;17:524-9. 86. Gillinov AM, Petterson G, Rice TW. Esophageal injury during radiofrequency ablation for atrial fibrillation. J Thorac Cardiovasc Surg 2001;122:1239-40. 87. Cox JL. The minimally invasive Maze-III procedure. Oper Tech Thorac Cardiovasc Surg 2000;5:79-92. 72 88. Doll N, Borger MA, Fabricus A, et al. Esophageal perforation during left atrial radiofrequency ablation: Is the risk too high? J Thorac Cardiovasc Surg. 2003;125:836-842. 89. Patwardhan AM. Esophageal injury during radiofrequency ablation for atrial fibrillation: Inherent safety of radiofrequency bipolar coagulation. J Thorac Cardiovasc Surg.2001;122:1241-1242. 90. Mohr FW, Fabricus AM, Falk V, et al. Curative treatmaent of atrial fibrillation with intraoperative radiofrequency ablation: short-term and midterm results. J Thorac Cardiovasc Surg. 2002;123:919-927. 91. Sueda T, Shikata H, Mitsui N, Nagata H, Matsuura Y. Myocardial infarction after a maze procedure for idiopathic atrial fibrillation. J Thorac Cardiovasc Surg.1996;112:549-550. 92. Benussi S, Nascimbene S, Calvi S, Alfieri O. A tailored anatomical approach to prevent complications during left atrial ablation. Ann Thorac Surg. 2003;75:1979-1981. 93. Guden M, Akpınar B, Sanisoglu I, Sagbas E, Bayindir O. Intraoperative saline-irrigated radiofrequency modified maze procedure for atrial fibrillation. Ann Thorac Surg. 2002;74:1301-1306. 94. Arcidi JM, Millar RC. Evolution of the Maze III procedure: are modifications necessary? Thorac Cardiovasc Surg.1999;47:362-364. 95. Landymore R, Kinley CE. Staple closure of left atrial appendage. Can J Surg 1984;27:144-5. 73 74