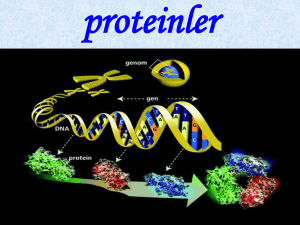
Proteomiğe Genel Bakış
Genomun tüm protein komplementlerini (proteom) çalışan bilim dalı Proteomiks olarak
adlandırılmaktadır. Proteomiks ve proteom terimleri Marc Wilkins ve arkadaşlarınca 1990
larda türetilmiştir. Bu kelimeler tüm bir organizmadaki tüm genlerin kolleksiyonlarını ifade
eden genomiks ve genom kelimelerinin yansımalarıdır. Omiks ‘omics’ terimi biyoloji ve
yaşayan sistemler hakkında nasıl düşündüğümüzün yeniden tanımlanmasını sembolize eder
(Şekil 1).
Şekil1: Genomiks ve proteomiksin biyokimyasal konteksti
Genom, bir organizmanın bütün DNA’sı, bir başka deyişle, genetik yapısı olarak da ifade
edilebilir. Değişik organizmaların büyüklükleri önemli farklılıklar gösterirler. Örneğin E.coli
bakterisinde genom 4,5x106 baz çiftinden oluşmuşken, insanda 3,2x109 baz çiftine ulaşır.
Bitki, hayvan gibi çok hücreli canlılarda hemen her hücre tam genomu içerir (insanda olgun
alyuvarlar genom içermezler). İnsan genomu, 50-250 milyon baz çifti içeren 24 kromozom
halinde düzenlenmiştir. Bu kromozomlara dağılmış olan genlerin sayısı, yaklaşık 35 bin
kadardır. Genler, organizmadaki işlevsel moleküller olan proteinleri kodlarlar. Bütün
genomun ancak y a k l a şı k %2’sini oluşturan genlerin içerdiği dizim hataları (mutasyonlar),
organizmalarda yapı
ya da işlev bozukluklarına, bir başka deyişle hastalıklara neden
olabilirler. 1945’te ABD Kongresi,Enerji Bakanlığının yeni enerji kaynakları ve teknolojileri
geliştirmekle, bu yeni enerjilerin üretim ve kullanımının sağlık ve çevre açısından sakıncaları
olup olmadığının derinlemesine araştırılmasıyla görevlendirdi. 1986’da Enerji Bakanlğı,
belirtilen görevinin çerçevesinde insan genomu dizisinin belirlenerek bir referans oluşturması
için insan Genomu girişimini başlattı ve Ulusal Sağlık Enstitülerinin de işbirliğiyle 1990’da
“İnsan Genom Projesi" başlatıldı. İnsan Genomu Projesinin temel amacı, tüm insan
genomunun dizisini ve bütün genlerini belirleyerek bir kaynak oluşturmaktı. Bunun yanı s›ra
diğer organizmalarn da genom dizilerini belirleyerek insanınkiyle karşılaştırmak, bunun
gerçekleştirilmesi için yeni teknikler geliştirmek ve elde edilecek bilgileri tarım,sağlık, çevre,
enerji gibi alanlarda değerlendirmektir.
Genomiks ve açılımı genom projesi görevini gerçekleştirirken bu fikirden doğan proteomiks
kavramı hızla gelişmeye başladı.
1990 ları ortalarına kadar , biyokimyacılar, moleküler biyologlar ve hücre biyologları belirli
genler, proteinler ya da spesifik biyokimyasal yollorla ilişkili unsurların küçük gruplarını
çalışıyordu. Northern blot (gen ekspresyonu için) ve Westhern blot (protein düzeyleri için)
yerlerine kullanılanılabilecek yeni teknikler az miktardaki gen ya da proteinin zor analitik
işlerinden daha fazlasını yapabilmeyi sağlayacaktı.
Üç gelişim biyolojik peyzajı tamamiyle değiştirdi ve yeni biyolojinin temelini oluşturdu.
Bunlardan ilki 1990lar boyunca genlerin (EST, ve protein sekans databazları) gelişimi
üzerineydi. Bu çalışmalar bir takım organizmaların eksprese ( ifade ) genlerinin kismi
katologlanmasından daima daha fafdalı hale dönüştü. 1990 ların sonlarındaki
sekanslama projeleri bakteri, maya, nematod, drosophila ve
genom
yakınlarda sonlanan insan
genomuyla ürnlerini verdi. Bitki genomları veya hayvanlar üzerindeki genom çalışmalarının
bir kısmıda tamamlandı. Bu genom databazları düzgün bir şekilde katologlanarak yaşayan
sistemler üzerinde bilgilerimizin çok daha fazlasını anlayabilmek için kullanılacaktır.
İkinci kilit gelişme; bu veri tabanlarından çıkarılacak bilgi için kullanımı kolay olan,
depolama temelli yöntemler üzerinde olmuştur. Bu web temelli ücretsiz
yöntemler
biyologlara probe yapımı, genlerin fonksiyonu, gen ürünleri gibi pekçok veriye ulaşmasını
sağlamaktadır.
Üçüncü kilit gelişme ise oligonükleotid mikroarraylerdir. Bu yöntem bir cip üzerindeki gen
spesifik oligonükleotid veya cDNA sekanslarınının bir serisini içerir. Array’e çalışılmak
istenilen örneğin floresan işaretli DNA’ sının karışımı eklenir ve bir seferde binlerce genin
ekspresyonu incelenebilir. Bir array binlerce Northern-blot analizinin yerine geçebilir ve bir
Northern in alacağı zaman kadar bir sürede tamamlanacaktır. Bunun ötesinde iki renkli
floresans prob işaretlenerek iki farklı örneğin genlerinin ekspresyonu bir slide veya cip
üzerinden direk olarak karşılaştırılabilir.
Şekil2: Cip üzerinde mayanın genomu vardır. Bu maya cDNA microarray’i Stanford
Üniversitesinde
Dr.
Patrict
Brown’nın
labratuvarında
üretilmiştir.
(http://cmgm.stanford.edu.pbbrown/)
Sacchromyces cerevisiea genomunun 6000 geninin herbiri için özgün sekansları içeren bir
array slid şekil 2 de gösterilmektedir. Bu tek bir arrayden maya genomundaki tüm genlerin
ekspresyonları değerlendirilebilir. Böyle resimler yeni biyolojinin meydan okumasıyla bizi
yüzyüze getirir. Tüm sistemi görebiliriz ancak dataların gösterdiği bu binlerce birleştirilmiş
bilginin sezgilerle yorumlanması bizim kabiliyetlerimizin dışındadır.
Yeni sınıfladırma
algoritmaları, serbest organizasyon haritaları ve benzer araçlar biyologların başarıya
ulaşabilmeleri için datalara en son yaklaşımları sunmalarını sağlayan araçlardır.
Array yönteminin en önemli özelliği büyük düşünebilme kavramına sahip olmasıdır. Bir
hücre farklı durumlarda binlerce hatta onbinlerce geni ekspresse edebilmektedir. Hücrenin
yaşam ve
ölümü bu genlerin ekspresyonu ve
protein ürünlerinin aktivitelerince
belirlenmektedir. Herbir protein ‘ transmembran reseptör, transkripsiyon faktörü bir protein
kinaz ya da şaperon’ aynı hücrede ekspresse olanlarda dahil
bütün diğer fonksiyonların ve
aktivitelerin dışında önemli olan bir fonksiyonu gösterebilir.
Şimdi biyologlar yalnızca
kompenentlerin ve komleksliğin duyarlılığından ziyade sistemi anlamaya çalışarak büyük
düşünmeye çabalıyorlar.
Protein Kimyası ve Proteomiks Arasındaki Farklar:
Yeni bir fikre terime ve yaklaşıma yaygın olarak verilen cevap şüpheyle yaklaşmaktır. Bu
nedenle proteomiks ve protein biyokimyası arasındaki farkların iyi bir şekilde açıklanması
önemlidir. Hem proteomiks hemde protein kimyası protein tanımlanmasını kapsamaktadır.
Peki farklılık nerededir?
Tablo 1
Protein Kimyası ve Proteomiks Arasındaki Farklılıklar
Protein Kimyası
Proteomiks
•Yalnızca Proteinler
• Kompleks karışımlar
• Tüm sekans analizi
• Kısmi sekans analizi
• Yapı ve fonksiyon üzerinde önem
• Databaz eşleştirmeleri
üzerinde önem
• Yapısal biyoloji
• Sistemlerin biyolojisi
Tablo 1’de, dikkate alınan kilit özellikler kısaca özetlenmektedir. Protein kimyası, protein
yapısı ve fonksiyonunun çalışmalarını kapsar ve yaygın olarak fiziksel biyokimya ya da
mekhanistik enzimolojinin alanıdır. Çalışma genelde
araştırmak için
yapının fonksiyonu nasıl yönettiğini
komple sekans analizi,yapısal belirleme ve modelleme çalışmalarını
gerektirir. Fiziksel biyokimyacılar ve enzimolojistler tipik olarak bir protein ya da bir
zamanda çok altüniteli protein kompleksini çalışırlar.
Proteomiks çoklu protein sistemlerini inceler. Çoklu sistemlerin karşılıklı etkileşimlerini ,
geniş sistem veya networklerin bir parçası olarak bunların rollerindeki farklı proteinleri
inceler. Analiz direk olarak kompleks karışımdır fakat komple sekans analizi değildir. Bunun
yerine databazın eşleştirme araçlarının yardımıyla kısmi sekans analizleriyle analizler yapılır.
Proteomiks kavramı yapısal biyoloji yerine sistemlerin biyolojisidir. Diğer bir deyişle
proteomiksin gösterdiği herhangi tek bir komponentin davranışı yerine sistemin davranışını
karakterize etmektir.
Gen Ekspresyon Düzeyini Ölçebilirken Neden Proteomiksle Uğraşarak
Kendimize Acı Çektiriyoruz ?
Gen microarrayleri bir hücredeki genlerin bir kısmı ya da hepsinin ekspresyonunu hızlı bir
şekilde eldesini sağlamaktadır. Şübhesizki mRNAnın düzeyi bir hücrede yerine geçen
proteinin düzeyini tahminde yeterli değildir.
translasyon etkinliğindeki farklılıklar
mRNA stabilitesindeki farklılıklar ve
yeni proteinlerin üretimini etkilemektedir. Bir
yapılanmada proteinler stabilite ve turn over oranlarında önemli ölçüde farklılık gösterir.
Sinyal transdüksiyonu, transkripsiyonal – faktör düzenlemesi ve hücre döngüsünde gerekli
birtakım proteinlerin
aktivitelerini düzenleme manasında çevrimleri hızlıdır. mRNA
düzeyleri; aktiviteleri ve fonsiyonları birtakım iç posttranslasyonel modifikasyonlara ve
çevresel ajanlar tarafından diğer modifikasyonlara belirlenen yerlerine geçen proteinlerin
düzenleyici durumu hakkında hiçbirşey söylemez.
Proteomiks : Analitik bir Meydan Okuma
Bir organizmadaki genlerin bir kısmının ya da tümünün ekspresyonlarının nasıl ölçüleceği
problemi cDNA veya oligonükleotid mikroarray tekniklerinin kullanımı ile çözülmüştür. Gen
ekspresyonunun mikroarrayler ve bağıntılı metodlarla analizleri
PCR ve komplementer
sekansların oligonükleotidlerle hibridizasyonu tekniklerine bağlıdır.
Şübhesizki protein
analizleri için buna anolog bir araç yoktur. İlk olarak PCR’ın protein için bir eş anlamlısı
yoktur. Yani PCR ile polipeptid moleküllerinin kendilerini çoğaltmaları diye bir şey söz
konusu değildir.
İkinci olarak komplementer aminoasid sekanslarının spesifik olarak hibridizasyonu yoktur.
Nükleotid sekanslarının bu komplementer hibridizasyon karekterleri microarray teknolojisinin
kullanımını
olasıkılmaktadır.
peptid veya proteinleri
Antibady ve oligonükleotid aptamerleri (Şekil 3) spesifik
tanıyabilsede tanıma oligonükleotidlerde olduğu gibi sekans
temelinde basitce bir tanıma değildir.
Şekil 3: a) Fonksiyonel protein mikroaray b) Fonksiyonel protein mikroaray
Proteomikte karşılaşılan diğer bir problemde her bir protein gen ürününün hücre içinde
yalnızca bir molekül girişiyle kaçınılmaz olarak yükselme vermemesidir. Çünkü proteinler
posttranslasyonel modifiyedirler. Geniş ve değişik modifikasyon çeşitleri belirli proteinler
için, hücredeki düzenleyici mekanizmalar için ve çevresel faktörlere göre farklılık gösterir.
Sonuç olarak bazı proteinler çoklu formda bulunur. Özel bir genin çoklu protein ürünleri
arasındaki
farklılıklarının belirlenmesinin gereksinimi proteomikin analitik meydan
okumasına bir ilavedir.
Proteom analizleri gen ekspresyon analizlerine göre daha fazla farklı grupta yöntem gerektirir.
Proteomun karakterizasyon işi modifiye ve modifiye olmamış formların tesbiti ve miktarının
tayini için analitik metodlara gereksinim duyar.
Proteomiks Araçları :
Analitik proteomiksin daha önce tanımlanmış dezavantajlarına karşın proteom ve
onun
kompenetlerinin karakterizasyonu işi pratikte yapılabilinmektedir. Bu; dört temel yöntemin
araştırmacılar tarafından geliştirilmesi ile başarılmıştır. İlk yöntem organizmanın eksprese
olan proteinlerinin tümünün tam kataloğunu sağlayan
databazlarıdır.
protein, EST ve komple genom
Drosophilanın tüm kodlayıcı sekansları temel alındığında ; EGF benzeri
domainli proteinleri kodlayan 110 geni biliyoruz. Buna göre Drosophila da proteomiks
yaparken geniş fakat olası proteinleri bildiğimiz bir indeksi tarıyor olacağız.
İkinci yöntem kütle spektrofotometrisidir (mass spectrometry:MS).
Son yıllarda MS
ölçümleri köklü değişiklikler geçirdi. Yüksek duyarlılıkta ve robotlaşmaşmada son noktaya
ulaşmış bu
yöntem; özellikle protein ve peptidlerin analizinde oldukça güvenilir bir
yöntemdir. Bu yöntem 100kDa veya daha üstü intak proteinlerin moleküler kütle ölçümlerini
doğru olarak sağlayabilmektedir. Böylece protein kütlelerini belirlemek için SDS page de
yürütmek yerine
tercih edilmektedir.
Yüksek
doğrulukta protein kütle ölçümlerinin
genellikle faydaları limitlidir. Çünkü bunlar sıklıkla yeterince duyarlı değildir ve net kütle
sıklıkla protein tanımlanmasında istenmeyen eksikliktedir. MS aynı zamanda proteolitik
olarak parçalanmış polipeptidlerin ölçümünde de kullanılır. Tüm protein kütle ölçümünün
aksine peptid kütle ölçümleri daha duyarlı ve kütle daha doğrudur. MS analizi kullanılarak
proteolitik kesime uğratılmış peptidlerin kesin sekans analizleri elde edilebilmektedir.
Şekil 4: Proteomikste kullanılan yöntemler ve fonksiyonal genomiksle etkileşimleri
Üçüncü yöntem databazdaki spesifik protein sekansları ile MS datalarını eşleştirebilen
yazılımları
ortaya çıkarmaktır. Daha önce belirtildiği gibi MS datalarından bir peptidin
sekansının belirlenebilmesi mümkündür. Bununla birlikte bu de nova sekans yorumu kısman
zahmetli bir iştir. Bu software töntemi yorumlanmış datayı alır ve protein sekansları, EST ve
özelleşmiş algritmaları ekleyerek genom sekan databazı ile eşleştirir. Bu yöntemin en büyük
kullanışlığı çok fazla MS datasını protein sekansları ile eşleştirirken otomasyonu getirmesidir.
Proteomik için dördüncü yöntem analitik protein ayrım teknolojisidir. Protein ayrımı
proteomikste iki amaca hizmet eder.
İlki kompleks protein karışımlarımlarını
belli
proteinlere ya da proteinlerin küçük gruplarına çözerek onları basitleştirir. İkincisi bu aynı
zamanda iki örnek arasında karşılaştırma yaparak protein düzeylerindeki açık farklılığıda
gösterir. Protein analitik ayrımı araştırıcıya analizi için spesifik proteinleri hedeflemesini
sağlar. 2D SDS page proteomiksle ilişkilendirilmiş en yaygın yöntemdir. İki boyutlu jel
kompleks örneklerin proteinlerinin çözümü için muhtemelen en iyi yötem olarak taktim
edilebilir. Bununla birlikte diğer protein ayırma teknikleri 1D- SDS- PAGE , HPLC, kapiler
elektroforez, izoelektrik fokuslama ve affinite kromotografisi analitik proteomiks için
kullanışlı yöntemlerdir.
Bu dört yöntemin birbirleri ile etkileşimleri proteomiksin günümüzdeki teknoşojisini meydana
getirmiştir.
Şekil 5 : Maya data setlerinin geniş ölçekte etkileşimleri biraraya getirilerek canlandırma
yapılmıştır. GRID databazından sağlanan 14.000 fiziksel etkileşim Osprey network gösterim
sistemiyle (bak http://biodata.mshri.on.ca/grid) gösterildi. Grafikteki herbir kenar Gen
ontoloji (GO) fonksiyonel
kurallarına göre renklendirilmiş nodlar arasındaki ilişkiyi
simgelemektedir. Data setleri içindeki komplekslerin fazlalığı, merkezi kütlenin çevresinde
görünen, diğer kompleks üyeler içerisinde en az üçünü paylaşan nodlardan kaynaklıdır. Tüm
grafik 4.543 nodu bu da maya genomundan kodlanan yaklaşık 6000 proteini göstermektedir.
20 yüksek etkileşimli kompleks 340 geni , 1,835 bağlantı ve 5.39 ortalama bağlanabilirliği
içermektedir.
Proteomiksin Uygulama Alanları
Proteomiks teknolojisi gerçekten etkileyicidir. Günümüzde pratikte dört temel uygulamayı
kapsamaktadır. Bunlar 1) mining (örnekteki proteinlerin tümü)
2) protein ekspresyon
profili, 3) protein network haritalaması ve 4) protein modifikasyon haritalamasıdır.
1) Mining bir örnekteki proteinlerinin tümünün (olabildiğince) tanımlanabilmesi çabasıdır.
Miningte işaret edilen ; genlerin ekspresyon datalarından (mikroaraylar gibi)
proteom
dataları yerine direk olarak proteomu katologlamaktır.
çıkarılan
Mining proteomiksteki
“kaba kuvvet” çalışmalarının en sonudur. Basitce çözümlenmiş proteinler için geniş boyutta
olasılıklar vardır. MS kullanımı ve ilişkili databazlar ve softwarelerle ne bulunduğu
tanımlanabilir. Mining için çeşitli yaklaşımlar ve herbirinin avantajları mevcuttur.
2) Protein ekspresyon profilinde;
organizmanın ya da hücrenin
belirli bir durumdaki
(diferensiyasyon, gelişme durumu veya hastalık durumu gibi) ya da bir ilaç, kimyasal veya
fiziksel stimüle edici ile karşılaşmadaki fonksiyonu gibi belirli örneklerdeki proteinlerin
tanımlanmasıdır.
Şekil6 :
Kütle spektrofotometre görüntüleri; rat beyninin enine kesitleri üzerinde ortalama
protein profilini çıkarmak için kullanılmıştır 15 lazer çekimi ve atomatik imajlama computer
algoritmaları kullanılarak tarama işlemi tamamlanmıştır. Beklendiği gibi bazı proteinlerin
çalışılan beyin bölgesine oldukça spesifik olduğu bulundu.
Ekspresyon profili aslında miningin özelleşmiş formudur. Yaygın olarak belirli bir sistemin
iki durumunun karşılaştırılmasında farklı analizler olarak uygulanabilir. Örneğin normal ve
hastalıklı hücre veya dokular
ekspresyonları belirlenebilir.
bir durum diğeriyle karşılaştırılarak proteinlerin farklı
Bu bilgiler hastalıklarda ilaç terapilerinin potansiyellerinin
tespiti anlamında müthiş bir çekiciliğe sahiptir.
Protein network, haritaları yaşayan sistemelerde hangi proteinlerin birbirleriyle etkileşimde
olduklarını belirleyen proteomiks yaklaşımlarıdır.
Bir çok protein fonksiyonlarını diğer
proteinler ile etkileşimleriyle ortaya çıkarırlar. Bu etkileşimler, sinyal transdüksiyon yolu ve
kompleks biyosentetik veya degredasyon yolları gibi proteinlerin fonksiyonal networklerinin
fonksiyonlarını belirleyen etkileşimlerdir. Birçoğu bireylerle, pürifiye proteinlerle ve yeast
two hyprid sistemleri ile yapılan in vitro çalışmalarla elde edilen protein – protein
etkileşimlerinden öğrenilmiştir. Bununla birlikte proteomiks yaklaşımları analitik proteomiks
metodlarıyla birleşmiş afinite capture teknolojisinin yaratıcı çiftlerinin sayesinde daha
kompleks networklerin kurulmasının fırsatlarını sunmuştur. Proteomiks yaklaşımları çoklu
protein komplekslerinin kompenentlerinin tanımlanmasında kullanılmaktadır.
Çoklu
kompleksler hücrede noktadan noktaya sinyal transdüksiyon yolunda devreye girmektedir.
Protein network profili bu yoldaki katılımcıların tümünün bir durumlarını hesap edebilmeyi
sağlar. Bunun gibi, protein network profillemesi proteomiksin gelecekteki uygulamalarında
potansiyel olarak bir güç sunmaktadır.
Protein modifikasyonlarının haritalanması, proteinlerin nasıl ve nerde modifiye olduklarının
belirlenmesi işidir. Birçok yaygın posttranslasyonel modifikasyon proteinlerin hedefleme,
yapı, fonksiyon ve turoverını yönetir. Buna ilaveten birçok çevresel kimyasal , ilaçlar endojen
kimyasallar reaktif elektrofillere yol açarak proteinleri modifiye ederler. Analitik yöntemlerin
çeşitliliği modifiye proteinler ve modifikasyonların doğasının tanımlanmasını geliştirdi.
Modifiye proteinler antibadiler ile (spesifik fosforlanmış aminoasid reziduoları için) tespit
edilebilir fakat spesifik modifikasyonun kesin sekans bölgesi sıklıkla bilinemez. Proteomiks
yaklaşımları posttranslasyonel modifikasyonların hem dağal hemde sekans spesifitelerini
sağlama anlamında en iyiyi sunar. Bir networkdeki regule olmuş proteinlerin modifikasyon
durumlarının simultene olarak karakterize edilmeleri için bu yaklaşımdaki genişleme yine
proteomiks teknolojisindeki kuvvetli bir gelişme ile sunulur. Bu yaklaşımlar proteomun
kimyasal modifikasyonlarının yaşayan sistemleri nası etkilediği sorusuna yaklaşımda yeni
yollar sunacaktır.