1
1. GİRİŞ
İnterfaz sırasında, DNA ve onunla birleşmiş proteinler (histonlar) kromatin yapıda
sıkıca paketlenmiştir. DNA’nın tümünün paketlenme oranı, yaklaşık 1000-10000 kez
katlanma şeklindedir. Bu, onun hiyerarşik organizasyonu ile başarılır. Kromatinin temel
alt birimi nükleozomdur, ilk defa 1974’de R.D. Kornberg tarafından tarif edilmiştir.
Histon genleri evrimsel olarak çok iyi korunmuşlardır (Alberts ve ark., 2002, s.210).
Bir nükleozom; H2A, H2B, H3 ve H4’ün her birinden iki kopya olmak üzere sekiz
histon molekülünden (oktamer) kor içerir. Yaklaşık 140-150 baz çifti (insanda 147 bp)
içeren DNA, histon korun etrafında 11 nm çapında ve 6 nm yüksekliğinde bir
nükleozom oluşturmak için 1,67 kere sarılır. DNA, birbirine çok yakın noktalarda
nükleozoma girer ve çıkar. H1, iki nükleozom arasındaki DNA’ya bağlanır. Her
nükleozom, diğerinden 50-70 bp uzunluğundaki bağlayıcı DNA ile ayrılır, bu da 157240 bp bir tekrar uzunluğunu verir. Histonların ve DNA’nın bu sıkı birlikteliği,
transkripsiyon ve tamir sırasında gevşeyecektir (Passarge, 2009).
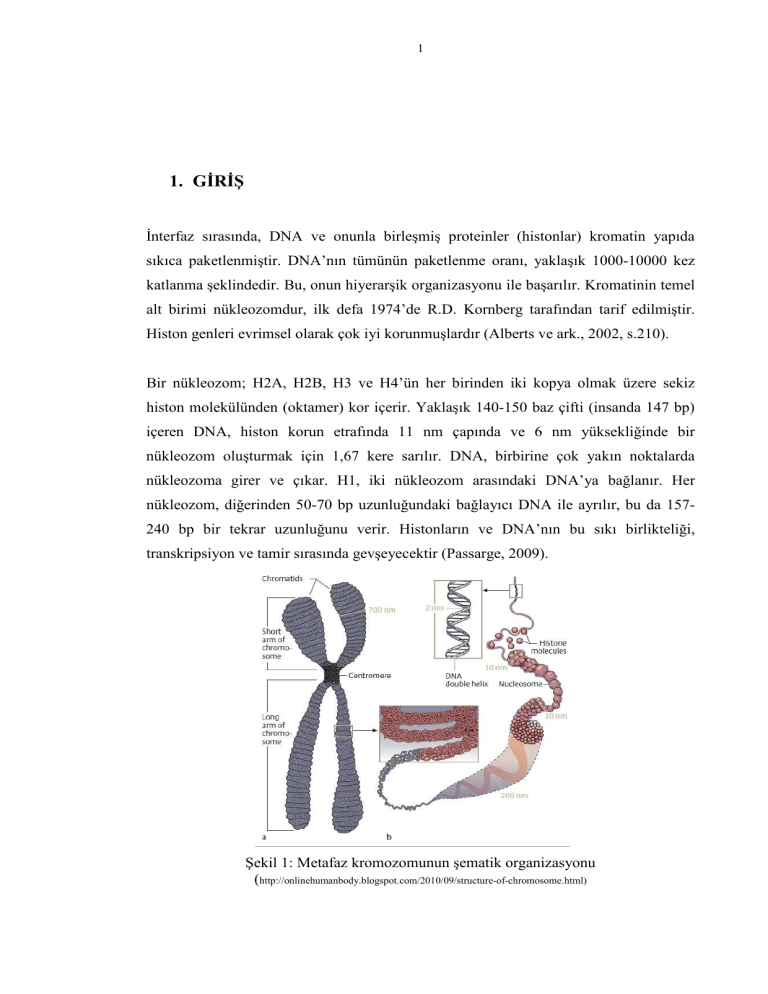
Şekil 1: Metafaz kromozomunun şematik organizasyonu
(http://onlinehumanbody.blogspot.com/2010/09/structure-of-chromosome.html)
2
Epigenetik değişimler, belirli genlerin ekspresyonunu DNA dizisini değiştirmeden
etkileyen, kalıtılabilir değişikliklerdir. Epigenetik terimi 1939’da C.H. Waddington
tarafından kullanılmıştır (Speybroeck, 2002).
Ökromatinde genler transkripsiyona açıktır, heterokromatinde değildir. Kromatinin
mevcut yapısı epigenetik bir durumdur. Bu, kromatin yeniden şekillendirme denilen
çeşitli mekanizmalarla geridönüşümlü olarak değiştirilebilir. Kromatin yeniden
şekillendirilmesi,
DNA
molekülünde
histonların
yerini
değiştirerek
genleri
transkripsiyona açık hale getiren, aktif ve geridönüşür bir süreçtir (Lewin, 2004).
Kromatinin yeniden şekillenmesinde; aktivatör proteinler heterokromatindeki “gen
kapalı” durumunu geri çevirebilir. Bunlar, kromatinde DNA’ya bağlanan, çoklu protein
komplekslerle etkileşebilen, özgül kontrol elemanlarıdır. Aktivatör proteinler bir aracı
proteine bağlanır, sonuçta kromatin gevşer ve gen “gen açık” durumunu alır. Genel
transkripsiyon faktörleri ve RNA polimeraz promotörde bir araya gelir ve
transkripsiyonu başlatır. Baskılayıcı proteinler kontrol elemanına bağlanınca bu süreç
tersine döner ve RNA polimeraz’ın transkripsiyonu başlatması engellenir (Passarge,
2009).
3
2. HETEROKROMATİN YAPININ OLUŞUMUNDA TRANSKRİP_
SİYON VE RNA ENGELLENMESİ
Ökaryotik DNA, gen ekspresyonu ve kromozom hareketini düzenleyen farklı yapısal
domenlere organize olur. Epigenetik olarak kalıtılabilen bu heterokromatik domenler;
geniş kromozom alanlarının ekspresyonunu ve yapısal kontrolünü sağladığı gibi hücre
bölünmesi sırasında kromozomların düzgün ayrılması için de gereklidir. Yapılan
çalışmalar, heterokromatin oluşumunda pek çok enzim ve yapısal proteinin birlikte
çalıştığını ortaya koymuştur. Heterokromatin yapının oluşum süreci, kromatin fiber
boyunca yaygın olan susturucu komplekslerin (“silencing complexes”) spesifik olarak
modifiye olmuş histonların amino-terminal uçlarıyla etkilişime girerek, adım adım
gerçekleşen histon modifikasyonunu (self-oligomerizasyon) kapsar. RNA interferans ve
kodlamayan RNA moleküllerinin de epigenetik kromatin domenlerinin oluşumunda rol
aldığı ortaya çıkarılmıştır (Grewal, 2003).
Kromozomlar, ökromatin ve heterokromatin olmak üzere iki yapıdan oluşurlar.
Heterokromatik alanlar (domenler), DNA’ya bağlanan faktörlerin geçişine izin
vermediği için transkripsiyonel açıdan sessizdirler. Buna karşın ökromatik kısımlar,
genomda sıklıkla erişilebilen aktif transkripsiyonel alanlar olarak tanımlanırlar.
Heterokromatinin büyük kısmı sentromer ve telomerler gibi fonksiyonel kromozom
yapılarını çevrelerken, daha küçük heterokromatik alanlar kromozom boyunca dağılmış
şekilde bulunur (Grewal, 2002).
Heterokromatin proteinleri, sentromerlerin çevresindeki DNA tekrarlarıyla ilişkili olup
kardeş
kromatidlerin
birbirleriyle
bağlanabilmesi
ve
kromozomların
düzgün
ayrılabilmeleri için gereklidir. Heterokromatin yapı aynı zamanda homolog tekrarlar
arasında rekombinasyonu engelleyerek; sentromer, telomer ve genomdaki diğer tekrarlı
DNA dizilerinin stabilizasyonunu sağlar (Grewal, 1997; Guarente, 2000).
4
Şekil 2.1.: Heterokromatin dağılımı ve sentromerik kromatin organizasyonu
1. Nature Reviews Genetics 9, 923-937 (2008)
2. http://www.studyblue.com/notes/note/n/chapter-4-dna-chromosomes-and-genomes/deck/1404309
Heterokromatin yapı genom stabilitesini sağlamasının yanısıra, gelişim ve hücresel
farklılaşma süresince gen ekspresyonunun düzenlenmesinde de merkezi rol oynar.
Heterokromatin benzeri yapılar, gelişimsel düzenleyicilerin inaktivasyonunda yer
alırlar. Bu düzenleyicilere Drosophila ve memelilerde homeotik gen kümeleri
(homeotic gene clusters), mantarlarda eşleşme tipi (mating-type) genleri örnek
verilebilir. Bunun dışında, dişi memelilerde dozaj dengelemesine bağlı olarak somatik
hücrelerdeki iki X kromozomundan biri heterokromatik inaktivasyona uğrar (Avner,
2001).
Heterokromatik durumun özelliklerinden biri, farklı gelişimsel ve çevresel koşullar
altında pek çok hücre bölünmesi sırasında epigenetik olarak kalıtılmasıdır. İkincisi,
heterokromatin
yapının
oluşum
mekanizması
ve
heterokromatinin
başlangıç
bölgesinden (nucleation site) çevreleyen DNA bölgelerine yayılması, dizi-spesifik
genetik kontrolden dizi-bağımsız epigenetik kontrole geçişi gerektirir.
5
2.1. Heterokromatin Yapının Oluşumundaki Faktörler
Mayalardan memelilere kadar değişik organizmalarla yapılan çalışmalar, histonların ve
translasyon sonrası histon modifikasyonlarının heterokromatin oluşumunda kilit rol
oynadığını göstermiştir. Ökaryotlarda DNA, herbiri iki molekülden oluşan dört histonun
(H2A, H2B, H3, H4) oluşturduğu oktamerik kompleksin etrafında yaklaşık iki tur
sarılarak nükleozomu oluşturmak üzere histonlarla bir araya gelir (Şekil 2.2.).
Histonların amino uçları (N-), çeşitli posttranslasyonel modifikasyonları içerir
(Jenuwein, 2001). Bunlar arasında en çok rastlananları, H3 ve H4 histonlarının yüksek
korunmuşluk gösteren amino uçlarındaki “lizin” birimlerinin asetilasyonu ve
metilasyonudur (Şekil 2.2.).
Şekil 2.2.: Nükleozomun şematik gösterimi ve histon uçlarında asetilasyon ve
metilasyon bölgeleri (Grewal, 2003).
(A) Nükleozom; kromatinin temel birimi. 147 bp genomik DNA molekülünün oldukça korunmuş histon
oktamer kompleksinin etrafında iki kez sarılmasıyla oluşur.
(B) Yeşil bayraklar, H3 ve H4 histonlarının amino uçlarındaki / globüler domenlerindeki asetil histon
modifikasyonlarının yerleşimini; Kırmızı işaretlerde aynı histon bölgelerindeki metil histon
modifikasyonlarının yerleşimini göstermektedir.
6
“Artmış asetilasyon” durumu transkripsiyonel aktiviteyle ilişkiliyken, “azalmış
asetilasyon” transkripsiyonel baskılanma durumu ile ilişkilidir. Bu yüzden, hemen
hemen tüm organizmalarda heterokromatik yapı, histonların hipoasetilasyonuyla
bağlantılıdır (Moazed, 2001) (Şekil 2.3.).
Şekil 2.3.: Ökromatik ve Heterokromatik bölgelerin özellikleri (Grewal, 2007).
Histon hipoasetilasyonunun dışında bölünen maya, Drosophila ve memelilerde histon
H3’ün 9. pozisyondaki Lizin (H3 Lys9) biriminin metillenmesi de heterokromatin
oluşumuyla ilişkilidir. Bu birim korunmuş bir metiltransferaz tarafından metillenir
(Drosophila’da “Su(var)3-9”, insanda “SUV39H1”, bölünen maya S. pombe’ de “Clr4”)
(Rea, 2000; Nakayama, 2001). Bu “H3 Lys9” metiltransferazlar da başka bir korunmuş
proteinle ilişkilidir ( bölünen maya da “Swi6”, Drosophila ve insanda “HP1”). Swi6 ve
HP1 proteinleri de, Clr4 / Suv39h enzimleri tarafından 9. pozisyondaki lizin birimleri
metillenmiş H3 histon kuyruklarına spesifik olarak bağlanırlar (Bannister, 2001;
Lachner, 2001) (Şekil 2.4).
7
Şekil 2.4: Kromatin domenlerinde sessizleşmenin oluşumu (Grewal, 2003).
DNA’ya direkt bağlanan proteinler ya da RNA’lar yoluyla hedeflenen spesifik bir heterokromatin bölgesinde nukleasyon başlatılır.
Deasetilaz ve metiltransferazlar gibi histon modifiye eden enzimler (E), sessizleştirici faktörlerin (SF, “Silencing Factors)
bağlanabileceği yer oluşturmak için histon kuyruklarını modifiye ederler. Bu nukleasyon aşamasından sonra, Swi6/HP1 ya da Sir3
gibi sessizleştirici faktörlerin birbiriyle etkileşimi sonucu yan yana bulunan histonların modifikasyonu gerçekleştirilerek SF’ler için
bağlanma bölgeleri oluşturulur. Birbirini izleyen modifikasyon ve bağlanma sonucunda, sessizleştirici kompleksin nukleozomal
DNA boyunca aşamalı şekilde yayıldığı gözlenir. Sessizleştirici komplekslerin yayılması, sınır elementlerinin (BE, “Boundary
Element”) varlığıyla bloke edilir. En alttaki resim, bölünen maya heterokromatininde (soldaki) ve ökromatininde (sağdaki) amino
uçlarından modifiye olan H3 histonlarını göstermektedir. H3 Lys9 deasetilasyonu ve metilasyonı, H3 Lys14 deasetilasyonunu takip
ederek Swi6 sessizleştirici faktör için bağlanma bölgesi yaratır.
8
2.2. Heterokromatin Nukleasyonunda (Başlamasında) Sessizleştirici (Silencers),
Tekrarlar (Repeats) ve RNA’ların Rolü
Öncelikli soru: Heterokromatin kompleksler spesifik bir kromozomal bölgeye nasıl
hedeflenirler? Heterokromatin nukleasyonunda “sessizleştiriciler” ve “dizi-spesifik
DNA bağlanma proteinleri” gibi spesifik düzenleyici bölgelerin rolü anlaşılmış olsa da;
tekrarlı DNA elementleri (repetitive DNA elements) ve kodlamayan RNA (noncoding
RNAs) moleküllerinin de heterokromatin komplekslerinin bölgesel hedeflenmesinde yer
aldıkları gösterilmiştir (Henikoff, 2000; Hsieh, 2000). Heterokromatik dizilerin büyük
bir fraksiyonunu kapsayan satellit tekrarları ve transpozonların, yakındaki genlerin
sessizleştirilmesine
yol
açarak
heterokromatin
mekanizmayı
görevlendirdiği
düşünülmektedir.
Değişik boyutlarda meydana gelen kodlamayan RNA molekülleri, kromozomal
davranışın düzenlenmesinde büyük rol üstlenir. Örneğin; Drosophila ve memelilerde
dozaj ayarlamasında (Park, 2001), yine memelilerde genomik damgalanma (“genomic
imprinting”) (Sleutels, 2002) gibi kromatini modifiye eden aktivitelerde RNA
moleküllerinin kromozoma özgü lokalizasyonları önemlidir.
RNA interferans (RNAi) yolunun post-transkripsiyonel (transkripsiyon sonrası) gen
sessizleştirilmesindeki rolü iyi anlaşılmış olmakla birlikte (Hannon, 2002), tekrarlı
DNA bölgelerinde heterokromatin yapının oluşumunda da yer aldıkları bildirilmiştir
(Hall, 2002; Volpe, 2002) (Şekil 2.5; Şekil 2.6).
RNAi mekanizmasının bileşenleri; PAZ/Piwi ailesinin üyelerinden Argonaute (ago1),
RNazIII-benzeri enzim Dicer (dcr1) ve RNA’ya bağlı RNA polimeraz (rdp1)’den
oluşmaktadır. Bu bileşenlerin S. pombe’de heterokromatin oluşumunda ve H3 Lys9
metilasyonunun hedeflenmesinde gerekli olduğu gösterilmiştir (Hall, 2002; Volpe,
2002).
9
Şekil 2.5: Heterokromatin yapının başlamasındaki mekanizmalar (Grewal, 2003).
Heterokromatik yapılar, sessizleştirici “silencer” denilen DNA bağlanma proteinleri tarafından tanınan “cis-acting” diziler ile
başlatılabilir (soldaki resim). Genomda transpozonlar gibi tekrarlı DNA elementlerinin, heterokromatin oluşumunda sinyal görevi
gördükleri düşünülmektedir (sağdaki resim). Tekrarlı DNA tarafından oluşturulan transkriptler; RNA-bağımlı RNA polimeraz
(RdRP), Dicer ve Argonaute proteinleri gibi RNAi mekanizmasının bileşenleri tarafından shRNA (“küçük heterokromatik
RNA)’lara dönüştürülürler.
Şekil 2.6: RNAi mekanizmasına ait bir model (Duggan, 2010).
Hücre içerisinde gen sessizleşmesi; sentetik RNA’lar, replikasyon yapay virüsler ya da nuklear genlerden transkripsiyonla oluşan
çift zincirli RNA (dsRNA) moleküllerinin oluşumuyla tetiklenir. Bu moleküller Dicer denilen enzim tarafından tanınarak küçük
müdahaleci RNA (siRNA)’lara dönüştürülür. Çift zincirli siRNA’ların RISC kompleksine (“RNA-induced silencing complex”)
dahil olmasıyla kompleksin aktivasyonu ve RNA dupleksinin (çift sarmalın) çözülmesi gerçekleşir. Aktive olmuş RISC
kompleksleri gen ekspresyonunu farklı düzeylerde düzenleyebilir. Bu kompleksler çoğunlukla RNA yıkımını teşvik ederek
translasyonal inhibisyona yol açarlar. Bunun dışında, benzer komplekslerin kromatinin yeniden şekillendirilmesinde görev aldıkları
bilinmektedir. Ayrıca bu yolun, çeşitli genetik hastalıklarla ilişkili genleri kodlayan spesifik dizilerin hedeflenmesinde
kullanılabilecek potansiyel terapi yöntemlerinden biri olabileceği bildirilmiştir (Hannon, 2002).
10
2.3. RNAi ve Heterokromatin Pre-mRNA Birleştirici (Splicing) Faktörleri
Sentromer yakınında heterokromatin oluşumu; tekrarlı DNA dizileri ve DNA bağlanma
proteinlerine gereksinim duymasına rağmen, Robin Allshire’ın laboratuvarında RNAi
mekanizmasındaki düzenleyici proteinlerin bölünen maya hücrelerinde kromatin
sessizleştirilmesinde gerekli olduğu keşfedilmiştir (Duggan, 2010). Düzenleyici
proteinlerin, pre-mRNA’dan olgun mRNA'nın oluşumunda intronları uzaklaştıran
proteinler olan birleştirici faktörlerin (“splicing factors”) oluşumunda yer alabileceği
bildirilmiştir. Son yıllarda yapılan çalışmalarda, pek çok “splicing” faktörün in vivo
olarak sadece RNAi mekanizmasıyla etkileşim halinde olmadığı, aynı zamanda
perisentromerik bölgelerde RNAi-yönlendirilmiş heterokromatin oluşumunda gerekli
olduğu kaydedilmiştir (Bayne, 2008; Tang, 1998). Bu yüzden, “splicing” faktörlerin
mayalarda heterokromatin oluşumunu sağlayan RNAi mekanizmasının düzenleyicisi
olduğu bildirilmiştir (Şekil 2.7).
Şekil 2.7: RNA aracılı gen susturulması (Hannon, 2010, Nature, 418, 244-251).
Çift iplikli RNA (dsRNA) molekülleri, ilgilenilen genlerin susturulması için deneysel olarak hücreye aktarılabilmektedir. Gen
susturulması; bitkilerde genetik mühendisliği aracılığıyla RNA virüsleri kullanılarak, kurtlarda dsRNA enjeksiyonu ya da besin
yoluyla tetiklenebilmektedir. Her iki sistemde de RNAi aracılı gen susturulması, sistemik ve organizma boyunca yayılan şekilde
gerçekleşmektedir. A) Susturucu sinyal, bitkinin damarlarından yaprak dokusunun içine doğru hareket etmektedir. Yeşil: GFP
(Green Fluorescence Protein), Kırmızı: GFP geni üzerinde susturucu etkisi olan klorofil floresans proteini temsil etmektedir. B) C.
elegans genetik mühendisliğiyle hücre nukleuslarında GFP proteinini eksprese edecek şekilde değiştirilmiştir. Sağdaki resimde
kontrol dsRNA ile muamele edilmişken; soldaki resimde GFP dsRNA kullanılmıştır. C) ORC6 genine karşı siRNA ile muamele
edilen HeLa hücrelerinde tubulinin yeşil, DNA’nın kırmızı boyanması. ORC6’nın azalması, multinukleuslu hücrelerin artışına yol
açmıştır. D) Yetişkin Drosophila’da RNAi teşvikiyle “white” geninin homoloğu olan siRNA ekspresyonu (soldaki resim), wildtype ile karşılaştırıldığında pigmentsiz gözün oluşumu (Sağdaki resim).
11
Heterokromatinle yakın ilişkili bölgelerde genlerin susturulmasına yönelik farklı bir
fonksiyonda, “yayılan (spreading)” özellikte susturmanın bir kromozomal bölgeden
diğerine aktarılmasıdır. Bu tip heterokromatik sessizleştirme PEV (“position effect
variegation”, pozisyon etkisine bağlı çeşitlilik) olarak tanımlanır. PEV, gelişmekte olan
Drosophila gözüne ait hücrelerde mozaik formda sessizleştirme şeklinde gözlenmiştir
(Huisinga ve Elgin, 2009) (Şekil 2.8).
Şekil 2.8: Drosophila ve bölünen mayada PEV “position effect variegation” (Volpe, 2011).
Drosophila’da “white” geni w(m4h)’ın heterokromatin tarafından sessizleştirilmesi sonucu gözde beyaz bölümlerin yerini kırmızı
rengin alması gösterilmektedir. Sessizleştirme erkek sineklerde geliştirilmektedir. Bölünen mayada, hetekromatik dizilerin yakınına
integre edilen ade6’nın sessizleştirilmesine bağlı kayıp, kırmızı koloniler üzerinde beyaz bölümlerin oluşmasına neden olmaktadır.
Ökaryotlarda kromatinin yüksek yapıda düzenlenmesi, genetik bilginin bütünlüğü ve
ekspresyonun düzenlenmesiyle ilişkilidir; aynı zamanda genlerin, kromozomların,
genomların
ve
organizmaların
evriminde
büyük
öneme
sahiptir.
DNA’nın
heterokromatine paketlenmesinde birçok önemli biyolojik süreçte epigenetik kontrol
kullanılır. Yapılan çalışmalar sonucu epigenetik kromatin oluşumlarının nasıl
gerçekleştiği, kromozom domenlerinde değişikliklere yol açan histonlar üzerinde nasıl
bir mekanizma çalıştığına yönelik soruların cevaplanması açısından bir devrim
gerçekleşmiştir. Bunun dışında heterokromatin oluşumunda RNAi mekanizmasının yer
aldığının keşfiyle, kromozom yapısının bölgesel kontrolünde RNA’nın rolü büyük
12
heyecan yaratmıştır. Yeni yapılacak çalışmalarla; kromatin domenlerinin oluşumunda
ve ilerlemesinde etkili olan, bunların oluşumda rol alan RNA molekülünün farklı
rollerinin keşfedilmesiyle epigenetik mekanizmalar hakkında daha detaylı bilgiler
edinilebileceği düşünülmektedir.










