İki Boyutlu Jel Elektroforezi
Two Dimensional Gel Electrophoresis
(2D-GE)
TEORİ
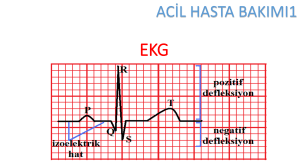
İzoelektrik nokta:
Proteinin net yükünün 0 olduğu pH
değeri.
Proteinler izoelektrik noktalarının
altındaki pH’larda pozitif (+)
yüklüdürler ve elektriki alanda katoda
(- yüklü elektroda) göç ederler.
İzolektrik noktalarının üzerindeki
pH’larda negatif (-) yüklüdürler ve
anoda (+ yüklü elektroda) göç
ederler.
İzoelektrik noktasında protein yüksüzdür. Anoda ya da katoda göç etmez.
Proteinler izoelektrik noktalarının
altındaki pH’larda pozitif (+) yüklüdürler
ve elektriki alanda katoda (- yüklü
elektroda) göç ederler.
İzolektrik noktalarının
üzerindeki pH’larda
negatif (-) yüklüdürler ve
anoda (+ yüklü elektroda)
göç ederler.
(2D-GE) (O’Farrell, 1975)
Amaç: Tüm gen ürünlerini ayırmak
Binlerce proteini aynı anda ayırma yeteneğine sahip tek yöntem
İlk boyut: İzoelektrik odaklama
(Isoelectric focusing, IF):
Proteinler
pH
gradienti
oluşturulmuş bir destek üzerinde,
izoelektrik noktalarına (yüklerine)
göre ayrışırlar.
İkinci boyut: SDS_PAGE
İzoelektrik
noktalarına
göre
ayrılmış proteinler denatüre jelde
molekül
ağırlıklarına
göre
ayrışırlar.
O' Farrell PH (1975) High resolution two-dimensional electrophoresis of proteins. J Biol Chem 250: 4007-4021
2D-GE
İlk Boyut
İzoelekrik noktalara göre ayırım 3 farklı yaklaşımla
gerçekleştirilir:
I.
Taşıyıcı amfolitlerle izoelektrik odaklama («carrier
ampholyte isoelectric focucing», CA-IEF)
II.
Dengesiz pH jel elektroforezi («non-equilibrium
pH gradient electrophoresis, NEPHGE)
III.
İmmobilize pH gradient elektroforezi
(«immobilized pH gradient electrophoresis», IPGE)
CA-IEF
Önce ticari olarak satılan
amfolit ya da amfolin® (düşük
molekül ağırlıklı sentetik
poliaminopoli karboksilli asitler)
karışımları (farklı pI
değerlerine sahip) jelde
elektroforezle ayrılır.
Daha sonra protein karışımı
uygulanır ve elektrik akımı
geçirilir. Her protein net
yükünün 0 olduğu pH
bölgesine doğru göç eder ve
orada odaklanır.
Elektrik akımı uygulandığında taşıyıcı amfolitler katoddan
anoda doğru pI düşecek şekilde yerleşirler. Her bir amfolit
kendi pI değerine eşdeğer lokal bir pH ortamı yaratır ve
böylece jel boyunca bir pH gradienti (derecelenmesi) oluşur.
Bir protein karışımı jel yüzeyine uygulandığında her bir
protein kendi izoelektrik noktasına karşılık gelen pH
bölgesine kadar elektrik akımının etkisiyle yürür. Bu
noktaya ulaştığında net yükü 0 olacağından sabit duruma
geçer. Difüzyon ile bu bölgeden anoda doğru azıcık
uzaklaşacak olsa, + yük kazanacağından tekrar katoda
çekilir veya katoda doğru difüzlenecek olsa – yük kazanır ve
anoda çekilir, böylece pI bölgesinde hapsolur ya da
«ODAKLANIR».
NEPHGE
Dengesiz pH jel elektroforezi (Nonequilibrium pH gel electrophoresis,
NEPHGE) İzoelektrik noktaları çok yüksek (pI 7.5-11) olan çok bazik
proteinler için geliştirilmiş bir tekniktir.
Bu proteinleri standart IEF ile ayrıştırmak zordur, çünkü IEF jellerindeki
üre tamponlama etkisi nedeniyle pH gradientinin bazik değerlere (pH
7.3-7.6’nın üzerine) ulaşmasını engeller.
Ayrıca, zamanla jelin özellikle iki ucundaki
gradient bozulur ve katoda doğru çekilme (cathodic
drift) denilen bir olay nedeniyle çok bazik proteinler
jelden çıkar. NEPHGE sırasında, proteinler
izoelektrik noktalarında tam olarak odaklanmazlar.
Jel boyunca yüklerine göre farklı hızlarda hareket
ederler. Bu nedenle jel boyunca yayılma şekli,
uygulanan elektriğin voltajına ve süresine bağlıdır.
Bu nedenle tekrarlanabilir ayırımlar elde etmek için
elektriksel parametreleri düşük ve her seferinde
aynı tutmak gerekir.
See for detail Nonequilibrium pH Gel Electrophoresis (NEPHGE) by Lopez, M. F.
in The Protein Protocols Handbook, 2nd Edition Edited by: J. M. Walker © Humana Press Inc., Totowa, NJ
SORUNLAR
Tekrarlı deneylerde farklı sonuçlar!
pH gradienti sabit değil
Zamanla katoda doğru kayar (‘cathodic drift’)
ÇÖZÜM
IEF için İmmobilize pH gradientlerini (IPG)
kullanmak (Bjellqvist et al. 1982).
IPG’lerde pH gradienti, akrilamit matriks
ile birlikte polimerize olan (kopolimerize), ‘Immobilin’ denilen sınırlı
sayıda (6-8) kimyasal tarafından
oluşturulur.
Bjellqvist B, Ek K, Righetti PG, Gianazza E, Görg A, Westermeier R, Postel, W (1982)
Isoelectric focusing in immobilized pH gradients: Principle, methodology and some
applications. J Biochem Biophys Methods 6: 317-339
IPGE : Immobilize pH gradient
elektroforezi
Ticari olarak hazırlanmış IPG DryStrip’leri
kullanımı:
Tekrarlı deneylerde farklı sonuçları
ortadan kaldırır.
pI rezolusyonu artar (0.01 pH
ünitesi)
Uygulama basitleşir.
Immobiline® akrilamido
tamponları POLİMERİZASYON
SIRASINDA akrilamid matriksi
içinde immobilize olur. Böylece
pH gradienti de sabitlenir.
Materyaller ve Aletler
ReadyStrip IPG Strips
Rehidrasyon/Dengeleme Tepsisi
PROTEAN IEF Hücresi (BIO-RAD)
Güç Kaynağı
PROTEAN II xi Elektroforez Aleti
(BIO-RAD)
(ReadyPrepTM 2-D Starter Kit, BIO-RAD, 163-2105)
Kit Bileşenleri (Kit Constituents)
İçerik (Content)
Rehidrasyon/Örnek Tamponu
(“ReadyPrep Rehydration/Sample
Buffer”)
8 M Üre
%2 CHAPS
50 mM DTT
%2 (w/v) Bio-Lyte ® 3/10 amfolit
Bromofenol mavisi (eser miktarda)
Dengeleme Tamponu I
(“Equilibration Buffer I”)
6 M Üre
%2 SDS (sodyum dodesil sülfat)
0.375 M Tris-HCl (pH 8.8)
%20 Gliserol
%2 (w/v) DTT
Dengeleme Tamponu II
(“Equilibration Buffer II”)
6 M Üre
%2 SDS
0.375 M Tris-HCl (pH 8.8)
%20 Gliserol
%2.5 (w/v) İyodoasetamid
Kapatma çözeltisi
(“Overlaying Solution”)
%0.5 Agaroz
25 mM Tris
192 mM Glisin
%0.1 SDS
Bromofenol mavisi (trace-eser)
Uygulama: Birinci Boyut
Şerit uzunluğu
7 cm
11 cm 17 cm
Örnek hacmi
125 μl 185 μl 300 μl
Protein Yükleme Miktarı 169 μg 250 μg 405 μg
Rehidrasyon sırasında örnek uygulama
Uygun hacimde örnek tepsideki kanala pipetle
uygulanır.
Uygulama : İlk Boyut
Pens yardımıyla şeritin
arkasındaki tabaka kaldırılır.
Şerit örneğin üzerine yerleştirilir. “+”
Ve “pH 4-7” yazısı tepsinin solunda ve
okunabilir olmalıdır.
Uygulama: Birinci Boyut
Her bir şeritin üzeri 2 to 3 ml mineral yağ ile
kaplanır (rehidrasyon sırasında evaporasyonu
önlemek için)
Tepsi plastik kapakla örtülür ve 1 gece (11-16
saat) oda sıcaklığında bekletilir (IPG şeritlerinin
rehidrate olması ve protein örneklerin
yüklenmesi için)
Rehidrasyondan sonra
örneklerin
uygulanabileceği
düzenekler de
mevcuttur (Örnek
kapları kullanılır)
Uygulama: Birinci Boyut
Odaklama tepsisindeki
kanalların her iki ucundaki
elektrot tellerinin üzerine
pens yardımıyla kağıt
filtreler yerleştirilir.
Elektrot filtreleri saf su ile
ıslatılır.
Uygulama: Birinci Boyut
Mineral yağ uzaklaştırılır
Şeritler Odaklama tepsisinin
oluklarına yerleştirilir.
Odaklama tepsisi PROTEAN IEF hücresine yerleştirilir, kapak
kapatılır ve sistem ayarlanarak çalıştırılır.
Uygulama: Birinci Boyut
7 cm
Voltage
Step 1 250
Step 2 4,000
Step 3 4,000
Total 5 hr 14,000 V-hr
Time
20 min
2 hr
-----
Volt-Hours
--------10,000 V-hr
Ramp
Linear
Linear
Rapid
11 cm
Step 1 250
20 min
Step 2 8,000
2.5 hr
Step 3 8,000
----Total 5.3 hr ~30,000 V-hr
--------20,000 V-hr
Linear
Linear
Rapid
17 cm
Step 1 250
Step 2 10,000
Step 3 10,000
Total 7 hr ~50,000 V-hr
--------40,000 V-hr
Linear
Linear
Rapid
20 min
2.5 hr
-----
BOYAMA
Kolloidal Coomassie Blue
Gümüş Boyama
Sypro Ruby
Çinko/Bakır (Zinc/Copper)
Negatif Boyama
SONUÇ
Pratikte proteomik çalışmalar 3
alanda yürütülür:
Ekspresyon («abundance») proteomiği (Klasik
proteomik)
AMAÇ: Belli koşullarda altında protein
ekspresyonlarını karşılaştırmak
İşlevsel proteomik («cell-mapping or cellular
proteomics»)
AMAÇ: protein-protein interaksiyonlarını göstermek
(hücreiçi sinyalleşmeyi ve protein işlevini oluşturan
kompleks ağların çerçevesini ortaya koymak için)
Yapısal proteomik
AMAÇ: 3 boyutlu yapıyı aydınlatmak
KLASİK PROTEOMİK
KONTROL
ALZHEIMER
HASTASI