kloroplast transformasyonu
advertisement

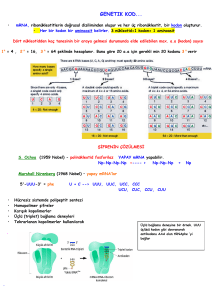
KLOROPLAST TRANSFORMASYONU ÖZGE ÇELİK HALİÇ ÜNİVERSİTESİ MOLEKÜLER BİYOLOJİ VE GENETİK BÖLÜMÜ PLASTİDLER Çift zarlı ve kendi genomlarını (plastom) taşıyan hücre organelleridir. Hücre DNA’sının %10-20’si kloroplastlarda bulunur. Karbohidratlar, pigmentler, amino asit ve yağ asitleri gibi önemli bileşiklerin sentezinde görevlidirler. 1 PLASTOM • Sirküler • Çift iplikli DNA molekülü • 120-160 kb boyutunda •Yaklaşık 130 gen •Yüksek oranda korunmuştur. • Büyük ve küçük kopya bölgeleri (LSC ve SSC) • 2 adet tekrar dizisi (IRA ve IRB) içerir Bitki mezofil hücresi, 10.000-50.000 adet plastid DNA kopyası taşır (Bendich, 1987). Yüksek organizasyonlu bitkilerde plastidler mühendislik uygulamaları için önemli hedeflerdir. genetik 2 Plastomun transformasyonu, nuklear transformasyona göre bazı avantajlara sahiptir. 1) Transgenlerin polenlerle çevreye yayılımı önlenmiştir (Maliga, 1993; Daniell et al., 1998). 2) Plastid kromozomlarının çok sayıda kopyası bulunur; yüksek oranda protein sentezi ve birikimi mümkündür (Mc Bride at al., 1995; Staub et al., 2000). 3) Gen transferi homolog rekombinasyon ile olmaktadır. Pozisyon etkisi veya çoklu integrasyon olaylarından kaçınılır (Fejes et al., 1990; Suab et al., 1990; Eibl et al., 1999). Plastom Transformasyonunun Avantajları 4) Plastom, prokaryotik gen organizasyonu gösterir; böylece birçok gen 1 operonda transkribe olabilir ( Staub and Maliga, 1995). 5) Gen sessizleşmesi olmaz ve gen ekspresyonu stabildir (Sidorov et al., 1999). 3 Seçici markır ve homolog yan bölgeleri içeren vektör oluşturulması Partikül bombardımanı ile veya PEG muamelesiyle hücreye aktarılması Transforme DNA’nın plastom içine homolog rekombinasyon ile girişi Yabani tip genomlaın eliminasyonu Plastid Transformasyonunda Kulanılan Metodlar BİOLİSTİK PEG METODU 4 MARKIR GENLER • Spektinomisin Direnci (Suab et al., 1990) • Kanamisin Direnci ( Carrer et al., 1993) • Ispanaktaki betain aldehit dehidrogenaz geni (BADH) (Daniell et al., 2000). aadA geni spektinomisin ve streptomisine direnç gösterir. Tütün için iyi bir plastom seçilim markırıdır ancak arpa ve A. thaliana için uygun değildir (Kofer et al., 1998). En iyi seçilim, seçici ortam kültür koşulları ile birlikte kullanılmalıdır. Diğer seçici markırlardan nptII dışında BADH’da kullanılabilir. 5 REPORTER GENLER • Kloramfenikol asetil transferaz (CAT) (Daniell et al., 1990) • β- glukoronidaz (uid A, GUS) (Ye et al., 1990) • Green –floresan protein (GFP) (Sidorov et al., 1999) kullanılmaktadır. BİOLİSTİK METODU 1 ml buz soğukluğunda %100 etanol 50 mg tungsten tozuna eklenir (partikül boyutu 1.1 µm) Max hızda 2 dakika vortekslenir (x3) 8000 rpm’de 2 sn santrifüjlenir Etanol uzaklaştırılır ve partiküller 1 ml buz soğukluğunda steril dH2O ile yıkanır (x3) Partiküller 1 ml suda süspanse edilir 50 µl tungsten partikül süspansiyonu+15 µg plazmid DNA+50 µl 2.5 M CaCl2+20 µl 0.1M spermidin Partiküller 1 ml suda süspanse edilir 30 dakika 4oC’de vortekslenir 6 200 µl %100 etanol eklenir ve 2 sn 8000 rpm’de santrifüj edilir. Etanol uzaklaştırılır Partiküller 200 µl buz soğukluğunda %100 etanolle yıkanır (x3) Partiküller 200 µl buz soğukluğunda %100 etanolle yıkanır Partiküller 8000 rpm’de 2 sn santrifüjlenir Partiküller200 µl taze etanolle süspanse edilir. Partiküller 30 µl % 100 etanolle süspanse edilir ve kullanıma kadar buzda bekletilir. Nicotiana tabacum cv. Petit Havana için biolistik metodu kullanılarak kloroplast transformasyonu yapılmıştır. Uygulanan Koşullar: Tank regülatöründeki helium basıncı: 1300-1400 psi Hareketli disk: Üstten 2. Seviye Petri taşıyıcı disk: Alttan 2. Seviye Vuruş anındaki vakum: 24-28 in.Hg 7 (Bock, 1998) İşlem sonrasında yapraklar 1-2 gün 25oC’de normal besiyerde bekletilir. Daha sonra küçük parçalara ayrılan yapraklar seçici ortama ekilirler (500 µg/ml spektinomisin). Dirençli kallus ve sürgünler 4-6 hafta sonra görülür. 8 Ancak tüm rejenere olmayabilirler. olanlar kloroplast transformantı 16S rRNA geninde spesifik nokta mutasyonu oluşumuyla spektinomisine dirençli hale gelebilirler. Mutasyon sonucu aadA geni birçok aminoglikozid antibiyotiğe direnç gösterir. Böylece spontan spektinomisin dirençli bitkiler streptomisine karşı hassastırlar. Bu nedenle gerçek kloroplast transformantları her iki ilacın bulunduğu ortamlarda seçilmelidirler. 9 Yapılmış Olan Çalışmalara Örnekler Daucus carota L. tuza hassa bir bitkidir. Tuz stresine metabolik adaptasyonlardan osmoprotektanların birikimidir. biri de Glisin betain, çevre ile osmotik dengenin sağlanması ve komplex proteinlerin kuaterner yapılarını stabilize ederek hücreleri tuz stresinden korur. Transgenik havuçta BADH enzim aktivitesi 100 mM NaCl varlığında 8 kat artmıştır (Daniell et al., 2005) (Daniell et al., 2005) 10 Pamuk, ticari öneme sahip bir bitkidir. Bt toksinine dayanıklı nüklear transforme bitkiler tamamen korumalı değildirler. Kumar ve ark.(2005), pamuk plastid genomuna transformasyonu başarmışlardır. (Daniell et al., 2005) 11 Soya (Glycine max. L.Merrill), önemli bir protein kaynağıdır. Yapılan ilk uygulama Zhang ve ark.’ları tarafından (2001) fotosentetik potansiyeli arttırmak için yapılmıştır. (Daniell et al., 2005) 12 Polietilen Glikol ile Plastid Transformasyonu Çıplak DNA, divalent katyonlar (genellikle kalsiyum) varlığında PEG uygulamasıyla hücreye direkt olarak aktarılabilir. PEG ve divalent katyonlar, bitki protoplastının hücre zarını destabilize ederler. Böylece yabancı DNA plastoma integre olur. Etkili bir PEG Metodu için; • Protoplast kültürü kurulmalı • Türler, protoplastlardan rejenere olmalı • Hedef doku ve organlar yüksek etkinlikte rejenere olabilmeli • Kullanılan vektör yaklaşık 1 kb boyutunda olmalı • Seçici marker ve düzenleyici elementler olmalı (Saub and Maliga, 1995). 13 PEG METODU 200 ml protoplast kültürüne 2% Driselase uygulanır Protoplast süspansiyonu 1.2×106 protoplasts ml–1 olacak şekilde 3M medium [15 mM MgCl2, 0.48 M mannitol, 0.1% 2-(N-morpholino)ethanesulfonic asit tamponu, pH 5.6]’da sulandırılır. Transformasyon için 250 µl protoplast solüsyonu 350 µl PEG solution (40% PEG 4000 in 3M medium, pH 6.0) ve 20 µg veya 50 µg DNA içeren 100 µl 0.1 M Ca(NO3)2 ile karıştırılır. 30 dakika inkübe edilir.. Transformasyon solüsyonu 3M medium ile her 5 dakikada bir 1, 2, 3 and 4 ml ilave edilir. Süspansiyon 10 dak 45 g’de santrifüj edilir ve pelet 3 ml rejenerasyon besiyerinde süspanse edilir. Süspansiyon 25 °C for 1 gün karanlıkta, takiben 10 gün aydınlıkta (70 µmol s–1 m–2, ışık/karanlık dozu16/8 h’da inkübe edilirler Süspansiyon selofan ile kaplanıuş agarlı petrilere yerleştirilir 3 gün sonra, selofanlı kültür 25 µg G418 ml–1 içeren besiyerine 2 haftalığına geçirilir. 2 haftalığına G418 içermeyen besiyerine geçirilirler. Seçilimin 2. aşamasında yaşayanlar stabil transformant bitkilerdir (Hohe et al., 2003) 14 VEKTÖRLER Başta kullanılan transformasyon vektörleri spektinomisin ve streptomisin direnci sağlayan nokta mutasyonlu plastid 16S rRNA (rrn16) geni taşıyan vektörlerdir. Resesif rrn16 markır genleri şimdi kullanılan aadA genine göre 100 kat daha az etkilidir. aadA geni, adenilasyon ile spektinomisin ve streptomisini inaktive eden aminoglikozid-3’-adeniltransferaz enzimini şifreler. Plastid vektörleri, LTR ve RTR olarak gösterilen sağ ve sol plastid hedefleme bölgelerine homolog hedeflenirler. Seçilen bölgeye homologdurlar ve 1-2 kb boyutundadırlar. 50 kb DNA (20-30 genlik) girişi için uygundur. Plastid tekrar vektör (pPRV) serileri, trnV-rps12 bölgesine girişi hedeflerler. 15 pRB94 ve pRB95 vektörleri, trnfM-trnG bölgelerine hedeflenirler. Plastid genomundaki tekbölgesidir. trnV-rps12 bölgeye sokulan genin 2 kopyası bulnur çünkü, giriş bölgesi tütün plastid genomunda inverted tekrar bölgesindedir. Plastid transgenleri, 5’-PL (promotör ve lider) ve 3’-T kaset (Tterminatör)de eksprese olurlar. PL kasedi, promotör ve translasyon kontrol dizisi içerir. Translasyon kontrol dizisi, mRNA 5’-transle olmayan bölge (UTR) veya 5’-translasyon kontrol bölgesi (TCR) olabilir. mRNA 5’-UTR, mRNA stabilitesi için gereklidir ve dizisi mRNA’nın ribozomlara yerleşmesini kolaylaştırır. 16 T-kasedi, mRNA 3’-UTR’yi şifreler. T-3’-UTR, translasyonun etkisiz terminatörü olarak görev yapar ve mRNA stabilitesi için gereklidir. PL ve T kasetleri ve kodlama bölgelerinde aynı RE kesim bölgelerinin olması gen düzenlenmesini kolaylaştırır. Fazla miktarda protein birikimi için dikkat edilmesi gerekenler: 1) İyi promotör seçimi 2) mRNA, 3’-UTR ile stabilize olmalıdır (Maliga, 2003). 17 Soyada Kullanılmış Olan pTRA140 ve pB5HYG vektörleri; GUS reporter geni Higromisin direnç geni CaMV 35S promotörü taşırlar (Reedy et al., 2003). Primer transplastomik hücre hatları, yabani tip ve transforme bitki genomlarının karışık bir populasyonunu içermektedir. Böyle hücre, doku veya bitkiler heteroplazmik olarak adlandırılırlar. Heteroplazmik durumlar genetik olarak stabil değildir ve 2 tip genom homojenitesine spontan olarak ayrışır. Bu hücre dışı genetik materyalin sınıflanması, random hücre bölünmesine bağlı olarak random organel bölünmesine dayanır. 18 Transplastomik hücre hatları ve bitki homoplazmiye ihtiyaç duymaktadır. Yüksek konsantrasyonda seçici antibiyotik varlığında yeterli sayıda hücre bölünmesi olduğunda homoplazmi sağlanır. PCR bazlı testler ile homoplazmi konfirme edilir. Heteroplazminin 2 tipi ayırt edilir. 1) İnterplastidik heteroplazmi: Yabani tip genom ve mutant genomları aynı hücrede bulunur. 2) İntraplastidik heteroplazmi: Yabani tip ve mutant plastid genomu aynı kloroplastta bulunur. 19 Interplastidik heteroplazmi, hızlı bir şekilde kaybolur çünkü, yabani tip genomlar seçici antibiyotiğe hassastırlar ve bu nedenle transforme kloroplastlar kadar etkili çoğalamazlar. Zıt olarak, intraplastidik heteroplazmiyi elimine etmesi çok zordur çünkü girdiği organelde direnç geninin bir veya birkaç kopyası direnç sağladığı için, antibiyotik direnç geni dominant seçici markır gibi davranır 20 Plastid Ekspresyon Teknolojisinin Evrimi (Maliga, 2003) 1988 Chlamydomonas reinhardtii, 1. stabil plastid transformasyonu, DNA aktarımı: biolistik Yaklaşım: Homolog hedefleme, Seleksiyon: Fotosentetik yetenek 1990 Nicotiana tobacum (tütün), 1. stabil plastid transformasyonu, DNA aktarımı: biolistik Yaklaşım: Homolog hedefleme, Seleksiyon: Spektinomisin-streptomisin rezistansı (rrn16) 1991 Chlamydomonas reinhardtii Seleksiyon: Spektinomisin-streptomisin rezistansı (rrn16) 1993 Nicotiana tobacum (tütün), DNA aktarımı: PEG Seleksiyon: Spektinomisin-streptomisin rezistansı (aadA) Seleksiyon:Kanamisin rezistansı (neo) Protein ekspresyonu:1. en fazla yabancı protein seviyesi; %2.5 GUS (bakteriyel) 1994 Nicotiana tobacum (tütün), Protein ekspresyonu:Nüklear kontrollü plastid gen ekspresyonu 1995 Nicotiana tobacum (tütün), Seleksiyon: düzenleme temelli markır geni Protein ekspresyonu:Polisistronik ekspresyon ünitesi Yeni agronomik özellik: Bacillus thuringiensis insektisidiyal protein Markır gen eliminasyonu:Ko-transformasyon 1996 Chlamydomonas reinhardtii, Markır gen eliminasyonu:Homolog rekombinasyon ile ilmek açmak ve ko-transformasyon 1998 Arabidopsis thaliana, 1. stabil plastid transformasyonu 1999 Solanum tuberosum (patates), 1.stabil plastid transformasyonu Oryza sativa (pirinç), 1.stabil plastid transformasyonu 2000 Nicotiana tobacum (tütün), Protein ekspresyonu:İlk insan proteini Markır gen eliminasyonu: Homolog rekombinasyon ile ilmek açma 2001 Lycopersicon esculentum (domates), Protein ekspresyonu:Meyvada eksprese olan ilk yabancı protein Nicotiana tobacum (tütün), Protein ekspresyonu:Heterolog RUBISCO ile fotoototrofik bitki Protein ekspresyonu:Süper ekspresyon kasetleri (>%10), Markır gen eliminasyonu: CRE-lox sistemi Yeni agronomik özellik: Glifosat (herbisit) toleransı, Yeni agronomik özellik: PPT(herbisit) toleransı Kloroplast genom mühendisliği ile yapılan ilk agronomik özellikler (Daniell et al., 2005) Özellik Transgen Promotör 5’/3’ UTRs Homolog rekombinasyon bölgesi Böcek direnci Cry1A Prrn rbcL/Trps16 trnV/rbs12/7 Herbisit direnci AroA Prrn ggagg/TpsbA rbcL/accD Böcek direnci Cry2Aa2 Prrn ggagg(doğal)/TpsbA rbcL/accD Herbisit direnci bar Prrn rbcl/psbA rbcL/accD Böcek direnci Cry2Aa2 operon Prrn Doğal 5’ UTRs/TpsbA trnI/trnA Hastalık direnci MSI-99 Prrn ggagg/TpsbA trnI/trnA Kuraklık toleransı tps Prrn ggagg/TpsbA trnI/trnA Fitoremediyasyon MerA/merB Prrn ggagg/TpsbA trnI/trnA Tuz toleransı badh Prrn-F ggagg/rps16 trnI/trnA Sitoplazmik erkek kısırlığı phaA Prrn PpsbA/psbA trnI/trnA 21 Plastidlere DNA Aktarımında Kullanılan Bitki Türleri (Heifets, 2000) Tür Arabidopsis Havuç Aktarım metodu Sonuç Biolistik Bütünleşmiş homoplazmik Biolistik Geçici Nicotiana plumbaginifolia Protoplast Geçici; Bütünleşmiş homoplazmik Tobacco (NT1 süspansiyon hücreleri) Biolistik Geçici Kadife çiçeği Biolistik Geçici Patates Biolistik Geçici; Bütünleşmiş homoplazmik Kırmızı biber Biolistik Geçici Pirinç Biolistik Bütünleşmiş homoplazmik Biolistik, protoplast Bütünleşmiş homoplazmik Tobacco (Petit Havana, Xanthi) Tütün Plastidlerinde Stabil Olarak Eksprese Olan Genler (Heifetz, 2000) Gen/Protein Kaynak aadA E.coli aadA:GFP Kimerik Aprotinin Sığır AroE Bacillus subtilis Bsn Klebsiella pneumoniae CoxII Petunia (mitokondri.) Crtl Erwinia carotova Cry1Ac Bacillus thuringiensis Cry2Aa2 Bacillus thuringiensis E5 Selülaz Thermomonospora fusca EPSPS Petunia GFP Aequorwa victoria GUS E.coli nptII Tn5 Poly(GVGVP) Elastin (sentetik) PPO Bitki (nukleus) RubiscoLSU Ayçiçeği Rubisco LSU Syncechococcus PCC6301 Somatotropin İnsan 22 Kloroplast genomunda biyofarmasötik proteinleri ve aşı antijenleri ekspresyonu (Daniell et al., 2005) Protein Transgen Promotör 5’/3’ UTRs Homolog rekombinasyon bölgesi Elastin türevli polimer EG121 Prrn T7 gen10/TpsbA trnI/trnA İnsan somatotropin hST Prrn, PpsbA T7 gen10, TpsbA/Trps16 trnV/rbs12/7 Kolera toksini CtxB Prrn ggagg/TpsbA trnI/trnA Antimikrobiyal peptid MSI-99 Prrn ggagg/TpsbA trnI/trnA Interferon α2b INFa2B Prrn Ppsba/TpsbA trnI/trnA Monoklonal antikorlar Guy’s 13; HSBV-lsc Prrn atpA/rbcL ggagg/TpsbA atpA/rbcL trnI/trnA psbA/5S/23S Antraks koruyucu antijen Pag Prrn Ppsba/TpsbA trnI/trnA Tetanoz toksini Tet C Prrn T7 gen10, AtpB/TrbcL Trnv/rpsa 12/7 Kaynaklar: Bock, R. Transgenic Plastids in Basic Research and Plant Biotechnlogy. J. Mol.Bio. (2001), 312, 425-438. Heifetz, P.B. Genetic engineering of the chloroplast. Biochimie (2000), 82, 655-666. Daniell, H., Kumar, S., Dufourmantel, N. Breakthrough in chloroplast genetic engineering of agronomically important crops. Trends in Biotechnology (2005). 23, 238-245. Maliga, P. Progress towards commercialization of plastid transformation technology. Trends in Biotechnology (2003), 21, 20-28. Bendich, AJ.Why do chloroplasts and mitochondria contain so many copies of their genome? Bioassays (1987), 6: 279-282. Carrer, H., Hockenberry, TN., Svab, Z., Maliga, P.Kanamycin resistance as a selective plastid marker. Mol.Gen. Genet. (1993), 241: 49-56. Daniell, H., Vivekaranda, J., Nelson, BL., Ye, GN., Temari, KK., Sanford, JC. Transient foreign gene expression in chloroplasts of cultured tobacco cells after biolistic deliver of chloroplast vectors.Proc. Natl.Acad. Sci.(1990), 87:88-92. Daniell, H., Datta, R., Varma, S., Groy, S., Lee, SB., Containment of herbicide resistance through genetic engineering of the chloroplast genome. Nature Biotechnol. (1998), 16: 345-348. Daniell,H., Mathukumar, B., Lee, SB. Marker free transgenic plants: engineering the chloroplast genome without the use of abiotic selection. Curr. Genet.(2000), 39:109-116. Eibl, C. In vivo analysis of plastid psbA, rbcL and rpI32 UTR elements by chloroplast transformation:tobacco plastid gene expression is controlled by modulation of transcript levels and translation efficiency. Plant J.(1999), 19(3): 333-345. Fejes, E., Engler, D., Maliga, P.Extensive homologous chloroplast DNA recombination in the pt 14 Nicotiana somatic hybrid. Theor. Appl. Genet. 79:28-32., Kofer, W., Eibl, C., Steinmüller, K., Koop, Hu. PEG mediated plastid transformation in higher plants. In vitroCell Dev.Biol.(1998), 34: 303-309. Mc Bride, KE., Suah, Z., Shaaf, DJ., Hogon, PS., Stalker, DM., Maliga, P.Amplification of a chimeric Bacillus gene in chloroplasts leads to an extraordinary level of an insecticidal protein in tobacco. Biotechnology (1995), 13: 362-365. Sidorov, VA., Karsten, D., Pang, SZ., Staub, JM., Nehra, NS. Stable chloroplast transformaion in potato: use of a green fluorescent protein as a plastid marker. Plant J.(1999), 19(2), 209-216. Staub, JM., Maliga, P. Expression of a chimeric uidA gene indicates that polycistronic mRNAs are efficiently translated in tobacco plastids. Plant J.(1995), 7:845-848. Svab, Z. Stable transformation of plastids in higher plants. Proc. Natl.Acad. Sci.(1990), 87: 8526-8530. Staub, JM., garcio, B., Graves, J.., Huntor, P., Nehra, N., Carroll, JA. High-yield production of a human therapeutic protein in tobacco chloroplasts.Nature Biotechnology (2000), 18: 333-338. Ye, GN., Daniell, H., Sanford, JC. Optimization of delivery of foreign DNA into higher plant chloroplasts. Plant Mol. Biol. (1990), 15: 809-819. 23