Yrd.Doç.Dr. Emre YALAMAÇ
Yrd.Doç.Dr. Emre YALAMAÇ
İÇERİK
•
Elektromanyetik Işıma
•
Işığın Doğası
– Işığın Dalga Doğası
– Işığın Parçacık Doğası
•
Atom Spektrumları
•
Madde ve Enerjinin Parçacık-Dalga İkililik Durumu
•
Atomun Kuantum-Mekanik Modeli
•
Atom Orbitali ve Elektronun Olası Yeri
•
Bir Atom Orbitalinin Kuantum Sayıları
•
Atomun Enerji Düzeyleri ve Orbitalleri
•
Atom Orbitallerinin Şekilleri
Yrd.Doç.Dr. Emre YALAMAÇ
Elektromanyetik Işıma
• Elektrik ve manyetik alanların dalgalar şeklinde
yayıldığı bir ortam veya vakumdan yayılan enerji
şeklidir.
• Işık, x-ışınımı, mikrodalga ve radyo dalgaları
elektromanyetik ışımalardır.
Yrd.Doç.Dr. Emre YALAMAÇ
Işığın Dalga Doğası
• Dalgaboyu ( lambda): İki tepe
veya çanak noktası arasındaki
mesafedir.
• Frekans ( nü): Bir saniyede
belirli bir noktadan geçen dalga
sayısıdır.
Birimi 1/s =Hertz(Hz)
Dalga Hızı: Birim zamanda alına yol
= Dalgaboyu X Frekans
c=*
Işık Hızı = 3,00 * 108 (m/s)
Sabit
Vakum ortamında
Yrd.Doç.Dr. Emre YALAMAÇ
Işığın Dalga Doğası
• Genlik: elektrik ve manyetik alan vektörlerinin en
uzun olduğu uzaklık.
Genlik, ışımanın yoğunluğu
ile ilişkilidir ve örneğin görünür
ışığın parlaklığı olarak alınır.
Yrd.Doç.Dr. Emre YALAMAÇ
Elektromanyetik Spektrum
Spektrumda yer alan bütün dalgalar vakum altında aynı hızla hareket
ederler, fakat farklı frekanslarla, dolayısyla farklı dalgaboylarında.
En kısa dalgaboylu mor renkten en uzun dalgaboyundaki kırmızıya kadar
uzanan görünür bölge, tüm spektrumun yalnızca küçük bir kısmını kapsar.
Yrd.Doç.Dr. Emre YALAMAÇ
ÖRNEK
Dişçi x-ışınımı (=1.00 A°) tekniği ile hastasının diş röntgenini
çekerken, hasta radyo (=325 cm) dinliyor ve pencereden mavi
gökyüzünü (=473 nm) bakıyor. Bu kaynaklardan gelen
elektromanyetik ışımaların frekanslarını hesaplayınız?
Çözüm:
Yrd.Doç.Dr. Emre YALAMAÇ
Enerji ve Madde Arasında Fark
Işık farklı Ortamlarda farklı
hızlarla hareket eder.
Işık bir ortamdan diğerine
90° açı dışında farklı bir açı
ile çarparsa hızının
değişmesi yönünün
değişmesine sebep olur bu
olaya(refraction) kırılma
denir.
Bir dalga herhangi bir
nesnenin kenarına çarparak
nesnenin etrafında
bükülmesine kırınım
(Diffraction) denir.
Yrd.Doç.Dr. Emre YALAMAÇ
Dalga Girişimi
Yrd.Doç.Dr. Emre YALAMAÇ
Işığın Parçacık Doğası
20. Yüzyılda fizikçileri 3 önemli olgu, madde ile ışık ilişkisinde
kafalarını karıştırmıştır.
1- Siyah cisim ışıması
2- Fotoelektrik olayı
3- Atom Spektrumu
Yrd.Doç.Dr. Emre YALAMAÇ
Işığın Parçacık Doğası
Siyah cisim ışıması
Isınan cisimler farklı renklerde ışık yayarlar, yayınlanan ışığın
rengi 1000K’lerde yanan kömürden çıkan açık kırmızı renkten,
bir elektrik ampulünün flamanındaki beyaz renge kadar değişir.
Isıtılan bir cismin bu yoğunluk ve yayılan ışığın dalgaboyundaki
değişimler siyah cisim ışımasının karakteristik özellikleridir.
Işık siyah cisim tarafından yayınır.
Klasik elektromanyetik teoriye göre yapılan bütün açıklamalar
bu gözlenen değişimler için başarısız olmuştur.
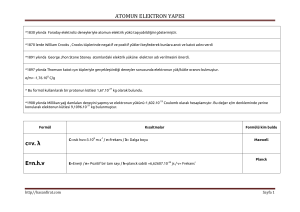
Planck’ın Enerji Kuramı “Enerji de madde gibi sürekli değildir.”
E nh
E h
n: Kuantum sayısı (tam sayı:1,2,3...)
: Frekans
h: Planck sabiti (6,626*10-34 J s)
Max Planck (1858-1947)
Yrd.Doç.Dr. Emre YALAMAÇ
Işığın Parçacık Doğası
Fotoelektrik Olayı
Yeterli frekanstaki monokromatik bir ışığın
metal plakaya çarpmasıyla akım oluşturmasını
enerjinin dalga modeli açıklayamamıştır.
1. Işığın frekansı belirli bir eşik değerin
üzerinde olması aski taktirde akım oluşmuyor:
Fakat dalga teorisi; ışığın enerjisini dalganın
genliği ile ilişkilendiriyor, frekans (renk) ile değil.
2. Bir zaman gecikmesinin olmaması:
Akım akışında, ışığın yoğunluğuna bakmadan,
ışığın minimum frekans anında metal plakadan
elektron fırlar. Fakat dalga teorisi, sönük ışıkta
akım akışı başlamadan önce bir zaman geçikmesi
bekler çünkü elektronların fırlayabilmeleri için
yeterli enerji emmeleri gerekir.
Yrd.Doç.Dr. Emre YALAMAÇ
Işığın Parçacık Doğası
Fotoelektrik Olayı
Planck’ın kuantum enerji kuramı, daha sonra A. Einstein tarafından ışımanın
tanecik şeklinde yorumlanmasını önermiştir. G. Lewis tarafından bu
elektromanyetik enerji paketciklerine foton adı verilmiştir. Dolayısıyla her
atomun enerjisi emdiği yada saldığı foton (ışık taneciği) ile değişir.
E foton h Eatom
Işığın frekansı belirli bir eşik değerin üzerinde olması: Bir ışık demeti
muazzam sayıda foton içerir. Işık parlaklığı(genliği) birim zamanda
yüzeye çarpan foton sayısı ile ilişkilidir fakat fotonların enerjileri ile değil.
Dolayısıyla belirli minimum (sınır) enerjiye sahip bir foton elektron
tarafından emilirse, elektron yüzeyden fırlayabilir.
Bir zaman gecikmesinin olmaması: Kendi enerjisi fırlamaya yeterli oluncaya
kadar elektron, minimum enerji seviyesinin altındaki fotonlardan enerji
biriktirmez. Elektron, foton enerjisi yeterli bir foton emdiğinde fırlar.
Yrd.Doç.Dr. Emre YALAMAÇ
Atom Spektrumları
Bir element buharlaştırıldıktan sonra ısıl yada elektriksel olarak uyarılırsa
ışık salar. Saçılan bu ışık güneş ışığı gibi sürekli spektrumda değil elemente
bağlı olarak belirli bir çizgisel spektrumda oluşur.
Bazı elementlerin
çizgisel spektrumları
Yrd.Doç.Dr. Emre YALAMAÇ
Atom Spektrumları
• Elektromanyetik spektrumun farklı bölgelerinde hidrojen
örneği için 3 tane farklı çizgisel spektrum bulunmuştur.
Rydberg denklemiyle verilen bir serinin herhangi bir çizgisinin yeri ve
dalgaboyu tahmini yapılabilinir.
: Çizgisel bir spektrumun dalgaboyu
n1 ve n2 : pozitif tam sayı
(n1=2 çizgisel görünür seriler)
R : Rydberg sabiti (1,096776*107 m-1)
Yrd.Doç.Dr. Emre YALAMAÇ
Bohr Atom Modeli
H atomunun mevcut çizgisel spektrumunu tahmin etmek
için Bohr bir model önermiştir.
1. H atomunun sadece uygun, izin verilen enerji seviyeleri vardır.
Bohr bunlara durağan konum(stationary state) der. Her bir
konum, elektronun çekirdeğin çevresinde sabit bir yörüngede
hareketiyle bağıntılıdır.
2. Atom herhangi bir durağan konumda iken enerji yaymaz. Yani
klasik fiziğin aksine bir yörüngede hareket ederken enerjisini
değiştirmez.
3. Atom diğer bir durağan konuma (elektron başka
bir yörüngeye hareket ettiğinde) sadece foton
yayarak yada emerek geçer. Bu fotonun enerjisi ise
iki konum arasındaki enerji farkına eşittir.
Niels Bohr
(1885-1962)
Yrd.Doç.Dr. Emre YALAMAÇ
Bohr Atom Modeli
• Bohr atom modeline göre atomun
spektrumunun sürekli olmaması nedeni;
atomun enerjisinin sadece kesin ayrı
seviyelerdeki konumlarda bulunmasıdır.
• Bohr modeline göre düşük kuantum
sayısı(n), küçük yörünge yarıçapı ve düşük
enerji seviyesiyle ilişkilidir.
• H atomu için en düşük (birinci) enerji
seviyesine temel konum, ikinci ve daha
sonraki enerji seviyelerindeki konumlara ise
uyarılmış konum(1’inci, 2’inci, gibi) denir.
Kuantum Merdiveni
Yrd.Doç.Dr. Emre YALAMAÇ
• Bohr atom modeli, maalesef diğer atomların
spektrum açıklaması için başarısız olmuştur.
Bohr’un 3 Elektromanyetik Seri için
Çizgisel Spektrumları
Yrd.Doç.Dr. Emre YALAMAÇ
H Atomunun Enerji Konumları
Elektrostatik çekim ve dairesel hareketin klasik
temellerinden yararlanarak Bohr iki konum arasındaki
enerji farkının hesabını yapmıştır.
Enerjinin negatif değeri, atomun enerjisinin elektronun
tamamen çekirdekten ayrıldığı zaman, sıfır olarak kabul
(E=0, n=) edilmesiyle açıklanır.
Yrd.Doç.Dr. Emre YALAMAÇ
Madde ve Enerjinin Parçacık-Dalga
İkililik Durumu
De Broglie’nin sabit(izin verilen) enerji seviyeleri açıklaması:
Eğer, enerji tanecik gibi davranıyorsa, madde olasılıkla dalga gibi davranır.
Örnek olarak: gitar telinin dalgalanmada
sadece
belirli
titreşim
aralığında
olabileceğini çünkü tel boyunun sınırlı
olduğuna dayanarak savunmuştur.
Eğer elektron dalga şeklinde hareket
yapıyorsa ve çapı belirli yörüngelerle
sınırlıysa bu da kesin olası frenkansları
ve enerjileri açıklar.
Louis de Broglie
(1892-1987)
Yrd.Doç.Dr. Emre YALAMAÇ
Madde ve Enerjinin Parçacık-Dalga
İkililik Durumu
m : kütle
u : hız
Yrd.Doç.Dr. Emre YALAMAÇ
Madde ve Enerjinin Parçacık-Dalga
İkililik Durumu
Elektron ve X-ışınının alüminyum folyo üzerindeki benzer
kırınım davranışları elektronunda elektromanyetik ışıma
gibi dalga şeklinde yol aldığını işaret eder.
Eğer elektronların enerji özelliği varsa, fotonların
madde özelliği var mıdır?
Kısa dalgaboylu fotonlar,
yüksek momentumludur.
A: X-ışını Kırınımı
B: Elektron Kırınımı
Yrd.Doç.Dr. Emre YALAMAÇ
Gözlemler ve Klasik Teoriden Kuantum Teorisine Geçiş
Yrd.Doç.Dr. Emre YALAMAÇ
Heinsberg Belirsizlik İlkesi
Elektronun hem parçacık hem de dalga özelliği varsa, atomun içinde onun
pozisyonunu neyle nasıl belirleyebiliriz?
Heinsberg belirsizlik ilkesi olarak ileri sürdüğü bağıntıda bir taneciğin aynı
andaki konumunun ve momentumunun kesin bir şekilde ölçülemeyeceğini
ileri sürmüştür.
x = Konumdaki Belirsizlik
u = Hızdaki Belirsizlik
mu =p
W. Heinsberg
(1901-1976)
Konumun büyük bir duyarlılıkla bilinmesi (küçük x) iken, hızın küçük bir
duyarlılıkla bilinmesine (büyük u) yada tersinin olmasına nedendir.
Bir beyzbol topu için çizeceği rotayı tahmin ederken x ve u çok etkili değildir.
Çünkü topun ağırlığı h/4 değerine göre çok büyüktür. Fakat bir elektron için
konum ve hızın bilip izleyeceği yolu bilmek tamamen ayrı bir durumdur.
ÖRNEK: ue=6x106 m/s %1 ise u =6x104 m/s iken x =10-9 m
olur buda bir atomun çapının(10-10 m) 10 katıdır.
Yrd.Doç.Dr. Emre YALAMAÇ
Atomun Kuantum-Mekaniksel Modeli
Madde ve enerjinin doğal ikililik durumunun kabulü ve belirsizlik ilkesi
kuantum mekaniği alanın içinde yer almaktadır ve kuantum mekaniği
objelerin atomik ölçekte dalgasal doğasını inceler. 1926 yılında E.
Schröndinger hidrojen atomunun kuantum-mekaniği modelini esas
alan bir denklem çıkarmıştır. Bu model, atomun kesin izin verilen
frekanslarda olmasından kaynaklanan kesin izin verilen miktarlarda
enerjisinin olduğu ve bir elektronun davranışının dalgamsı ve tam
kesin yerini bilmenin mümkün olmayacağını ifade eder.
: Dalga Fonksiyonu
H : Hamiltonian operatör
E: Enerji
E. Schröndinger
(1887-1961)
Yrd.Doç.Dr. Emre YALAMAÇ
Atom Orbitali ve Elektronun Olası Yeri
Elektronun madde dalga durumu çekirdek etrafında üç boyutlu alan kaplar.
Belirli bir fonksiyonu için izin verilen bir enerji değeri çıkar.
Verilen dalga fonksiyonuyla ilişkili her çözüme bir atom orbitali denir.
Kuantum-mekaniğinde bahsedilen bu orbital kavramı, Bohr atom modelinde
bahsedilen yörünge kavramı ile ilişkili değildir. Orbital matematiksel bir
fonksiyondur ve fiziksel bir anlamı yoktur.
Elektronun herhangi bir zaman nerde olduğunu kesin olarak bilemeyiz sadece
olası yerini tahmin ederiz. Dalga fonksiyonunun () karesi olasılık yoğunluğunu
(2) ifade eder ve belirtilen enerji seviyesi için elektron olası yoğunluk
diyagramını verir. Bu diyagrama bazen elektron bulutu da denir.
Yrd.Doç.Dr. Emre YALAMAÇ
Atom Orbitali ve Elektronun Olası Yeri
Elektron olasılık yoğunluğu, çekirdekten uzaklaştıkça düşer. Elektronun çekirdekten
uzak olduğu durumda olasılığı çok küçüktür fakat sıfır değildir.
Elektronun çekirdekten herhangi bir “r” uzaklığında toplam bulunma olasılığı olasılık
yoğunluğu değerlerinin toplamıdır ve çekirdekten itibaren çemberimsi ince
tabakalara bölersek elektronun toplam bulunma olasılığı ikinci tabakada birinciden
fazladır. Çekirdeğin yakınında her tabakanın hacim artışı, olasılık yoğunluğu
azalışından hızlıdır. Bu birbirine ters olma durumundan dolayı, toplam olasılık
çekirdekten biraz mesafe sonra tepe noktası yapar bu da radyal olasılık dağılımı
grafiği olarak gösterilir.
Yrd.Doç.Dr. Emre YALAMAÇ
Bir Atom Orbitalinin Kuantum Sayıları
Bir atom orbitali 3 kuantum sayısı ile tanımlanır.
Bu 3 kuantum sayısı arasında hiyerarşik bir ilişki vardır.
Temel kuantum sayısı (n) (Orbital büyüklüğü) değeri açısal momentum (l)
(orbital şekli) değerini sınırlar ve O da manyetik (ml) (oryantasyon) değerini
sınırlar.
Toplam orbital sayısı verilen bir n sayısına göre n2’dir.
Yrd.Doç.Dr. Emre YALAMAÇ
Atomun Enerji Düzeyleri ve Orbitalleri
1. Enerji düzeyi (kabuk): Atomun enerji seviyesini söyler ve n değeri ile
ifade edilir.
2. Alt enerji düzeyi (alt kabuk): Atomun enerji düzeyleri alt enerji düzeyleri
ya da alt kabuklar içerir. Ve bu da orbital şekli ile ifade edilir ve her alt
kabuk bir harfle gösterilir.
l:0
l:1
l:2
l:3
s
p
d
f
3. Orbital: Her izin verilen n, l ve ml değerlerinin kombinasyonundan atomun
belirlenen bir orbitali tanımlanır.
Yrd.Doç.Dr. Emre YALAMAÇ
ÖRNEKLER
Temel (baş) kuantum sayısı (n) 3 ise, açısal (l) ve manyetik (ml)
kuantum sayıları nelerdir?
Cevap:
n = 3 l : 0,1,2
l = 0 ml : 0
l = 1 ml : -1,0,+1
l = 2 ml : -2,-1,0,+1,+2
Aşağıdaki durumlar için, olası manyetik kuantum sayılarını, orbital
sayılarını ve alt enerji düzeyi adlarını yazınız?
Cevap:
Yrd.Doç.Dr. Emre YALAMAÇ
Atom Orbitallerinin Şekilleri
s orbitali: l=0 küre şeklindedir, ve çekirdek merkezindedir.
Örnek H atomunun temel durumda elektronun 1s orbitalinde olduğu durumda
elektron olası yoğunluğunun en yüksek olduğu yer çekirdektir.
Çeyrek elektron bulutunun gösteriminde en karanlık kısım çekirdektir.
Radyal (yarıçapsal) olasılık dağılımı (elektronların çoğu zamanını geçirdiği yer)
çekirdekten biraz dışarıda en yüksektir.
2s orbital için iki tane yüksek elektron yoğunluğu bölgesi vardır.
İkinci bölgenin hacmi çok daha büyük olduğu için (2) olasılık yoğunluğu
toplamı daha büyüktür.
Bu iki bölge arasında bir düğüm bölgesi bulunur ve burada olasılık (2 =0)
sıfıra düşer.
Yrd.Doç.Dr. Emre YALAMAÇ
S orbitalleri
Yrd.Doç.Dr. Emre YALAMAÇ
Atom Orbitallerinin Şekilleri
p orbitali: l=1 yüksek olasılıklı iki bölge (lob) biri diğerine
göre çekirdeğin diğer tarafında dolayısıyla çekirdek düğüm
yüzeyinde bulunur ve dambıl şeklinde bir orbitaldir.
Bir p orbitali iki lobtan oluşur ve elektron zamanını eşit
şekilde her iki tarafta da geçirir.
p orbitalinin uzayda belirli bir oryantasyonu vardır ve l=1 için
3 olası ml değeri -1, 0,+1 bulunur. Bunlar birbirlerine diktirler.
Hepsi aynı büyüklük, şekilde ve enerjidedirler fakat farklı
oryantasyonları vardır. x, y, ve z eksenleri ile ifade edilir.
Yrd.Doç.Dr. Emre YALAMAÇ
Atom Orbitallerinin Şekilleri
d orbitali: l=2 ve 5 olası ml değeri mevcuttur. -2,-1,0,+1,+2 dolayısıyla 5 değişik
oryantasyona sahiptir. 5 orbitalden 4’ünün 4 lobu vardır(yonca yaprağı) ve iki
tane dik düğüm yüzeyi ile tanımlanır. 3 tanesi xy, xz ve yz düzlemlerine diktir
ve dxy,dxz ve dyz şeklinde, 4’üncü orbital dx2-y2 şeklinde tanımlanır ve xy
düzleminde bulunur fakat lobları eksenler üzerindedir. 5.’inci orbital dz2 şeklinde
tanımlanır ve 2 majör lobu z ekseninde yer alır ve merkezde donut şeklinde
bir kemer bölgesi bulunur.
Yrd.Doç.Dr. Emre YALAMAÇ
Atom Orbitallerinin Şekilleri
f orbitali: l =3 ve 7 (2l+1) f orbitali kompleks çoklu
lob şekli oluşturur.
l =4 g orbitalleridir fakat kimyasal bağlarda
önemli bir rol oynamadığı için bahsedilmeyecektir.
H Atomunun Özel Durumu
H atomunun enerji durumu sadece temel kuantum
sayısına (n) bağlıdır. Çünkü sadece bir elektronu vardır.
Eğer elektron yüksek n orbitalini işgal ediyorsa yani
çekirdekten uzakta ise; enerjisi yüksektir. Bir diğer
değişle, n=2 orbitalleri (2s ya da 2p) aynı enerji
seviyesindedir. Tabiki diğer atomlar için elektronlar
arası itme ve çekme kuvvetlerinin etkisinden dolayı
n ve l değerleri etkendir.