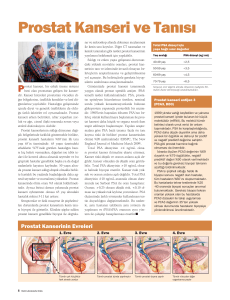
prostat hacmi
advertisement

T.C. SAĞLIK BAKANLIĞI ŞİŞLİ ETFAL EĞİTİM VE ARAŞTIRMA HASTANESİ 1.ÜROLOJİ KLİNİĞİ Şef: Prof. Dr. Erbil ERGENEKON TRUS BİYOPSİDEKİ PERİNÖRAL İNVAZYONUN TÜMÖR POZİTİF KORLAR VE BU KORLARDAKİ TÜMÖR YÜZDESİ İLE İLİŞKİSİNİN ARAŞTIRILMASI Dr. Oktay AKÇA UZMANLIK TEZİ TEZ YÖNETİCİSİ Op. Dr. Ayhan DALKILINÇ İSTANBUL – 2008 TEŞEKKÜR Üroloji eğitimim süresince derin bilgi, birikim ve tecrübelerinden faydalandığım, çalışma ortamımızı ben ve diğer asistan arkadaşlarım için samimi bir aile meclisi haline getiren çok saygıdeğer hocam klinik şefimiz Sayın Prof. Dr. Erbil EGENEKON’a, hekimlik ahlakı ve insani değerler adına birçok hususda kendisinden değerini hiçbir zaman ödeyemeyeceğim meziyetler öğrendiğim, eğitimim için hiçbir fedakarlıktan çekinmeyen çok değerli şef yardımcımız Sayın Op. Dr. Ayhan DALKILINÇ’a, asistanlık eğitimimin başlangıcında kısa bir süre de olsa bilgi ve tecrübelerinden faydalandığım hocamız Sayın Doç. Dr. Turhan ÇAŞKURLU’ya, eğitimim süresince üzerimde ciddi emekleri bulunan ve hiçbir zaman unutmayacağım uzman abilerim Op. Dr. Soner GÜNEY’e, Op. Dr. Nurettin Cem SÖNMEZ’e, Op. Dr. Serdar ARISAN’a, Op. Dr. Osman Nuri AKBULUT’a, Op. Dr. Serdar OGAN’a, Op. Dr. İlker ÇÖMEZ’e, Op. Dr. İbrahim DUMAN’a, üroloji eğitimimde çok şey borçlu olduğum, sadece medikal kimliğiyle değil sosyal kimliğiyle de kendime örnek aldığım ve o derecede de sevdiğim abim Op. Dr. Murat Can KİREMİT’e, herzaman yakın dost ve arkadaş olduğumuz Op. Dr. Bahadır ERMEÇ’e, Op. Dr. Zeynel CANOĞULLARI’na, Op. Dr. Ömer Onur ÇAKIR’a, kardeşim gibi bildiğim Op. Dr. Ramazan Gökhan ATIŞ’a, bereber sevinip beraber üzüldüğümüz, evimizden ailemizden ziyade hep birlikte olduğumuz fedakar ve çalışkan asistan kardeşlerim Dr. Burhan COŞKUN’a, Dr. Tucay ARI’ya, Dr. Yılmaz OFLUOĞLU’na, Dr. Mehmet PEHLİVANOĞLU’na, Dr. Mecit YAVUZ’a, Dr. Fatih KILINÇ’a, hem servis hemşiremiz hem ablamız olan Nurten Hemşire’ye ve Aysel Hemşire’ye, en sıkıntılı anlarında bile bizden ablalığını esirgemeyip bizi hiç kırmayan servis sekreterimiz Sema Hanım’a, ameliyathane hemşiremiz Kezban Hemşire’ye ve Sevil Hemşire’ye, Hemşire kardeşlerim Kader Hemşire, Özden Hemşire, Özgür Hemşire, Aysel Hemşire, Filiz Hemşire ,Şeniz Hemşire ve Suna Hemşire’ye, yardımcı sağlık personeline, beni her zaman anlayışla karşılayan eşime ve desteğini her zaman dağ gibi hissettiğim ailem ve arkadaşlarıma en derin saygı, sevgi, hürmet ve teşekkürlerimi bildirmeyi bir borç bilirim... Dr. Oktay AKÇA -2- İÇİNDEKİLER TEŞEKKÜR................................................................... İÇİNDEKİLER.............................................................. GİRİŞ ve AMAÇ............................................................ GENEL BİLGİLER....................................................... A) PROSTAT.......................................................... 1) Embriyoloji................................................ 2) Anatomi...................................................... B) PROSTAT KANSERİ....................................... 1) Etiyoloji ve Risk Faktörleri...................... 2) Epidemiyoloji............................................. 3) Patoloji........................................................ 4) Tanı............................................................. 5) Ayırıcı Tanı................................................ 6) Evreleme..................................................... C) TRUS................................................................... 1) Prostat Hacmi Hesaplanması.................... 2) TRUS Bulguları.......................................... 3) TRUS Biyopsi Teknikleri........................... D) TUR-P Sonrası İnsidental Prostat Kanseri...... MATERYAL ve METOD................................................ BULGULAR...................................................................... TARTIŞMA....................................................................... SONUÇ............................................................................... ÖZET.................................................................................. KAYNAKLAR................................................................... -3- 2 3 4 6 6 6 7 14 15 16 18 21 31 31 35 37 37 41 43 45 47 52 56 57 58 GİRİŞ ve AMAÇ Prostat kanseri gelişmiş ülkelerde, erkeklerde en sık görülen kanserdir (1,2). Günümüzde daha fazla hasta erken evrede tanı almaktadır. Prostat kanserinin biyolojik heterojenitesi, her hastaya spesifik tedavi planı yapmayı gerekli kılmaktadır. Bu ihtiyaç, tümörün pek çok hastada yavaş ilerleyen bir seyir göstermesi, ileri yaş hasta grubunda görülmesi, tedavi alternatiflerini karşılaştıran iyi planlanmış, randomize, yeterli izlem süresi ve hasta sayısı olan çalışmaların bulunmaması ve hastanın komorbiditesi, yaşı, yaşam kalitesi ile ilgili beklentiler gibi birçok yan faktörün seçilecek tedavi yönteminde ve elde edilecek sonuçta etkili olmasından doğmaktadır. Çok sık rastlanılan bir kanser olmasına karşın, kanser oluşumuna ve progresyona yol açan mekanizmalar net değildir (2,3). Tanıdan sonra üroonkologlar prostat kanserinin evresini ve olası senaryoları planlamak arzusundadırlar. Bunun esas nedeni, prostata sınırlı hastalığı öngörebilmektir. Çünkü bugün için potansiyel olarak “kür” sağlanabilecek prostat kanserleri sadece organa sınırlı kanserlerdir (3). Bununla beraber “latent” veya “klinik önemli olmayan” kanserleri öngörebilmek de, karar aşamasında önemlidir (4). Bir başka deyişle, prostat kanserinde agresif kanserleri öngörebilecek parametreleri bulabilmek tedavi seçimi ve takipte önem kazanmaktadır (2,3). Son 20 yılda yeni tanı koyulan prostat kanseri olgusu sayısındaki büyük artış, prostata özgü antijen (PSA) testinin çok yaygınlaşmasına ve iğne biyopsisi sayısındaki artışa bağlıdır. 1986-1991 yılları arasında 65 yaşın üzerindeki erkeklerde prostat iğne biyopsisi sayısı, 100.000’de 685’ten 2.600’e çıkmıştır (5). Bütün bu gelişmelere paralel olarak prostat görüntüleme ve biyopsi tekniklerinde de gelişmeler dikkati çekmektedir. 1963 yılında Takahashi transrektal ultrasonografi (TRUS) ile ilk kez prostatı görüntülemiştir (6). TRUS’un prostat zonal anatomisini görüntülemedeki üstünlüğü sonucunda TRUS eşliğinde prostat biyopsisi, prostat kanserinin histolojik tanısında yaygın olarak kullanılmaya başlanmıştır (7,8). Nitekim TRUS eşliğinde yapılan prostat iğne biyopsisi prostat kanseri tanısında 1989 yılında ilk kez Lee ve arkadaşları tarafından bildirildiğinden beri altın standarttır (9). Biyopsi sonucunda sadece kanser tanısı koyulmayıp aynı zamanda tedavi planı ve progresyon hesapları da yapılmaktadır. -4- Prostat kanserinde hangi tedavi uygulanırsa uygulansın, hem hastalar hem de üroonkologlar için tedavi sonuçlarıyla ilgili bazı belirsizlikler vardır. Bu belirsizlikler kanser tedavisi ve tedavi sonucu oluşabilecek ciddi yan etkileri içerir (10). Prognoz hakkında bilgi sahibi olmak, prostat kanseri tedavi alternatifleri arasında seçim yapmak ve daha sonraki dönemdeki riskleri belirlemek açısından önemlidir. Günümüzde patolojik evreyi belirlemede en önemli göstergeler; PSA, klinik evre ve histolojik derece olarak kabul edilmektedir (10). Bu göstergeler patolojik evrenin yanı sıra progresyonu göstermede de en önemli öngörü araçlarıdır (11). Bu bağlamda biyopsideki perinöral invazyonun (PNI) değerlendirilmesi de tedavi şekli, progresyon, organ sınırlılık, cerrahi sonuçlar, hastalıksız yaşam süresi, PSA nüksü olmadan yaşam süresi gibi başlıklar altında literatürde yer almaktadır (12). PNI biyopsilerde %38 oranında saptanır ve tek malignite bulgusu olabilir (13). İğne biyopsilerinde saptandığında yüksek ekstraprostatik uzanım olasılığına işaret eder (14), ancak Gelason Skoru, serum PSA ve kanser yaygınlığı göz önüne alındığında bağımsız bir prognostik faktör değildir (15), yine de varlığı ekstraprostatik uzanım ile ilişkilidir (%93-%38) (16,17). Buna karşın lenf nodu metastazı ve progresyonu bağımsız olarak öngördüğünü, radyoterapi ardından olumsuz gidişle ilişkili bağımsız bir risk faktörü olduğunu bildiren çalışmalar da vardır (18). Alberto ve ark.’nın 2007 yılında yapmış oldukları çalışmada biyopsideki PNI oranı tümör hacmi hesaplamasında da kullanılmıştır (19). Algaba ve ark. 2005’te 300 hastanın biyopsi ve radikal prostatektomi sonuçlarını içeren çalışmalarında biyopsideki PNI pozitifliğini, ekstraprostatik yayılım için 3,95 kat artmış risk olarak rapor etmişlerdir ve ayrıca tümör hacmiyle ilişkisini de literatüre benzer şekilde anlamlı bulmuşlardır (16,20). Biz bu çalışmamızda Nisan 2004 - Eylül 2008 arası, kliniğimizde TRUS biyopsi yapılan 282 hastadan patoloji sonucu prostat adenokarsinomu saptanan 85 hastanın iğne biyopsi patoloji bulgularını retrospektif olarak inceledik. İğne biyopsisindeki PNI pozitifliğinin, kanser pozitif korlar ve korlardaki tümör yüzdesi ile ilişkisini araştırmayı amaçladık. -5- GENEL BİLGİLER A) PROSTAT 1) Embriyoloji Erkek genital sisteminin en büyük aksesuar bezi olup, erkek üretrasının başlangıç kısmını oluşturur (23). Prostat, mezonefrik kanal girişinin hem yukarı hem de aşağısındaki üretral epitel tomurcuklarından gelişir. Bu basit tübüler oluşumlar 11. haftanın sonunda 5 ayrı grup halinde gelişirler ve 16. haftada gelişme tamamlanır. Bunlar dallanır ve ürogenital sinüsün etrafında farklılaşan mezenkimal hücrelerle karışan, karmaşık bir kanal sistemiyle sonuçlanır. Bu mezenkimal hücreler 16. haftada tübüller çevresinde gelişmeye başlar ve periferde daha da yoğunlaşarak prostatik kapsülü oluşturur. 22. haftada müsküler stromanın oldukça geliştiği görülür ve doğuma kadar gelişmesini sürdürür (21). Beş grup epitel tomurcuğundan nihayet anterior, posterior, median ve iki lateral lob olmak üzere 5 lob gelişmeye başlar. Başlangıçta bu loblar birbirlerinden oldukça ayrık olmasına karşın daha sonra aralarında herhangi bir septum olmaksızın birleşirler. Her bir lobun tübülleri iç içe girmez, yalnızca yan yana dururlar (21). Anterior lobun tübülleri diğer loblarınki ile aynı anda gelişmeye başlar. Erken evrelerde anterior lob tübülleri genişlemiş olmalarına ve birden fazla dallanma göstermesine karşın yavaş yavaş küçülür ve dallanmalarının çoğunu kaybederler. Kontrakte olmayı sürdürürler ve bu nedenle doğumda artık lümenleri görünmez, ufak sert embriyonik epitelyal oluşumlar şeklinde görülürler. Posterior lob daha az sayıda ancak yaygın ve daha geniş dallanmalar gösteren tübüllere sahiptir. Bu tübüller büyüdükçe gelişmekte olan median ve lateral lobların posterioruna yayılır ve prostatın rektumdan hissedilen posterior yüzeyini oluştururlar (21). PSA 28. haftada ortaya çıkar; olgun prostata kıyasla gelişmekte olan prostatın tüm kısımları ile daha zayıf reaksiyon verir. Prostatik asit fosfataz (PAP) aktivitesi PSA ile aynı zamanda ortaya çıkar, aktivitesinde farklılıklar gösterir, en yüksek aktiviteye periferal zonun lateral kesimlerinde rastlanır (22). -6- Prostatik kanallar, postpartum 5. ve 6. hafta arasında prolifere olarak sekresyon oluşturmaya başlar. Bunu takiben alveol oluşur. Maternal hormonlar tarafından indüklenen alveolar epitel ve verumontanum metaplazisi tersine döner ve prostat puberteye kadar değişmeden kalır. Puberteden sonraki 6-7 sene içinde prostat olgun büyüklüğüne erişir. Yaşamın daha sonraki bölümlerinde, stroma tarafından indüklenen transizyonel zonun periüretral bezleri farklılaşarak benign hiperplaziyi oluşturur. Erişkinde normal prostat, fibromuskuler bir stroma içinde 30-50 adet tubuloalveoler bezlerin bulunduğu bir organdır. Bezler 16-32 arasında değişen sayıdaki ekskretuvar kanalla verumontanumun iki yanından prostatik üretraya açılmaktadır. Prostat esas olarak epitelyal hücreler ve stromadan oluşur. 2) Anatomi Kısmen tubuloalveoler bezlerden, kısmen de bu bezlerin arasını dolduran ara dokudan oluşan prostat, yaklaşık 3 cm yüksekliğinde, 4 cm genişliğinde ve 2 cm kalınlığında iri bir ceviz büyüklüğünde olup, yaklaşık 18-20 gram ağırlığındadır. Prostat bezi, pelvis minörün aşağı bölümünde, symphysis pubis’in arka sınırının gerisinde, ampulla recti’nin önünde, diaphragma urogenitale’nin yukarısında ve mesane’nin altında bulunur. Prostatın basis kısmı mesane tarafında yani yukarda ve apex kısmı da aşağıda bulunur. Prostatın basis’i komşusu olduğu mesane ile devamlılık halindedir. Apex kısmı m.sphincter urethra externus ve m.transversus perinei profundus’un üst yüzü ve fasyası ile komşudur (24), (Şekil 1). Şekil 1. Prostatın Anatomisi ve Komşulukları (A ve B kesit yerleri). -7- a) Prostatın Lobları Bazı tümörler prostat bezinin belli bölgelerini etkilediği için prostat bezinin loblarının tarifi önemlidir. Prostat bezinin bütün lobları disseksiyonla birbirinden ayrılabilir. Bezin loblarının tamamında anatomistler arasında küçük isimlendirme farklılıkları bulunmaktadır. Bezin rektal komşuluğunu dorsal lob oluşturur. Bu kısım hariç üretranın etrafını median lob oluşturur. Daha ön kısımda ise lateral loblar vardır. Ductus ejeculatoriusların prostat bezine girerken oluşturdukları çukurlar, bezin arka yüzünü yukarıda küçük, aşağıda ise büyük olan iki bölüme ayırırlar. Yukarıda kalan küçük bölüme lobus medius denir. Bu lob, bezin üretra ve ductus ejekulatoriuslar arasında kalan bölümüdür. Arka yüzün aşağıda kalan büyük bölümünün orta kısmında uzunlamasına bir oluk bulunur. Bu median oluk, bezi lobus dexter ve lobus sinister olmak üzere iki esas bölüme ayırır. Bu iki lob üretranın arka tarafında birbirleriyle devamlılık gösterirler. Üretranın ön-üst tarafında bu lobları birbirine bağlayan bölüme ise isthmus prostate denir. Isthmus kısmı kapsül yapısında olup, bez dokusu içermez (23,25). Bazı anatomistler ise bezin loblarını üretra ve ductus ejeculatoriusları kullanarak adlandırmışlardır. Buna göre üretranın önünde kalan kısma lobus anterior, üretranın arkasında kalan kısma lobus posterior, üretra ile ductus ejeculatoriuslar arasında kalan kısma lobus medius ve yan taraflarda kalan kısımlara ise lobus lateralis (iki adet) adını verirler (24,26,27,28,29,30). b) Prostatın Zonları Prostat bezini oluşturan glandüler doku 3 farklı alt zonda incelenebilir. Bunlardan periferal zon dokunun %70’ini, santral zon %25’ini ve transizyonel (periüretral) zon ise %5’ini oluşturur. Nonglanduler doku (fibromuskuler stroma) periferal zonlar arasındaki aralıkları doldurur. Santral zon prostatik üretranın arkasında olmak üzere ductus ejeculatoriusu çevreler ve verumontanumun apexinde koni şeklini alır. Transizyonel zon, santral zonun apexinde ve ductus ejeculatoriusun hemen proksimalinde prostatik üretranın distal kısmının etrafında bulunur. Bu kısmın kanalları preprostatik sfinkterin hemen aşağısında ve periferal zonun kanallarının hemen yukarısında olmak üzere prostatik üretraya girer. Periferal zon, ön kısım hariç olmak üzere -8- santral transizyonel zonu ve prostatik üretrayı çevreler. Ön kısım ise fibromuskuler stroma ile doludur. Bu dokuda prostatik üretranın etrafında, mukus salgılayan basit bezler yer alır. Bu basit bezler kadın üretrasındaki bezlerle aynı özelliktedir (31,32). Prostat bezinin zonal anatomisi özellikle klinik olarak çok önemlidir, çünkü birçok karsinoma periferal zon kaynaklıdır. Halbuki BPH (benign prostat hipertrofisi) transizyonel zondan gelişir. Ductus ejeculatoriusu çevreleyen santral zon nadiren hastalıklardan etkilenir (31,32). Zonal anatomi bazı radyolojik görüntüleme metodlarında da önemli olup bu zonlar birbirinden ayırtedilebilir. Transrektal ultrasonografide (TRUS), santral ve periferal zonlar genellikle uniform bir yapıda görünürler ve düşük seviyeli ekojeniteye sahiptirler. Oysa prostatik üretra daha az ekojeniteye sahip bir dokuyla çevrelenir. Bu doku preprostatik sfinkter, periüretral bez dokusu ve transizyonel zondur. Ductus ejeculatoriusları görmek için bezin saggital taraması yapılmalıdır. Vesicula seminalisler ise hipoekojen yada anekojen özelliktedir (31,32), (Şekil 2, Şekil 3). Şekil 2 - Transvers Şekil 3 - Sagital Prostat zonlarının transvers ve saggital planlarda şekil çizimleri ve TRUS görüntüleri.(AFS:Anteriorfibromuskuler stroma, U:Üretra, TZ:Transziyonel zon, PZ:Periferik zon, EJD:Ejekülatör dukt, CZ:Santral zon, DV:Dorsal ven kompleksi, L:Levator kası, NVB:Nörovasculer bundle). -9- Magnetik rezonansda T2 ağırlıklı görüntülerde de zonal anatomi incelenebilir. Normal periferal zon yüksek yoğunlukta iken, santral ve transizyonel zon nispeten daha az yoğunluktadır. Verumontanum, santral zonun ortasında daha fazla yoğunlukta olduğu için rahatlıkla görüntülenebilir. Yaşın ilerlemesiyle normal olarak zonların ilişkileri değişebilir. Santral zon atrofiye olurken, transizyonel zon büyür ve sonradan BPH oluşturabilir. Bu durumda sıklıkla hipertrofiye olmuş transizyonel zonun kenarlarında, periferal zonun sıkıştırılması sonucunda düşük sinyalli bir bant oluşur (31,32). c) Prostatın Fasyaları Prostatik Fasya (Prostat Kapsülü): Bez, dış taraftan, pelvic fasyadan köken alan ince ve sağlam fibröz bir kapsülle sarılmıştır. Bu kılıf öne ve yana doğru direkt olarak devam etmektedir. Dorsal venin major dalları bu kapsülle birlikte ilerlerler. Sinir ayrılması sırasında bu kılıf yerinde bırakılmalıdır. Fibröz kapsül ön tarafta puboprostatik ligamentlerle devam ederek pubise tutunur. Aşağıda ise m. sphincter urethra externus, m.transversus perinei profundus ve perinenin derin fasyalarıyla devam eder. Arka kısımda kılıfın kökeni farklı olup tamamen avaskülerdir. Beze sıkıca yapışmış olan fibröz kılıf, bezin içine fibromuskuler bölmeler göndererek, bezi daha küçük bölümlere ayırır (25,31,32,33). Levator Fasya (Fasya Subseroza): Prostat kapsülünün dışında, pelvik fasyanın organlar üzerindeki devamı olup, oldukça gevşek bir tabakadır. Bu tabaka pelvik kaslara komşudur. Prostat bezi apexinin distalinde levator fasya, m.sphincter urethra externusun üzerini çevreler. Prostat bezini besleyen kan damarları ve otonom sinirler levator fasya ile prostatik fasya arasında ilerledikleri için burada disseksiyon esnasında çok dikkatli olunmalıdır (25,31,32,33). Retrovesical Fasya (Denonvillier Fasyası): Oldukça hassas bir bağ doku tabakası olup, rectum ön duvarı ile prostat bezi arasındaki çok dar ve klinik olarak çok önemli bir aralıkta yer alır (25,31,32,34,35). Prostat bezini oluşturan tubuloalveolar bezlerin sayısı 30-40 adet olup, kanalları kısmen birleşerek, kısmen de ayrı ayrı olarak, bazıları - 10 - colliculus seminalis üzerine, bazıları da bu kabartının yanlarındaki sinus prostaticuslara 20-30 adet delikle açılırlar (24,28,30). Prostat bezi kanallarında bir miktar salgı depo edebilir. Ejekulasyon sırasında ara dokuda bulunan kasların kasılmasıyla buradaki salgı üretraya boşaltılır (24,28,30). Prostat içinde 3 tip bez vardır; 1. Mukozal bezler: En içte yer alırlar ve mukus salgılarlar. 2. Submukozal bezler: Bezin ortasında yer alırlar. 3. Esas (external) Prostatik bezler: Bezin dış kısmımda yer alırlar, prostat salgısının büyük kısmını oluştururlar ve prostat kanseri genellikle bu bezlerden gelişir (31,32,33,34). d) Prostatın Fonksiyonu Semenin %60 kadarı seminal vesiküllerden, %20 kadarı prostat bezinden, %10 kadarı ductus deferensden ve %10 kadarı da küçük müköz bezlerle bulboüretral bezlerden gelen salgılarla oluşturulur. Prostat salgısının içinde bulunan maddeler, meninin 20-30 dk içinde akışkan hale gelmesine (likefaksiyon) neden olmaktadır. Prostat sıvısı baziktir. Kadında vajinanın pH’ı asidik olup, 3,5-4’tür. Spermler ise ortamın pH’ı 6-6,5 olana kadar hareketlilik göstermezler. Prostat bezinin salgısının pH’ının bazik olması nedeniyle ortam nötralize edilir ve spermlerin hareketliliği sağlanır. Bu da fertilizasyon için şarttır (30,31,32,36,37). Salgının bir kısmı idrarla atılır ama esas kısmı ejekulasyonda semenle birlikte atılır. Bu salgı keskin bir koku veren spermin hormonu içerir. Prostatik sıvı su, sitrik asit, asit fosfataz, amilaz, kolesterol, kalsiyum, çinko, tamponlayıcı tuzlar, fosfolipidler, prostaglandinler, fibrinojen, seminalplasmin, β-mikroseminoprotein ve prostatik spesifik antijen (PSA) içerir. Bu salgılar spermleri hareketlendirmeye ve vajina ortamının asiditesini nötralize etmeye çalışırlar. PSA, ejekulasyondan sonra meniyi sıvılaştıran serin proteaz içerir. Asit fosfataz ve PSA’nın serum değerleri prostatik karsinomanın belirlenmesinde önemli değerlerdir (30,31,32,36,37). Prostat bezinin salgısı içinde bulunan ve seminalplasmin denilen antibiyotik, penisilin, streptomisin ve tetrasiklinin antimikrobiyal aktivitesine benzer etki gösterir. Bu sayede vajinada bulunan bakteriler - 11 - yok edilerek spermlerin vajinal ortamda enfeksiyonla karşılaşması önlenerek fertilizasyona yardımcı olunur (30,31,32,36,37). e) Arterleri A.vesicalis inferior, a.pudenta interna ve a.rectalis medianın dallarıyal beslenir. Bu arterlerin dalları bez ile mesanenin birleştiği yerde arka-dış bir hat boyunca bezi delerek içine girerler. A.vesicalis inferior, vesicula seminalise ve mesane tabanına birkaç küçük dal verdikten sonra, iki tane büyük grup prostatik damarlar halinde sona erer. Mesane boynuyla prostatın birleştiği yerde beze giren arterler, mesane boynu ve üretranın periüretral kısmını beslerler. Prostatın transurethral rezeksiyonu (TUR) sırasında sıklıkla bu arterler saat 5 ve 7 yönünde karşımıza çıkmaktadırlar. Lateral pelvik fasyada pelvis yan duvarı boyunca uzanan kapsüler dallar, prostat bezinin dış kısımlarını beslerler. Arterlerin yanında venleri de içeren bu kapsüler damarlar aynı zamanda kavernöz sinirlerin dayanacağı bir iskelet görevi de görürler. Böylece nörovasculer demetler oluşur. Bu demetler mikroskobik kavernöz sinirlerin belirlenmesinde yardımcı olan makroskobik landmarklardır (24,25,28,29). f) Venleri Bütün prostat venleri v.iliaca interna ve vesical venlere drene olur. Prostattan çıkan venler bezin alt ve yan taraflarında plexus prostaticusu oluşturular. Bu plexusa prostat cerrahisi sırasında çok dikkat edilmelidir. Venöz ağların hasar görmesi çok ciddi kanamalara yol açabilir. Kapsül etrafında oluşan bu venöz plexusa gelen en önemli dal v.dorsalis penis profundadır. Bu ven, penisin derin fasyası olan Buck fasyasının altında olmak üzere penisi terkederek üregenital diyaframı deler. Bu arada 3 büyük dala sahiptir (24,25,28,29). Bunlar; Superfsial dal: Prostat ve mesane boynunun üzerinde olmak üzere orta hatta seyreder. Retropubik operasyonlarda kolaylıkla görülebilir. Mesane pelvik yan duvarlarına birleştirici dallar verir. Sağ ve Sol lateral plexuslar: Mesane boynuna doğru arkaya dışa giden plexuslar daha sonra obturator ve vesical plexuslarla birleşirler. Bunlara ilave olarak prostat bezinin ön tarafında bezin apexi çok yoğun vasküler bir dorsal venöz plexus ile çevrelenmiştir. Buna Santorini Dorsal Venöz Plexusu denir. - 12 - Prostatın etrafındaki venöz plexus ile eksternal vertebral venöz plexus (ektradural venöz plexus) arasında bağlantılar bulunmaktadır. Eksternal vertebral plexus ise daha içerde bulunan internal vertebral plexus (Batson Plexusu) ile bağlantılıdır. Batson plexusu vertebra korpusundan gelen v.basivertebralislerin drene olduğu plexus olup, yukarıda ve aşağıda olmak üzere tüm vertebral kanal boyunca medulla spinalisi sarar. Yukarıda dura sinüslerinden marginal sinus ile bağlantılı olduğu için bu plexus abdomen ve pelvisdeki patolojilerin hematojenik yolla beyine geçmesine neden olan yapıdır. Tüm bu bağlantılarda kapakçık bulunmamaktadır. Özellikle öksürme, aksırma, ıkınma ve geyirme gibi karın içi basıncı artıran durumlarda, prostatın venöz akımı tersine dönerek eksternal vertebral plexusa gider. Böylece Prostat kanseri sırasında prostat bezinin bir kısım kanı kalbe gitmeden direkt olarak veretebra korpuslarına ve beyine gider. Bu bağlantılarla prostat kanserinin, uzak kemik metastazı olarak da adlandırılan vertebralara, kafa kemiklerine ve beyine neden metastaz yaptığı açıklanabilmektedir. g) Lenf Drenajı Esas olarak internal iliak lenf düğümleri olmak üzere, sakral ve obturator lenf düğümlerine drene olur. Bezin arka yüzünden çıkan bir lenf damarı, mesanenin lenf damarlarına katılarak eksternal iliak lenf düğümlerine de drene olur. Yine ön yüzden ayrılan bir lenf damarı da üretranın membranöz bölümünün damarlarıyla birlikte internal iliak lenf düğümlerine drene olur (24,25,28,29). h) İnnervasyon Pelvik organların otonomik sinirler tarafından innervasyonu adrenerjik, kolinerjik, ve nonadrenerjik-nonkolinerjik peptiderjik sinir lifleri aracılığıyla gerçekleşmektedir. Pelvik (parasempatik) ve hipogastrik (sempatik) sinirlerden oluşan pelvik ganglion dalları prostatı inerve eder (38). Parasempatik sinirler asinüslerde sonlanır ve sekresyonu uyarır. Sempatik lifler kapsül ve stromanın düz kaslarının kontraksiyonunu sağlar. Prostatik inervasyon ejekülasyon ve işemenin kontrolünü idare eder (39). Prostat intramural ganglialar gibi tek tek ayrımı zor olan birçok siniri içeren zengin bir sinir dağılımına sahiptir. Sempatik lifler; spinal kordun son 3 torasik (T10-12) ve ilk 2 lomber (L1-2) segmentlerin gri cevherlerinin lateral sütunlarından - 13 - oluşur, lomber sempatik paravertebral zincirden geçer ve süperior hipogastrik pleksus ve sempatik trunkusun pelvik uzantıları aracılığıyla pelvik pleksusa ulaşır. Süperior hipogastrik pleksus; çöliak pleksus ve iki hipogastrik sinire ayrılan ilk 4 lomber splanik sinir tarafından oluşturulur (38,40,41). Prostat diğer kromafin organlardan 5-6 kat daha fazla sempatik sinir dağılımına sahiptir (42). Parasempatik lifler; S2-4 sakral spinal sinirlerin intermediolateral sütunlarından köken alır. Pelvik splenik sinir olarak ortaya çıkarlar, hipogastrik sinirle ve sacral sempatik gangliondan gelen dallarla pelvik (inferior hipogastrik) pleksusu oluşturmak için birleşirler (41,43). Pelvik pleksus; kaudal kısmı, prostatı innerve eder ve kavernozal sinirleri oluşturur (44). Seminal veziküllerin uçlarından geçtikten sonra, bu sinirler lateral endopelvik fasyada Denonvillier fasyasıyla birleşme yerine yakın uzanırlar (45). Prostatın posterolateral sınırında rektum önünde ve prostatik kapsüler damarların lateralinde seyrederler (46,47). Bu yapı nörovasküler demet (NVB) olarak adlandırılır. Prostatik cerrahi sırasında, özellikle saat 5 ve 7 lokalizasyonunda olmak üzere apekste bu sinirler yaralanmaya açıktır (48,49). Bu demetten çıkan bazı sinir lifleri prostat kapsülünü perfore ettikten sonra sonlanırlar (43). Pelvik pleksusun anterior dallarından gelen diğer lifler mesane boynunun ön yüzü ile birleşmek için prostatın lateral yüzeyinden geçerler (43). B) PROSTAT KANSERİ Prostat kanseri gelişmiş ülkelerde, erkeklerde en sık görülen kanserdir (1,2). Günümüzde daha fazla hasta erken evrede tanı almaktadır. Prostat kanserinin biyolojik heterojenitesi, her hastaya spesifik tedavi planı yapmayı gerekli kılmaktadır. Bu ihtiyaç, tümörün pek çok hastada yavaş ilerleyen bir seyir göstermesi, ileri yaş hasta grubunda görülmesi, tedavi alternatiflerini karşılaştıran iyi planlanmış, randomize, yeterli izlem süresi ve hasta sayısı olan çalışmaların bulunmaması ve hastanın komorbiditesi, yaşı, yaşam kalitesi ile ilgili beklentiler gibi birçok yan faktörün seçilecek tedavi yönteminde ve elde edilecek sonuçta etkili olmasından doğmaktadır. - 14 - Özellikle 50 yaş üzerindeki erkeklerde hasta sağlığını ciddi şekilde tehdit eden ve sıklığı artan bir kanserdir. Klinik olarak fark edilenler arasında bile biyolojik davranış ve metastatik potansiyel olarak geniş farklılıklar vardır. Prostat kanserinde klinik davranış spektrumunun çok farklı olması sonucu, her hastanın kişisel olarak tedavi edilebileceği bir çok seçenek vardır. Bu seçenekler sadece takipten, radikal cerrahi rezeksiyona kadar değişir (56). Perinöral invasyonun (PNI) ve tümör hacmi gibi parametrelerin önemi ise, 0.5cc’nin üzerindeki tümörlerin ve iğne biyopside PNI pozitif olanların daha yüksek grade, ekstrakapsüler yayılım ve metastaza eğilimli olduğu bilgisine dayanmaktadır (14,57). 1) Etyoloji ve Risk Faktörleri Etyolojisi halen kesin olarak bilinmemekle birlikte bazı faktörlerin sorumlu olabileceği bildirilmektedir. a)Yaş: Prostat kanseri riski yaşla artmaktadır. 40 yaşın altındaki erkeklerde nadiren saptanır ve yaşın ilerlemesi ile insidansı giderek artarak, 8. dekadda en üst düzeye ulaşır (57). Örneğin 39 yaşından küçük erkeklerde prostat kanseri gelişme ihtimali 1/10000 iken, 60-70 yaş arasında bu oran 1/8’e çıkar (58). Elli yaşını aşmış erkeklerin %30’unda, 80 yaşını geçmiş erkeklerin %70’inde klinik olarak bulgu vermeyen histolojik prostat kanseri bulunmaktadır. b)Irk : Belirgin coğrafi ve etnik varyasyonlar gösterir. Klinik prostat kanseri sıklığı doğu ülkelerinde düşük İskandinav ülkelerinde daha yüksektir. Zencilerde, benzer eğitim seviyesi ve sosyoekonomik durumdaki beyazlara oranla sıklık daha yüksektir (58). c)Genetik Yatkınlık : Tüm prostat kanserlerin yaklaşık %9’unda ve 55 yaşın altındaki olguların %43’ü otomozal dominant geçiş gösteren bir genetik yatkınlık saptanmıştır. Bundan 1q kromozomun uzun kolundaki HPC1 (Hereditary Prostate Cancer) geni sorumlu tutulmuştur (59). Bir erkekte kanser gelişme riski, kanserin ortaya çıkış yaşına ve etkilenen akrabaların sayısına bağlıdır. 50 yaşında kanser tanısı konmuş ve birinci derecede yakınlarında da kanser olan hastanın babasında ya da erkek kardeşinde hastalığın ortaya çıkma ihtimali, 70 yaşında tanı konmuş ve ek aile hikayesi olmayan bir hastanın babası ya da kardeşine göre 7 kat fazladır. Birinci derece akrabalarından birinde - 15 - prostat kanseri olan bir kişinin prostat kanseri gelişme riski 2 kat artarken, akraba sayısı 2 ve 3 olursa bu risk 5 ve 11 kat artmaktadır (60). d)Hormonlar: Doğumsal anorşili olgularda ve genç yaşta kastre edilenlerde kanser oluşmaması, prostat kanserli olgulara androjen verilmesiyle kanser hücrelerinde hızla çoğalma olması kastrasyonun hastalığın seyrinde dramatik bir gerilemeye neden olması hormonal faktörlerin önemli ve etkili olduğunu düşündürmektedir (58 , 61). e)Diyet: Özellikle aynı ırksal kökene sahip ama farklı coğrafi bölgelerde yetişen erkeklerde kanser insidansının farklı olması,diyetteki yağ ve kırmızı etle beslenme oranının önemli bir risk faktörü olduğunu düşündürmektedir. Son dönemde E Vitamini, selenyum ve likopen alımının prostat kanseri riskini ve özellikle agresif hastalığa karşı olduğunu belirtmişlerdir ancak tam tersini savunan literatür de mevcuttur (58). f)Enfeksiyon ve Çevresel Etkenler: Enfeksiyöz ajanların kanser etyolojisindeki rolünü araştıran epidemiyolojik, virolojik, immünolojik çalışmalarda çelişkili sonuçlar yayınlanmıştır. Çevresel faktörler ile kanser arasında tam bir sebep – sonuç ilişkisi ortaya konamamıştır (57). 2) Epidemiyoloji Prostat kanseri insidansı ırk, diyet alışkanlığı, yaşam tarzı, coğrafya, tarama çalışmaları ve “chemoprevantion” gibi nedenlerden dolayı, ülkeden ülkeye hatta aynı ülkenin farklı yerleşim bölgelerine göre değişmektedir. Orta yaşını aşmış erkeklerde kansere bağlı ölümlerde akciğer kanserinden sonra ikinci sırayı alan prostat kanseri önemli bir sağlık sorunu olmaya devam etmektedir (62). Irklara ve dünya coğrafyasına göre değişen oranlarda insidans ve mortalitesi olmakla beraber dünya üzerindeki erkeklerde görülen en sık dördüncü kanserdir. Prostat kanseri en sık siyah ırkta görülmektedir. ABD bu açıdan değerlendirildiğinde etnik kökenlere bağlı olarak farklılık göstermekle beraber bu hastalığın en sık görüldüğü ülkelerden biridir. ABD’deki Afrika kökenli erkeklerde 1995 yılı itibariyle prostat kanseri görülme insidansı yüzbinde 170, Latin kökenlilerde yüzbinde 104, Asya kökenlilerde yüzbinde 82 olarak saptanmışken beyaz ırkta bu oran yüzbinde 110’dur (63). Dünyanın diğer coğrafi bölgelerine - 16 - bakıldığında İskandinav ülkelerindeki oranın Doğu ve Güney Avrupa ülkelerine oranla daha fazla olduğu görülmektedir. Örneğin Norveç’te prostat kanseri görülme hızı yüzbinde 24 iken bu oran İspanyada yüzbinde 13’tür. Prostat kanserinin en az görüldüğü ülkeler Çin ve Japonya gibi Uzak doğu ülkeleridir. Japonya’da bu oran yüzbinde 4’tür. (64) Kuzey Avrupa ülkelerinde daha yüksek oranda saptanmasının nedeni olarak bu ülkelerde yapılan tarama testleri ve yaygın olarak uygulanan transurethral rezeksiyonun (TUR) olabileceği de düşünülebilir ama daha sonra tartışılacak olan etiyolojik faktörlerin de varlığı göz ardı edilmemelidir. Ülkemizde prostat kanseri insidansı konusunda kesin rakamlar yoktur. Fakat Fidaner ve ark. (2001)’nın 1993-94 yılları arasında İzmir’de yaptıkları çalışmada prostat kanserinin İzmir’deki insidans hızı yüzbinde 9.1 olarak belirtilmiştir. Bu oran Doğu Avrupa ülkeleri seviyesindedir ve Amerika Birleşik Devletlerinin 12’de biridir. Yaşam boyu mikroskobik prostat kanseri gelişme riski %30 civarındadır. Bu kanserlerin bir çoğu yavaş büyüme eğilimindedir ve klinik hastalık oluşturma oranı %10 dur. Böylece yaşam boyu prostat kanserinden ölme riski %3 tür. Son yıllarda klinik öneme sahip prostat kanseri insidansında önemli artışlar yaşanmaktadır. Bununla beraber dünyadaki insan populasyonu gittikçe yaşlanan bir toplum haline gelmektedir (65). Yaşlanan toplumların bir sonucu olarak prostat kanseri insidansının yıllar içinde artacağı öngörülebilir. Amerika Birleşik Devletlerinde yapılan çalışmalarda (SEER,1999) yaşa uyarlanmış prostat kanseri insidansında 1973 ve 1988 yılları arasında yıllık yüzbinde 2.7’lik bir artış tespit edilmiştir. Bu artış toplumun yaşlanması, TUR’un yaygınlaşması sonucu daha sık organa sınırlı hastalığın yakalanması, ultrasonografi ve biopsi tekniklerindeki gelişmelere paralel olarak daha fazla hastanın tanı alması gibi nedenlere bağlanmıştır. Bunu takip eden 1988 ve 1992 yılları arasında ise insidans yıllık yüzbinde 16.2’lik bir artış göstermiştir. Bu duruma neden olan en önemli faktör 1990’larda prostat spesifik antijenin kanser taraması aracı olarak yaygın bir biçimde kullanılmaya başlanmasıdır. Bu sayede daha konvansiyel metotlarla yakalanmayan her yaş grubundan kanserlere tanı konurken , eski yılların tersine daha fazla oranlarda lokalize hastalıklar tespit edilmeye başlanmıştır (66). Bütün bunların yanı sıra Danimarka’da tarama yapılmıyor olmasına rağmen kanser görülme oranının artmış olması, tarama sonucunda artan kanser - 17 - yakalama oranından çok gerçekten klinik prostat kanserinin insidansının artmakta olduğunu gösteriyor olabilir (67). Görüldüğü gibi prostat kanseri insidansı Amerika Birleşik Devletlerinde 1987’den itibaren çok hızlı bir şekilde artmış ve 1992 yılında zirve yaparak düşüşe geçmiştir (68). 1992 –95 yılları arasında yıllık yüzbinde 11.7’lik bir düşüş görülmüştür. Bu düşüşte etkili olan faktörün önceden de belirtildiği gibi tarama programları ile toplumda var olan kanserlerin çoğunluğunun ortaya çıkarılmış olması ve böylece tanı konacak hasta havuzunun küçüldüğü düşünülmektedir. 1995-1999 yılları arasında ise yıllık yüzbinde 1.4’lük bir artış saptanmıştır. Bu dönemde PSA ile yapılan taramalar sonucunda daha fazla TRUS biyopsi yapılmış ve bu nedenle de prostat kanseri insidans hızı artmıştır. Prostat kanserine bağlı mortalite değerlendirildiğinde ise 1999 SEER verilerine göre Amerika Birleşik Devletlerinde 1973-1987 arasında %0,9 , 1987–1991 arasında %3 oranında artış saptanmışken, takip eden yıllarda 19911994 arasında % 7 ve 1995-1999 yılları arasında %4,3’lük bir düşüş saptanmıştır. A.B.D’de 1995 yıllında 244.000 yeni prostat kanseri vakasına rastlanırken yaklaşık 44.000 kişi bu hastalık nedeniyle ölmüştür. Amerika Birleşik Devletleri için 2001 yılında tahmin edilen yeni vaka sayısı 198.000 olarak belirlenirken , aynı yıl 31 900 kişi prostat kanseri nedeniyle ölmüştür. Görüldüğü gibi geçen 7 yılda prostat kanserine bağlı ölümlerde bir azalma olmuştur (69). Ancak aynı şekilde 1995’de 44.000 olan ve 2001’de 31.000 rakamına gerileyen prostat kanseri ölümleri için farklı açıklamalar yapılmaktadır. Prostat kanseri için tarama yapılmasını savunan yazarlar mortalideki bu düşüşün erken tanı sayesinde hastalara verilebilen etkili tedavi programlarının eseri olduğunu öne sürmektedirler. Ancak tarama programlarının etkin olarak uygulanmadığı İngiltere ve Galler’de de 1992 sonrası prostat kanseri insidansında görülen artışın çok az olmasını ve bu ülkelerde de prostat kanseri ölümlerinin son yıllarda azalma eğilimi göstermesini bu şekilde açıklamak mümkün olmamaktadır (68). 3) Patoloji Prostat kanserleri %98 oranında adenokanserdir ve çoğunlukla periferik zondan köken alır (%70). %10-15 oranında santral zondan, - 18 - geri kalanı ise transizyonel zondan köken alır. Prostat kanseri %85 oranında multifokaldir. 40 yaşındaki her 100 erkeğin 30’unda mikroskobik latent prostat kanseri vardır. Çok yavaş geliştikleri için bir çoğu klinik önemli hale gelmezler. Klinik önemli kanser genelde 0.5 cm3’ten büyük ve/veya gleason skoru 7 ve ya daha fazla olan kanser olarak tanımlanır. Gleason skorlaması en sık kullanılan prostat kanseri derecelendirme sistemidir. Gleason skorlamasında glandüler yapı dikkate alınır. En iyi diferansiye olmuş glandın skoru 1, en az diferansiye glandın skoru 5 olacak şekilde puanlandırılır. En sık görülen gland yapısıyla, daha az görülenin skorları toplanarak toplam bir skor elde edilir. Buna kombine Gleason skoru da denmektedir. Bu skor çok önemli bir prognostik göstergedir. Gleason skorlamasına göre 10 üzerinden; 2-4 skorları iyi diferansiye, 5-7 skorları orta diferansiye, 8-10 skorları az diferansiye kanser için kullanılır (57). a)Perinöral İnvazyon: Literatürde, biyopsilerde %7-35 oranında rapor edilmektedir (16). Biyopsideki tek malignite bulgusu olabilir. Malignite için önemli bir kanıttır, ancak patognomonik değildir, çünkü nadiren benign asinuslarda da izlenebilir. Buna karşın siniri çepeçevre kucaklama, intranöral invazyon ve ganglion invazyonu sadece kanserde görülür. İğne biyopsilerinde saptandığında yüksek ekstraprostatik uzanım olasılığına işaret eder (14), ancak Gleason skoru, serum PSA ve kanser yaygınlığı göz önüne alındığında bağımsız bir prognostik faktör değildir (15), ancak varlığı ekstraprostatik uzanım ile ilişkilidir (%93-%38) (16,17). Buna karşın lenf nod metastazı ve progresyonu bağımsız olarak ön gördüğünü, radyoterapi ardından olumsuz gidişle ilişkili bağımsız bir risk faktörü olduğunu bildiren çalışmalar da vardır (18). (Şekil 4) Diğer bir yandan çok nadir olmakla beraber nöronal mesafeye benign invasyonlar da olabilir. Ali ve Epstein 2005 yılında benign prostatik dokunun perinöral yayılımını “Benign Perinöral Yayılım” olarak isimlendirmişlerdir ve 27 vaka sunmuşlardır (129). Şekil 4. PNI. Patoloji preparatındaki görüntüsü. - 19 - b)Ekstraprostatik Uzanım (EPU): Kanserin prostat sınırları veya kapsülü dışına uzanması EPU için diagnostiktir. Prostat içinde yağ dokusu son derece nadirdir. Dolayısı ile neoplastik bezler yağ hücreleri ile temas ettiğinde EPU kolayca tanınır. Ancak EPU için tümörün mutlaka adipositlerle birlikte olması şart değildir. Neoplasm prostat dışına ilerlediğinde yağ dokuda desmoplastik reaksiyona yol açar, dolayısı ile bezin dışında mı yoksa prostatın fibröz dokusu içinde mi olduğunu değerlendirmek güçleşir. Prostatın eksternal yüzeyi takip edildiğinde, dışa doğru ilerleyen tümörün yol açtığı normal dışı bir bombeleşme ve düzgün konturda bozulma, normal prostatik asinusların ötesindeki neoplastik bezlerle birlikte EPU için yeterlidir. Bu özellikle androjen deprivasyon tedavisi almış ve ekstraprostatik doku içinde desmoplastik reaksiyon uyandırabilen tümörlerde akılda tutulmalıdır. Nörovasküler demetler kanserin prostattan kaçması için en düşük direnç yollarıdır. Bu demetler posterolateral köşelerde bulunur. Yağ dokusu ile temas halinde olmasa bile nörovasküler demetlerde perinöral invasyon EPU ifadesidir. Ancak perinöral invasyon tek başına EPU göstergesi demek değildir ve prostat stroması içindeki büyük olabilecek sinirler nörovaskuler demet sanılamamalıdır. Diğer bir nokta anteriorda prostat fibromuskuler stromasının pubik kemiğe komşu çizgili ve düz kas dokusu ile iç içe olmasıdır ve bu bölgede ekstraprostatik dokuyu tayin etmeyi sağlayacak yağ dokusu genellikle yetersizdir; dolayısı ile EPU’yu tanımak zordur, ancak prostat stroması ile çizgili kas arasındaki düzgün yuvarlak sınırı tümör tartışmasız olarak aşmışsa teşhis edilebilir. En sık EPU posterior ve posterolateral prostatta izlenir, zira tümörler en sık bu bölgelerde yerleşirler. Tümör hacmiyle EPU ve seminal vesikül invasyonu arasında kuvvetli bir ilişki vardır. Bir otopsi çalışmasında hacmi 0,47cc’den düşük olan tümörlerde EPU %2 iken, daha büyük tümörlerde bu oran %52 bulunmuştur (123). EPU varlığında %57-81 hastada cerrahi sınır pozitiftir (124,125). Prostat dışında sadece bir iki neoplastik bez izlenmişse EPU’nun fokal olduğu belirtilmelidir. Nitekim EPU derecesi radikal prostatektomi sonrası progresyon riskiyle ilişkilidir. (Şekil 5). - 20 - Şekil 5. L0,L1 ve L2 prostata sınırlı hastalığın üç seviyesini göstermektedir. L3, pT3a evresindeki hastalığı gösteriyor olup “F” fokal invasyonu, “E” ise ekstraprostatik uzanımı göstermektedir.(H.Bonkhoff, Pathologe 2005·26:433–443 DOI 10.1007/s00292005-0792-z © Springer Medizin Verlag 2005). 4) Tanı Prostat kanseri periferal zondan köken aldığı için sıklıkla erken dönemde bulgu vermez. Prostat kanserine bağlı semptomların ortaya çıkması lokal ilerlemiş veya metastaz yapmış hastalığın habercisidir. Son yıllarda özellikle tarama çalışmalarının artmasıyla prostat kanserli hastaların başvuru şekilleri de oldukça değişmiştir. Önceki yıllarda prostat kanserli hastalar ileri evre hastalık nedeni ile kilo kaybı kemik ağrıları yorgunluk ve üriner retansiyon ile başvururlardı. Son zamanlarda asemptomatik olarak saptanan veya erken evrelerde yakalanan olgu sayısı artmaktadır. Mesane çıkımı obstrüksiyonu semptomları, prostat kanserinin kendisine bağlı olabileceği gibi, daha sıklıkla beraberindeki BPH’ne bağlıdır. Obstrüktif semptomlar zayıf idrar akım hızı, rezidülü işeme iken irritatif semptomlar ise urgency, sık idrara gitme olarak sayılabilir. Lokal ileri evre prostat kanseri semptomları arasında hematüri, dizüri, inkontinans sayılabilir. Nörovasküler sinir demeti invazyonuna bağlı ağrı olabilir. Rektum invazyonuna bağlı konstipasyon, tenesmus ve rektal kanama görülebilir. Seminal vezikül invazyonuna bağlı hemospermi nadir olarak gözlenebilir. Metastatik hastalığa bağlı semptomlar olarak kemik metastazlarına özellikle pelvis ve lumbar vertebra metastazlarına bağlı sırt ağrıları sayılabilir. Patolojik kırıklar ve özellikle femur başı - 21 - kırıkları görülebilir. Spinal kord kompresyonuna bağlı nörolojik semptomlar bulunabilir. Lenf nodu metastazlarına sekonder üreter obstrüksiyonu gelişebilir. Ayrıca alt ekstremite de ödem, bel ağrısı, anüri, anemi, kilo kaybı ve kanamalara sebep olabilir. Bunların dışında nadir olarak da periüreteral yayılıma bağlı olarak retroperitoneal fibrozis, paraneoplastik sendromlar ve dissemine intravasküler koagulasyon olabilir. Rutin serum PSA ve rektal muayene ile prostat kanseri taraması yapılmasının prostat kanseri mortalitesini azaltıp azaltmadığı tartışmalı bir konudur. Elli yaş üzerindeki erkeklerde parmakla muayene ve serum PSA ölçümleriyle prostat kanseri taraması yapılmasını öneren araştırmacıların dayanaklarını şu şekilde sıralayabiliriz: İlerlemiş prostat kanserinin tedavisi yoktur. Basit olan bu testler organa sınırlı hastalığı yakalamada oldukça etkindir ve organa sınırlı prostat kanserinin etkin tedavisi mümkündür. Prostat kanseri için tarama yapılmasına karşıt olanlar ise şu görüşleri savunmaktadır. Erken prostat kanseri tanısı alıp tedavi edilen ve tedavi edilmeyen hastaların uzun dönemdeki sağ kalımlarını ortaya koyan randomize bir çalışma yapılmamıştır ve erken tanının prostat kanseri mortalitesini azalttığını gösteren bir veri olmaksızın yapılan PSA ölçümü ileri gereksiz testlerin ve tedavilerin yapılmasına neden olabilir. Ayrıca tedavi hastaya fazladan morbidite yüklemektedir (70). Son yıllarda, “prostat kanser antijeni” (PCA) ile ilgili çalışmalar da artan sayıda literatürde yerini almaktadır. a) Tanı Yöntemleri Parmakla rektal inceleme (PRİ), prostat spesifik antijen (PSA) ve transrektal ultrason (TRUS) eşliğinde biyopsi, prostat kanserinin erken tanısında kullanılan tanı yöntemleridir. Prostat kanseri riskini belirlemede en yararlı olarak kullanılacak test PRİ ve PSA kombinasyonudur. Düşük prediktif değeri ve maliyet nedeniyle TRUS, tarama testinde ilk test olarak tercih edilmemektedir. Parmakla rektal inceleme prostat kanseri tanısında en basit ve en güvenli araçtır. Parmakla rektal incelemede prostat asimetrisi, nodül, seminal vezikül ve rektum patolojileri anlaşılabilir. Palpabl prostat nodüllerinin sadece - 22 - 1/3’ü aslında prostat kanseridir. Geri kalan 2/3 ise BPH, prostat taşı, prostatit, seminal vezikül anomalileri ve rektal patolojilerdir. Parmakla rektal inceleme yöntemi prostat kanserlerinin lokal yayılımlarının değerlendirilmesinde ilk kullanılan yöntemdir. Ancak, prostat kanserlerinin az bir bölümünün palpabl olması ve palpabl kanserlerin de bu aşamada prostat kapsülünü aşmış durumda bulunması, bu yöntemin önemli dezavantajlarını oluşturmaktadır (71). TRUS’un kullanım alanına girmesiyle birlikte palpabl olmayan kanserler de belirli oranda görüntülenebilir hale gelmişlerdir. TRUS ve beraberinde alınan prostat biyopsileri ile günümüzde prostat kanserinin daha yüksek oranlarda tanısı mümkün olmuştur. Bugün için PRİ’nin pozitif öngörü değeri %23 ile %56 arasında değişmektedir (71). Belirgin prostat kanseri riski nedeniyle, PRİ’sinde patoloji saptanan erkeklerden PSA düzeyleri ne olursa olsun biyopsi alma gerekliliği vardır. Çünkü prostat kanserlerinin %25’inde serum PSA değeri normal kabul edilen 4 ng/dl’nin altındadır. PRİ ile kanserlerin %23-%45’i atlanmaktadır (71). Üstelik PRİ ile yakalanan kanserler genellikle ileri evre kanserler olmaktadır. Serum PSA ölçümlerinden önceki yıllarda doktorlar sadece parmakla muayene bulgularına dayanarak kanser tanısı koymaktaydılar. b) Prostat Spesifik Antijen (PSA) 1970 yılında prostatta tanınmasını takiben, laboratuarda PSA ölçümü 10 yıl sonra 1980’de yapılmıştır. 1987’de Stamey’in ilk büyük klinik yazısını takiben, 1991 ve 1992’de yapılan tarama çalışmalarında PSA çağı gerçek anlamda başlamış ve prostat kanseri için yeni bir dönem açılmıştır. PSA semenin likefaksiyonundan sorumlu bir glikoproteindir. Kallikrein gen ailesinin bir üyesi olan PSA, bir serin proteaz olup erkeklerde prostatik epitel ve periüretral bezlerden salgılanmaktadır. PSA’yı kodlayan genin DNA sıralaması 19. kromozom üzerinde olduğu belirlenmiştir. PSA seminal sıvı içinde yüksek konsantrasyonlarda bulunmaktadır (mg/ml). Serumda ise düşük konsantrasyonlardadır (ng/ml). Serumdaki PSA %65-90 oranında bağlı durumdayken geri kalanı serbest formda bulunur. Büyük çoğunluğu alfa-1-antikimotripsin ve alfa-2-makroglobulin gibi proteazlara - 23 - bağlıdır. Bugün için immünolojik testlerle ölçülebilen serbest PSA ve alfa-1 antikimotripisine bağlı bağlı PSA’dır. Alfa-2 makroglobuline bağlı PSA serumda tespit edilememektedir. Serumdaki serbest ve bağlı PSA oranlarının ölçümleri kanser tanısını kesinleştirmek için kullanılmaktadır. Bağlı PSA serumdan karaciğer yoluyla kaldırılır. PSA’nın serumdaki yarı ömür 3 gün kadardır. Dolayısıyla radikal prostatektomi ile prostatın tamamı çıkarıldığında PSA’nın ölçülemez düzeylere düşmesi birkaç hafta alacaktır. PSA salgılanması androjenler tarafından etkilenir. Serum PSA düzeyleri puberteden sonra başlayan lüteinize edici hormon ve testosteron salgılanmasıyla birlikte artmaktadır. Serbest PSA’nın klirensi ise böbrekten glomerüler filtrasyon yoluyla veya antiproteazlarla yeni kompleksler oluşturma yoluyla olmaktadır ve yarı ömrü bağlı PSA’dan daha kısadır (2-3 saat). Serum PSA yükselmesi prostatik doku bütünlüğünün bozulması sonucu prostatik dokudan kana karışan PSA nedeniyle gerçekleşmektedir. Bu duruma prostat hastalıkları neden olabileceği gibi buna çeşitli prostat manipülasyonları da (prostat masajı, prostat biopsisi) neden olabilir. Prostat biyopsisi sonrası artan PSA düzeyinin normale dönmesi 4 haftayı bulmaktadır. PSA 4 ng/ml’nin üzerinde olan hastaların ancak %20-25’i prostat kanseri iken , PSA 10 ng/ml’nin üzerinde olanların prostat kanseri oranları %60’a kadar bildirilmiştir. Parmakla muayene sonrası serum PSA düzeylerindeki yükselmelerin klinik olarak yanlış yorumlanmayacak düzeylerde olduğu bildirilmiştir (72). Prostat hastalığının varlığı (prostat kanseri, selim prostat hiperplazisi, prostatit) PSA yükselmelerindeki en önemli faktörlerdir (73,76). PSA yüksekliği prostat hastalığını göstermektedir ancak prostat hastalığı olan herkesin serum PSA değerleri yüksek olmadığı gibi PSA yüksekliği kansere de spesifik değildir. Kanser ve selim prostat hiperplazisi için uygulanan prostata yönelik tedaviler prostatik epitelin hacmini azaltarak serum PSA düzeylerindeki düşmeye neden olur. Antiandrojenler, LHRH analogları, orşiektomi, prostatın cerrahi eksizyonu, prostat radyoterapisi serum PSA düzeyini düşüren işlemlerdir. PSA’nın rutin kullanımı, kanser yakalama oranlarını PRİ ile verilen rakamların üzerine çıkarır. PRİ’nin pozitif öngörü değerini, organa sınırlı kanserlerinin tanı alma oranını arttırır. Serum PSA değerinin yüksek olması kanser açısından tek başına parmakla muayeneden veya TRUS ile tespit edilen bir lezyondan daha değerlidir. Kanser riski serum PSA değerinin düzeyi ile - 24 - doğrudan ilişkilidir. Düzey ne kadar artarsa kanser ihtimali de o ölçüde artmaktadır (71). Her ne kadar kanser için serum PSA değerleri en yüksek pozitif prediktif değeri olan test olsa da PSA’nın parmakla muayene yapılmadan kullanılmasının sakıncalı olacağı bildirilmektedir. Çünkü kanserlerin %25’inde serum PSA değerleri 4 ng/dl değerinin altında olmaktadır. Serum PSA düzeyi ölçümleri prostat kanser tanısı almaya kadar geçen süreyi kısaltmaktadır. PSA kullanılmaya başlamadan önce prostat kanseri tanısı almış hastaların dondurulmuş serumlarında yapılan çalışmalarda, serum PSA üst sınırı 4 ng/dl alındığında hastalara tanı aldıkları gerçek tarihten 4 - 6 yıl öncesinde tanı koymanın mümkün olabileceği görülmüştür. Bir başka bulgu da PSA ile tanı konulan hastaların patolojik olarak PRİ ile tanı konulan hastalara benzerlik gösterdikleridir. Yani PSA ile tanı konulan hastalar, tıpkı palpe edilebilir bir lezyon gibi klinik olarak önemli bir grubu temsil etmektedirler (74). PSA kullanımının artması ve toplumun bilinçlenmesi Amerika Birleşik Devletlerinde “Stage migration” yaratıp, tanı alan erkeklerin yarısından fazlasının T1c evresinde, yani PSA yüksekliği nedeniyle biyopsi yapılıp organa sınırlıyken yakalanmasına yol açmıştır (75). Serum PSA düzeylerinin yaşlanma ve selim prostat hiperplazisi nedeniyle arttığının gösterilmesi, araştırmacıların PSA’nın kanser ve selim olaylar arasında ayrım yapabilme yeteneğini arttırmaya yönelik çalışmalara yöneltti. PSA’nın özgüllüğünü artırmak için literatürde birçok çalışma vardır. Bu amaçla, serum PSA değerinin prostat hacmine göre ayarlanması (PSA dansitesi), serum PSA düzeyinin yaşa göre ayarlanması, PSA düzeylerindeki değişim hızının hesaplanması (PSA velositesi, ya da hızı) gibi yöntemler PSA’nın pozitif öngörü değerini arttırmak amacıyla kullanılmaya başlanmıştır (77,78). Yeni immünolojik testlerin bulunmasıyla serum PSA’nın moleküler formaları ölçülmeye başlamış ve serbest formdaki PSA’nın düzeyleri kanser ayrımı yapmakta bir araç olarak kullanıma girmiştir. Son dönemde PSA sınırını düşürmeye yönelik araştırmalar yayınlanmaya başlanmış, PSA sınırını 3 hatta 2.5 ng/ml alırsak önemli oranda kanser yakalayabileceğimize dair önemli bilgilere ulaşılmıştır (79). Son günlerde yine bir human kallikrein gen ailesinin bir ürünü olan ve aminoaist dizilimini PSA’nınkiyle %78 benzer olan hK-2 üzerinde - 25 - durulmaktadır. hK-2’in PSA’dan daha fazla şekilde tümör spesifik olduğu Darson ve ark. tarafından da gösterildikten sonra bu protein üzerinde çalışmalar yapılmış ve hk-2/PSA oranının kesim değeri 8,3 alındığında kanser yakalamada %90’nın üzerinde özgüllük ve %60’nın üzerinde duyarlılık ile başarılı olduğu gösterilmiştir (80,81). Tek bir kan tetkikiyle serbest ve total PSA değerleri kadar kanser yakalamada etkin bir tanı aracı bulma girişimlerinde, ACT ile bağ yapan kompleks PSA düzeyleri araştırılmıştır. Yapılan çalışmalar kompleks PSA’nın tek başına total PSA kadar etkin olduğunu, kompleks/total PSA oranının S/T PSA kadar etkin olduğunu ama tek başına kompleks PSA’nın S/T PSA oranına üstünlüğü olmadığını göstermiştir (82,83,84). c) Yaşa Göre PSA Serum PSA düzeylerinin ilerleyen yaş ile artmasının nedeni yaşlılıkla büyüyen prostat bezidir. Bazı araştırmacılar bundan hareketle PSA’nın yaşa göre ayarlanmasının, her yaş için aynı üst sınırın kullanılmasına kıyasla kanser yakalamada daha başarılı olduğunu öne sürmüşlerdir. 1993 yılında Oesterling ve ark. prostat kanseri olmayan her yaş grubundan erkeklerde yaptıkları kohort çalışmada yaşa göre normal PSA düzeyi aralıklarını bildirmişlerdir. Buna göre olabilecek en yüksek normal PSA düzeyleri 40-49 yaş arası 0-2.5 ng/dl , 50-59 yaş için 0-3.5 ng/dl, 60-69 yaş için 0-4.5 ng/dl ve 70 yaş üstü için 0-6,5 ng/ml olarak belirtilmiştir. Böylece tedaviden fayda görecek olan genç hastalar daha fazla tespit edilirken tedaviden fayda görme ihtimali az olan yaşlı hastalara yapılacak olan gereksiz değerlendirmelerin de önüne geçilmiş olmaktadır (73). Ancak 50-70 yaş arası erkekler için sınır 4 ng/dl olarak kabul edilirse maksimum sayıda kanser yakalanacağını ve minimum sayıda gereksiz biyopsi yapılacağını söylemişler, yaşa göre PSA düzenlemesinin ek bir avantaj olmadığını belirtilmişlerdir (85,86). d) PSA Dansitesi Catalona ve ark. (87), PSA yüksekliği olan kişilerin %80’inin PSA düzeylerinin 4 ve 10 ng/dl arasında olduğunu belirtmişlerdir ve bu insanlardaki PSA yüksekliğinin nedeninin, kanserden çok prevelansı - 26 - yüksek olan selim prostat büyümesi olduğunu söylemişlerdir. Bu bulgudan yola çıkarak Benson ve ark. (88) serum PSA değerini prostatın ultrasonografik olarak ölçüm hacmine oranlayarak hesapladıkları PSA dansitesinin (PSAD) kanserleri ayırt etmekte yararlı bir gereç olduğunu göstermişleridir. Başka araştırmacılar da, PSAD ile kanser arasında doğrudan bir ilişkinin varlığına dikkat çekmişler ve PSA düzeyi 4-10 ng/dl arasında olan, parmakla muayenesi ve TRUS bulgularında kanser şüphesi olmayan hastalarda prostat biyopsisi almak için PSAD üst sınır değerinin 0.15 olarak bildirmişlerdir (77). Fakat PSAD’nin yararlılığı bütün çalışmalarda doğrulanmamıştır. Catalona ve ark. (87) yukarıda belirtilen değerlere göre biyopsi yapıldığında kanserlerin yarısının atlanacağını bildirmişlerdir. Brawer ve ark. (89) PSAD’nin, serum PSA değerinin 4-10 ng/dl olması durumunda kanser tanısı koymada serum PSA düzeyinin tek başına özgüllüğünü arttırmayacağını göstermişlerdir. Ayrıca pozitif biyopsisi olan erkelerin PSAD’lerinin negatif biyopsisi olanlara kıyasla yüksek olması, küçük prostatlarda sekstant biyopsilerle kanser yakalamanın daha kolay olmasından kaynaklanmaktadır (77). PSAD kullanımı ile ilgili bu çelişkili açıklamarın altında birçok değişik neden yatabilmektedir. Her şeyden önce boyutları ile prostatların salgıladıkları PSA arasında farklılıklar olmaktadır. Bunu nedeni PSA salgılayan epiteller arasında miktar olarak farklılıklar olmasıdır. Bu gün için PSA salgılayan prostat ölçecek girişimsel olmayan metod epitelinin miktarını bulunmamaktadır. Ayrıca prostat hacminin hesaplanması için geliştirilen formüllere şekil olarak uygunluk göstermeyen bazı prostatların da hesaplanan hacimleri gerçeğinden farklı olabilmektedir. Prostat kanseri olmayan erkeklerde dolaşımdaki PSA’nın belirleyicisinin transizyonel zon epiteli olduğu Lepor ve ark. (90) tarafından belirtilmiştir. Selim prostat hiperplazisinde de büyüyen kısmın transizyonel zon olması ve serum PSA düzeyinde esas olarak bu bölgenin etkili olması, transizyonel zon PSAD’nin kanser ve selim prostat hiperplazisinin ayrımında faydalı olacağı görüşünü gündeme getirmiştir (91). Her ne kadar PSAD kanser tahmini için mükemmel bir yöntem olmasa da PSA değerleri 4-10 ng/dl arasında olan erkeklerde biyopsi kararı almakta potansiyel bir yardımcı olmaktadır. Kliniğimizde 1999 yılında yapılan bir çalışmada transizyonel zon PSA dansitesinin serbest PSA yüzdesi haricinde, diğer PSA - 27 - parametrelerinden daha üstün olduğu gösterilmiştir (Sönmez NC.:Prostat kanserinde transizyonel zon PSA dansitesinin PSA ve PSA dansitesi ile karşılaştırmalı tanısal değeri.Uzmanlık tezi,1999). e) PSA Velositesi Ölçülen PSA düzeylerinin zaman içinde gösterdikleri değişim PSA velositesi ya da PSA değişim hızı olarak adlandırılır. Donmuş serumlarda yapılan çalışmalar, prostat kanseri olan hastaların serum PSA’larındaki artışın kanser olmayanlara göre daha hızlı olduğunu ve bu hızın kanser olmayanlarda yılda maksimum 0.75 ng/dl olduğunu göstermiştir (92). Başka çalışmalar da kanser olan hastaların PSA artış hızlarının yılda 0.75 ng/ml den fazla olduğunu göstermiştir. PSA değişim hızının hesaplanması için önerilen en kısa takip süresi 18 ay olarak bildirilmiştir (77). f) PSA’nın Moleküler Formları PSA’nın serumda bağlı ve serbest formlarının bulunması ve bunların ölçülebilir hale gelmesiyle bu moleküler formların kanser tespit etme yeteneğini arttırabileceği gündeme gelmiştir. Prostat kanseri olanların serumunda PSA’nın çoğunluğunun kimotripsine bağlı , az bir kısmının ise serbest olarak bulunduğu, kanser olmayanlarda ise bunun tersinin doğru olduğu görülmüştür (77). Christensson ve ark (93) prostat kanseri olan ve olmayan kişilerde serbest/total PSA oranlarına bakmışlar, 0.18 ve daha küçük oranların kanser yakalama oranını, tek başına total PSA ölçümüne kıyasla daha çok arttırdığını göstermişlerdir. Catalona ve ark. (94), PSA değerleri 4-10 ng/dl arasında olan kişilerde serbest/total PSA oranının tek başına kanser yakalamada hastanın yaşı, prostat boyutu, parmakla muayene gibi diğer parametrelerden daha değerli bilgiler verdiğini göstermişlerdir. Serbest/total PSA oranında duyarlılık ve özgüllük açısında kesim noktası olarak belirlenen rakamın optimum hale gelmesi prostat hacmine göre değişmektedir. Çünkü burada en çok büyümüş prostatı ile birlikte kanseri olanlar ve kanseri olmaksızın prostat büyümesi olanlar arasında karışıklık yaşanmaktadır. Serum PSA’sı 4-10 ng/dl arasında olan kişilerde yaptıkları çalışmada Catolana ve ark. (94) prostat hacmi - 28 - 40 cc’den büyük olanlarda serbest PSA oranının kesim noktasının %23 ve aşağısı olarak alınmasıyla gereksiz biyopsilerin %31’nin elendiğini, oysa prostat hacmi 40 cc’den küçük olan kişilerde serbest PSA oranının %14 ve aşağısı olarak belirlenmesiyle gereksiz biyopsilerin %79 oranında azaldığını belirtmişlerdir. Dolayısıyla serbest PSA ölçümleri, PSA değerleri 4-10 ng/dl arasında olan kişilerin , kanser açısından yüksek ve düşük riskli olarak sınıflandırılıp bu şekilde biyopsiye gidecek bireylerin daha sağlıklı seçilmesine yaramaktadır. PSA prostat kanseri tanısı için kullanılan testler içinde en büyük pozitif prediktif değere sahip testtir. PSA ile tespit edilen kanserler boyut ve grade olarak parmakla muayene ile tanı konulan kanserlerle kıyaslanabilir özelliktedir. Tarama çalışmaları, sadece parmakla muayene ile tanısı konan kanserlerin büyük çoğunluğunun ileri evre olduğunu, ancak parmakla muayene ve PSA ile beraber tanı konulanların ise çoğunluğunun organa sınırlı olduğunu göstermiştir. Evreleme açısından PSA, klinisyenin en çok yararlandığı yöntemlerden biri olup Gleason skoru, sistematik biyopsi ve PSA preoperatif dönemde kombine kullanılan parametrelerdir. Preoperatif gleason skoru <6, PSA <20 ng/ml ve evre T1a veya T2a kombinasyonundaki hastaların %80-90’ının hastalığı organa sınırlı iken, evresi T1b,T2b veya T2c olan hastaların %60-70’inin organa sınırlı olduğu gösterilmiştir (57). Evreleme açısından, PSA tek başına sadece %50-60’lık bir doğruluk sağlar. Örneğin Oesterling ve ark. PSA’nın doğruluk oranını kapsüler penetrasyon için %55 ve seminal vezikül ve lenf nodu tutulumu için %50 olarak yayınlamışlardır. Ercole ve ark. PSA’nın ekstrakapsüler tümörü olan hastaların %59’unda yüksek (10 ng/ml’nin üzerinde ) ve kapsüle sınırlı hastalığı olanların %7’sinde yine yüksek olduğunu rapor etmişlerdir. Stamey ve ark. PSA’nın, düzeyi 10 ng/ml’nin altında olan olguların lenf nodu tutulumuyla ilişkisiz, 40 ng/ml’nin üzerindeki seviyelerin ise %63 ihtimalle lenf nodu tutulumuyla ilişkili olduğunu bulmuşlardır (57). PSA’nın en değerli yanı, radikal prostatektomi sonrası nükslerin saptanmasıdır. PSA’nın radikal prostatektomi sonrası sıfıra inmesi beklenir aksi rezüdüel hastalık varlığını düşündürür. Radikal prostatektomi sonrası başlangıçta sıfıra inen PSA değerleri sonradan yükselirse, bu hastalığın nüks ettiğini düşündürür (57). - 29 - PSA, ilerlemiş kanseri olan hastaların takibinde de etkin tümör belirleyicisi gibi gözükmektedir. Killian ve ark. düzenli olarak ölçülen PSA değerleri ile hastalıksız sağkalım oranları arasında anlamlı bir korelasyon saptamışlardır. Ercole ve ark., evre D2 prostat kanseri olan 86 hastanın %98’inden, PSA seviyelerinde yükselme olduğunu bulmuşlardır. Stamey ve ark. evre D2 hastalığı olan 22 olgunun %100’ünde PSA’nın yüksek olduğunu saptamışlardır (57). g) Diğer Tümör Belirteçleri Tümör grade’i ve PSA’dan ayrı olarak DNA ploidisinin de kanser prognozunu belirlemede yararlı olduğu bildirilmiştir. Birçok çalışmada düşük grade’li tümörlerin diploid, yüksek grade’li tümörlerin aneuploid olduğu saptanmıştır. Tribukait’in çalışmasında da, diploid tümörlerin tedaviye aneuploid tümörlerden daha iyi cevap verdiği görülmüştür. Ploidi ile yaşanan problemler arasında, heterojen tümörlerde örnekleme hataları ve standardize yöntemlerin olmayışıdır. Ploidinin tümör grade’i üzerine, değerlendirme farklıklarından doğan hataların daha az olması gibi bir avantajı vardır (57). Tanı sırasındaki tümör hacmi de prognostik önem taşımaktadır. Birçok çalışmada ekstrakapsüler uzanım ve metastazların tümör volümüyle doğru orantılı olduğu gösterilmiştir. Buradaki problem, mevcut tekniklerin, tedaviden önce tümör volümünü doğru olarak saptamada yetersiz kalmasıdır. Bu konuda en çok kullanılan metod TRUS’tur. Bununla birlikte hipoekoik olmayan tümörlerde TRUS’un ortalama %40 hata payı bulunmaktadır. Halen klinik olarak kullanılmayan, araştırma safhasında olan bir çok teknik bulunkatadır. Örneğin, patoloji spesmeninde veya serumda polimeraz zincir reaksiyonuyla (Polymerase Chain Reaction PCR) p53 geni, retinoblastoma geni, emyc, CIS, ras, c-erbB-2, caveolin gen ekspresyonlarının tespiti, bc1 1-2, p27, Ecadherin, büyüme faktörü ve sitokin ekspresyonu seviyelerinin (tranforming growth alpha, beta) tahmin edilmesi, manyetik rezonans spektroskopisi bu yeni tekniklerdendir (57,95). - 30 - 5) Ayırıcı Tanı Rektal muayenede prostatta anormal bulgular saptanması pek çok değişik durumla ilişkili olabilir. Bir prostat anormalliğinin biyopside malign sonuçlanması ihtimali %33 ile %50 arasında değişir. Prostatik nodüller, benign hiperplazi, kronik inflamasyon ve prostatit, prostat tüberkülozu, önceki biyopsilere bağlı fibrozisler , prostat kistleri yada taşlarıyla ilişkili olabilir. Hastanın öyküsü ve fizik muayenesindeki ipuçları diğer hastalıklara yönlendirilir. Benign hiperplazi, genellikle uzun bir obstruktif üriner semptomlar hikayesi ve kanserde olduğundan daha büyük prostatla ilişkilidir. Tüberküloz, etkenle karşı karşıya kalma öyküsünde, önceden geçirilmiş pulmoner tüberküloz hikayesinde, ateş, steril piyüri varlığında akla gelmelidir. Epididim lezyonlarında prostat tutulumu da sıktır. Prostatit sıklıkla uzun bir hikaye ve prostatik sekresyonlarda ya da idrarda patolojik düzeyde lökosit bulunması durumunda düşünülmelidir. Hepsinde de tanı, biyopsi ve histopatoloji ile doğrulanır. Hematüri ve mesane çıkım obstrüksiyonu bulguları ile başvuran hastalar, diğer hematüri ve obstrüktif semptomlar yönünden araştırılmalıdır. Bunlar arasında benign prostat hiperplazisi, mesane ve böbrek patolojileri vardır. Kemik ağrısı, patolojik kırıklar ve vertebral kollaps nedeniyle omurilik basısı yine prostat kanserinin ekarte edilmesi için rektal muayeneyi gerektirir. Kemik pelviste sklerotik lezyonları, anormal serum alkalen ve asit fosfatazı olan asemptomatik hastalarda, paget hastalığı da göz önünde bulundurulmalıdır. Normal PSA düzeyleri ve ağırlık taşıyan hatlar boyunca karakteristik subperiosteal kortikal kalınlaşma paget hastalığının ayrımını sağlar. 6) Evreleme Prostat kanseri evrelemesinde ilk olarak Whitmore-Jewett sistemi kullanılmıştır. İlk sistem Whitmore tarafından 1956 yılında önerilmiştir (50). Bu öneriye göre Whitmore prostat kanserini; Evre 1: Klinik olarak latent prostat kanseri, Evre 2: Klinik olarak manifest erken prostat kanseri, Evre 3: Klinik olarak manifest, uzak metastaz belirtisi bulunmayan lokal ileri prostat kanseri ve Evre 4: Klinik olarak manifest, uzak metastaz belirtisi bulunan ileri evre prostat kanseri, - 31 - olarak sınıflandırmıştır. Bu tarife göre Evre 1’de prostatta kanser tespiti sadece patolojik olarak vardır, biyokimyasal ve klinik hiçbir belirti yoktur. Evre 2’de PRM pozitiftir, fakat hasta asemptomatiktir. Evre 3’de buna prostatizm semptomları da eklenmiştir. Evre 4’de ise metastaz varlığı şüphe götürmeyecek şekilde mevcuttur. Daha sonraki yıllarda bu sistem Prout (51) ve Jewett (52) tarafından modifiye edilmiştir. TNM Sistemi: Daha sonraki yıllarda UICC/AJCC (Union Internationale Contre le Cancer)/(American Joint Committee on Cancer) TNM (TumorNodes-Metastasis) sistemi baskın olarak kullanılmaya başlanmıştır. Prostat kanseri günümüzde artık hemen heryerde TNM sistemine göre evrelendirilmektedir. Bu sınıflandırma UICC’nin kitabına (53) göre sadece adenokarsinomlar içindir. Başka hiçbir histolojik grubu içermez. AJCC’nin sınıflandırması (54) ise biraz farklıdır. Buna göre adenokarsinom ve müsinöz, küçük hücreli, papiller, duktal, ve nöroendokrin gibi alt grupları ile prostatın skuamoz kanserleri de sınıflandırmaya dahildir, fakat sarkom yada prostatın değişici epitel hücreli kanserlerini kapsamaz. Prostatın değişici epitel hücreli kanseri, üretra tümörü olarak sınıflandırılır. Hastalığın patolojik yada sitolojik olarak kesinleştirilmesi TNM sınıflandırması için şarttır. En son versiyon 2002 yılında çıkmış ve bu sistemde bir anlamda T kategorisinin evrelendirmesinde 1992 sistemine geri dönüş yapılmıştır (53,54). Diğer kategoriler 1997 sistemi ile aynı kalmıştır. Prostat kanserinde klinik evrelendirme (cTNM) ve patolojik evrelendirme (pTNM) vardır. Patolojik evrelendirme klinik evrelendirme ile aynıdır, ancak patolojik evrelendirmede T1 kategorisi yoktur, pT2’den başlar. Patolojik evrelendirme için genellikle radikal prostatektomi yapmak gerekir. Ancak, pozitif rektum biyopsisi pT4 için, pozitif periprostatik yumuşak doku veya seminal vesikül biyopsisi pT3 sınıflandırması için yeterlidir (54). En son TNM sistemi (2002) ile orjinal Whitmore-Jewett sistemi Tablo 1’de gösterilmiştir. TNM evre grupları Tablo 2’de gösterilmiştir. - 32 - Tablo 1. 2002 TNM Sistemi ve Whitmore-Jewett Sisteminin Karşılaştırılması (55) Whitemore- TNM Primer Tümör (T) Jewett Tx Primer tümör değerlendirilemiyor To Primer tümör varlığına dair bir belirti yok A T1 Tümör klinik olarak saptanamıyor; palpe edilemiyor, görüntülenemiyor. T1a Tümör, rezeke edilen dokunun ≤ %5’inde insidental olarak mevcut. T1b Tümör, rezeke edilen dokunun > %5’inde insidental olarak mevcut A1 Tümör rezeke edilen dokunun ≤ %5’inde veya ≤ 3 kanser odağı var ve Gleason toplamı ≤ 7. A2 Tümör rezeke edilen dokunun > %5’inde veya > 3 kanser odağı var ve Gleason toplamı >7. T1c Tümör ancak iğne biyopsisi ile belirlenebiliyor. B T2 Tümör prostat dışına çıkmamış1. T2a Tümör tek bir lobun yarısında yada daha azında sınırlı. B1 Prostatın tek lobunda sınırlı < 1,5 cm palpable nodül. B2 > 1,5 cm palpable nodül. T2b Tümör tek bir lobun yarısından daha fazla yer kaplıyor. T2c Tümör her iki lobu da kaplıyor. C T3 Tümör kapsülden prostat dışına çıkıyor2. T3a Kapsül dışına taşma (tek taraflı yada çift taraflı)3. T3b Tümör seminal vesikül/leri invaze ediyor. C1 Tek taraflı seminal vesikül invazyonu. C2 Çift taraflı seminal vesikül invazyonu. C3 Kemik pelvis duvarlarına invazyon. T4 Tümör fikse yada seminal vesiküller dışındaki dokuları invaze ediyor (mesane boynu, eksternal sfinkter, rektum, levator kasları ve/veya pelvis duvarı). Bölgesel Lenf Düğümleri (N) Nx Bölgesel lenf düğümleri değerlendirilemiyor. No Bölgesel lenf düğümlerinde metastaz yok. D1 N1 Bölgesel lenf düğüm/lerinde Metastaz var Uzak Metastaz (M)4 Mx Uzak metastaz değerlendirilemiyor. Mo Uzak metastaz yok. D2 M1 Metastaz var. D2 M1a Bölgesel olmayan lenf düğüm/lerinde metastaz. D2 M1b Kemik/lerde metastaz var. D2 M1c Kemik metastazı olsun/olmasın başka bölge/lerde metastaz var. 1. İğne biyopsilerinde tek bir lobda yada iki lobda tespit edilen fakat palpe edilmeyen yada güvenilir bir şekilde görüntülenemeyen tümörler T1c olarak sınıflandırılır. - 33 - 2. Prostat apexi içine yada prostat kapsülü içine (ötesine yada dışına değil) invazyon T3 olarak değil, T2 olarak sınıflandırılır. 3. Patolojik evrelendirmede cerrahi sınır pozitifliği “R1” (mikroskobik residüel hastalık) işaretiyle belirtilmelidir. 4. Birden çok lokalizasyonda metastaz olduğu durumlarda en ileri kategori tayin edilir. En ileri kategori pM1c’dir. Tablo 2. 2002 TNM Sisteminin Evre Gruplandırması (55). Evre T Evre 1 T1a Evre 2 T1a T1b T1c T1 T2 Evre 3 T3 Evre 4 T4 Herhangi bir T Herhangi bir T N No No No No No No No No N1 Herhangi bir N M Mo Mo Mo Mo Mo Mo Mo Mo Mo M1 Derece G1 G2,3-4 Herhangi bir G Herhangi bir G Herhengi bir G Herhangi bir G Herhengi bir G Herhengi bir G Herhangi bir G Herhangi bir G DRM lokal yayılımın belirlenmesinde değerli bilgiler verebilir. Mevcut endurasyonun lateral kenarlarda devamlılığı, pelvik ve rektal duvardaki endurasyonlar, seminal veziküllerin palpe edilebilir hale gelmesi, kötü prognostik bulgulardır. Ancak DRM ile evreleme, birkaç nedenle değerlendirme hatalarına açıktır. Patolojik muayene ile karşılaşıldığında, tümör hacmi genellikle olduğundan daha küçük olarak değerlendirilir. DRM ile tüm evre T1 kanserler atlanır (57). 153 hastalık bir seride, DRM anormalliği tek lobda mevcutken, TRUS eşliğinde bilateral biyopsiler yapılmış ve %42 olguda bilateral kanser saptanmıştır (95). TRUS ile prostat kanserinin ekstrakapsüler yayılımı hakkında fikir edilinebilinir. TRUS ucuz olması, daha az zaman alması ve aynı anda biyopsi almaya imkan tanıması yönüyle avantajlıdır. BT veya MRI ile pelvik lenf nodu tutulumu araştırılabilir. BT’nin lenf nodu tutulumunu tespit etmekteki duyarlılığı %50-75, özgüllüğü %86-100, doğruluğu ise %83 - 92 arasında değişir. PSA >20 ng/ml, gleason skoru>7 olmadıkça başvurulacak bir yöntem değidir. Ganglion tutulumu için kriter, sadece lenf nodunun büyüklüğü olduğu için, yanlış negatif ve yanlış pozitif bulgular sıktır. Bu nedenle BT ancak yaygın hastalık durumunda yararlı olabilir (57). - 34 - MRI , kanser tanısında değerli değildir. Çünkü maliyeti yüksektir ve benign–malign proses MRI’da maskelenebilir. Ancak, bilinen hastalığın ekstrakapsüler ya da seminal vezikül invazyonu yapıp yapmadığını ultrasonografiye oranla dahi iyi ortaya koyar. MRI tekniğin evrelemedeki doğruluğu %83-90 arasındadır. Son zamanlarda endorektal MRI kullanım alnına girmiştir ve bu yeni teknik ekstrakapsüler yayılımı daha doğru saptamaktadır. MRI’ın bir avantajıda, nörovasküler sinir koruyucu cerrahiye yardımcı olmasıdır (57). İskelet sistemine olan metastazları belirlemede metilen difosfanat ile işaretlenmiş Tc99m sintigrafileri kullanılır. Kemik sintigrafilerinde yalancı pozitiflik oranı %2’den az olarak rapor edilmiştir. Yalancı pozitiflik nedenleri dejeneratif artrit, paget hastalığı ve travmadır. Tanıda ilgili bölgelerdeki lezyon direkt grafiler ile kontrol edilmelidir. Şüpheli durumlarda BT ince kesitleri ve lokalize (endorektal) MRI yararlı olabilir. Kesin tanı için kemik biyopsisi gerekebilir (57). Prostat kanserinde lenf nodu tutulumunu gösteren en iyi teknik pelvik lenf nodu disseksiyondur (PLND). Lateralde iliak arter lenfatiklerinin korunması, aşırı pelvik lenfatik dokunun çıkarılması ile oluşabilecek alt ekstremitede ödem riskini azaltmaktadır. Pelvik lenfadenektominin diğer komplikasyonlarından semptomatik lenfosel ancak %2-3 hastada görülmektedir. Son zamanlarda laparoskopik PLND popüler hale gelmiştir (57). C) TRANSREKTAL ULTRASONOGRAFİ (TRUS) Prostatın ultrasonik incelemesi transabdominal, perineal, transüretral ya da transrektal yoldan yapılabilir. En iyi görüntü kalitesi transrektal yoldan elde edilir. Bugünkü prostat görüntüleme tekniği 1971 yılında Watanabe tarafından önerilen yönteme dayanır (96). Transdüserin yerleştirilmesinden sonra yapılması gereken ilk hareket normal periferik zonun homojen bir görüntüsünü sağlamak olmalıdır. Çünkü görülecek olan lezyonların ekojenitesi bu görüntüyle karşılaştırılarak hipoekoik, izoekoik yada hiperekoik olarak sınıflandırılacaktır. İşleme öncelikle tranvers planda inceleme ile mesane tabanından başlanır. Seminal veziküller ve bunların ejekülatör - 35 - kanallara açıldığı bölge dikkatlice incelendikten sonra transdüser saat yönünde ve aksi yönde döndürülerek prostatın tamamı görüntülenir. Verumontanum çevresinde prostat, maksimum büyüklüğünde olduğu için buradan transvers ve anterior-posterior ölçümler yapılır. Transvers kesitler ürogenital diyafram içindeki prostat apeksine kadar alınır. Transvers incelemenin tamamlanmasını takiben biplanar transdüser saggital plana alınarak sağ tarafın önceliği ile incelemeye başlanır. Sagittal görüntüleme transdüserin mediale döndürülmesiyle yapılır. Bu esnada sefalokaudal boyut alınır, sol taraf da aynı teknikle incelenir (57). Ultrasonografik incelemede görülebilen lezyonların beli başlı olanları şöyle sıralanabilir. Sıvı dolu kistler anekoik lezyonlarla karakterizedir. Hipoekoik alanlar, normal periferik zona kıyasla ses dalgalarını daha az yansıtan bölgelerdir. İzoekoik alanlar ise görünüm olarak normal periferik zondan ayırt edilemezler. Hiperekoik, ses enerjisinin neredeyse tümünün yansıtıldığı alanlardır. Ultrasonografi sırasında bir lezyona rastlandığında o bölge inceleme sahasının ortasına alınarak detaylı olarak incelenmelidir. Transrektal ultrasonografinin birincil endikasyonu olası kanseri görüntülemek olduğundan teşhise yönelik ipuçları açısından dikkatli olunmalıdır. En önemli bulgu hipoekoik bir periferal zon lezyonudur. Bunun yanı sıra kanser açısından şüphe uyandırabilecek olan prostat kapsül düzensizliği ya da bombeleşmesi, hipoekoik alanların santral zondan seminal veziküllere doğru uzaması ya da parmakla muayenede hissedilen anormalliğe karşılık olabilecek her lezyon aynı dikkatle incelenmelidir. Non-palpabl olup TRUS ile tanı konan ve radikal prostatektomi yapılan olgularda patolojik olarak organa sınırlı pek çok hastanın bulunması bu metoda yönelik ilginin artmasına neden olmuştur. Ancak daha sonra yapılan pek çok çalışmada kanser tanısında yeterli ölçüde özgüllük ve duyarlılığa sahip olmadığı gösterilmiştir. Carter ve ark.’larının yaptığı bir çalışmada, TRUS’un özgüllüğü %68, duyarlılığı ise %52 olarak bulunmuştur. Sistematik sekstant biyopsilerin ve seminal vezikül biyopsilerinin yapılabilmesi TRUS’un güvenirliliğini arttırsa da, mesane boynuna yayılımın, üretral ve transizyonel zonun tutulumunun saptanmasında güvenilir değildir. Bütün bu bölgeler normalde karışık ekojeniteye sahiptir ve komplikasyon ihtimali nedeniyle biyopsi yapılması zordur. - 36 - Transizyonel zonda gelişen kanserler, yine transizyonel zon boyunca dağılmış küçük odaklar halindedir ve bu nedenle ultrasonografik aletlerinin rezolüsyonları dışındadır. Prostat kanserinin TRUS ile tanısı, malign nodüllerin sonografik olarak gözlendiğinde hipoekoik görünmesi gerçeğine dayanır. Malign tümörün kompakt ve ileri derecede sellüler yapısının, hücreler arasında minimal interfaz yarattığı, bunun da minimal internal ekolara neden olduğu varsayılmaktadır. 1) Prostat Hacminin Hesaplanması Prostat hacminin TRUS ile tahmini; PSA dansitesi (serum PSA’sının prostat hacmine oranı) hesaplanmasında, brakiterapi ve kriyoterapi planlanmasında önem taşımaktadır. Prostat hacminin belirlenmesinde iki yöntem tanımlanmıştır. Birinci metod prostatın bir elipsoid, küre veya prostatın sferoid olduğunu kabul ederek matematiksel bir formül ile prostat hacmini hesaplar (97). Bu formüle göre ; prostat hacmi= anterior-posteror çap x transverse çap x saggital çap x π/6 olarak hesaplanır (98). Prostatın küre olduğu kabul edilirse formül R3.π/6 olarak değiştirilir. Terris ve Stamey bu formülün 80 gr üstündeki prostatlar için daha güvenilir olduğunu söyleyerek 80 gr altındaki prostatlar için, sferoid formülü olan, R2.r.π/6 formülünü kullanmışlardır (R: Büyük çap, r: Küçük çap). Planimetrik metod ise prostattan alınan 2-5 mm’lik kesitlerin yüzey alanlarının hesaplanması ve bu alanlardan hacim tayinine gitme esasına dayanır. Bu işlem yavaş ve zahmetli olmakla birlikte diğer yöntemlere kıyasla gerçeğe daha yakın bir sonuç verir (97,98). 2) Transrektal Ultrasonografi Bulguları Prostatın ultrasonografik anatomisi 40 yaş altındaki erkeklerle daha yaşlı erkekler arasında çarpıcı farklılıklar gösterir. Gençlerde periferik ve santral zon prostatın ana kitlesini oluştururken ilerleyen yaşla birlikte ortaya çıkan benign prostat hiperplazisi (BPH) nedeniyle transizyonel zon, santral ve özellikle periferik zonu sıkıştırmaya başlar. Transrektal ultrasound’da BPH’sı olmayan erkeklerde prostat santral kesimde hipoekoik bir bölge görülür. Burası periüretral bezler, normal - 37 - transizyonel zon ve internal düz kas sfinkterinden oluşur. Bu alan orta hatta mesane boynundan verumontanum seviyesine kadar uzanır (99). Normalde santral zon ve periferik zon homojen, gri renktedir ve prostatın posterior 1/3’lük kısmını kaplar. Bu iki bölgeye oranla daha heterojen görünümlü olan transizyonel zon daha anteriorda yer alır. Transizyonel zondaki BPH nodülleri izoekoik veya hiperekoik olabilmekle beraber sıklıkla hipoekoik görünümdedir. Prostat, yaşlanmayla beraber gelen BPH nedeniyle global olarak büyür ve TRUS ile net olarak görülür. Normalde prostatın %5’ini oluşturan TZ, BPH’ın gelişmesiyle birlikte prostatın %90’ını kapsayacak şekilde büyüyebilir. Transizyonel zonun genişlemesiyle santral ve periferal zonlar sıkışır. Bu büyüme nedeniyle belirginleşen cerrahi kapsül (BPH adenomu ile normal prostat ayrımını yapan sıkışmış doku) ortaya çıkar. Sıklıkla cerrahi kapsül üzerinde noktasal kalsifikasyonlar görülür ve bu ultrasonda transizyonel zonun santral ve periferik zonlardan ayrımını kolaylaştırır. BPH’nin ekojenik paterni değişiklikler gösterir ve hipoekoik, hiperekoik veya izoekoik olabilir (100). Bazen transrektal ultrasonda transizyonel zon içinde santral yerleşimli kistlere rastlanır. Bunların ultrasonik görünümü vücudun diğer yerlerindeki kistlerden farklı olarak, hipoekoik internal eko içermeyen ve arka duvar belirginleşmesi gösteren yapılar şeklindedir. Lee ve ark.’larının (121) prostat kanserinin en sık görünümünün hipoekoik ve bir periferik zon lezyonu olduğunu göstermelerine kadar tipik prostat kanserine ait ekojenik patern tartışmalı bir konuydu (101,102,103). TRUS’un kullanılmaya başlandığı ilk yıllarda prostat kanserinin normal prostat dokusuna göre hiperekoik olduğuna dair çalışmalar yayınlanmıştır (102,103). Ancak daha sonraları 5 ve 7 MHz’lik yüksek frekanslı transdüserlerin kullanıma girmesiyle çoğu kanserlerin, özellikle küçük ve düzgün sınırlı olanların, hipoekoik görünümler verdiği anlaşılmıştır (103). Daha önceki yanılgılara, 3.5 MHz gibi düşük frekanslı transüderlerin kullanımı sonucunda yakın odaklamanın yapılamaması neden olmuştur. Yüksek frekanslı transdüserlerde ise, doku penetrasyonu düşük olmakla birlikte prostatın periferik bölgesinin rezolüsyonu artmaktadır. Kanser dokusunun çoğunlukla hipoekoik olduğu geniş kitlelerce kabul görmekle birlikte, bunun nedeni henüz aydınlatılamamıştır. 1987 yılında Salo ve ark. histolojik diferansiyasyon ve ekojenite arasında belirgin korelasyon - 38 - olduğunu göstermektedir. Yazarlar arasındaki yaygın görüş, normal prostat bezinin eko yapısının, prostatik stroma ile sıvı dolu asiner lümen arasındaki arayüzden yansıyan ses dalgalarına bağlı olduğudur. Bu nedenle, normal prostatın özellikle periferik ve santral bölgelerinde, bezlerin üniform dağılımı nedeniyle homojen ekojenik yapı ortaya çıkmaktadır. Buna göre yüksek dereceli kanserlerdeki artmış hipoekojenitenin nedeni kanserli asinuslerin az miktardaki stroma içinde birbirlerine yakın gruplaşmaları olabilir. Prostat kanserlerinde farklı ekojenik görünümlere yol açan faktörlerle ilgili değişik hipotezler ileri sürülmektedir. Tümörün büyüklüğü kanser ve normal doku arasındaki reaksiyonlar, normal dokunun infiltrasyonu, tümör içi kristaloid formasyonu bunlardan bazılarıdır. Prostat kanserlerinin ekojenik özellikleri ile ilgili farklı sonuçlar bildirilmektedir. Shinohara ve ark.’nın (104) 5 MHz’lik transdüser ile 70 prostat kanserli hasta grubunda yapmış oldukları çalışmada; tümörlerin %60’ının hipoekoik, %30’unun ise izoekoik özellikler taşıdığı bildirilmektedir. Rifkin ve arkadaşları ise 51 hastayı kapsayan serilerinde prostat kanserlerinin %59’unun hipoekoik, %12’sinin izoekoik, %20’sinin mikst ekojenik ve %10’unun hiperekoik özellikte olduğunu bildirmişlerdir (104). Literatürdeki oranlarla ilgili farklı sonuçlar araştırmacıların tümör ekojenitesini belirlerken değişik kriterler kullanmalarından kaynaklanmaktadır. Örneğin Rifkin’e göre mikst ekojenitedeki lezyon hipo ve hiperekoik foküslerin birlikte olmasını ifade etmektedir. Lezyon içindeki hipo ve hiperekoik alanlardan biri diğerinden daha fazla olabilir ya da eşit bir şekilde dağılım gösterebilir. Aynı çalışmada, tümörün ekojenitesini belirleyen en önemli faktörün stromal fibrozis olduğunu öne sürmüşlerdir. Yanı sıra, stromal fibrozisin Gleason derecesini arttırdığını göstermişlerdir. Sonuçlarına göre hiperekoik tümörler ile hipo ve hiperekoik odakların birlikte bulunduğu mikst ekojenitedeki tümörler hipoekoik olanlara göre daha yüksek Gleason dereceli grupta yer almaktadır. Diğer bazı araştırmacılara göre lezyon içinde hipoekoik bir alan varsa, hiperekoik odaklar dikkate alınmadan bu lezyonun hipoekoik olduğu kabul edilmektedir. Bu şekilde araştırmacılar arasında farklı terminoloji kullanılması yayınlanan sonuçların birbirleri ile kıyaslanmasını güçleştirmektedir. Shinohara ve ark. (104) çalışmalarında, iyi differansiye tümörlerin izoekoik, kötü diferansiye tümörlerin ise hipoekoik özellikte olduğunu - 39 - bildirmektedirler. Bu sonuç şu şekilde açıklanmaktadır; prostat kanseri normal prostat bezinden farklı yapıdadır ve küçük glandüler doku oluşturan ya da glandüler doku oluşturmayan hücrelerden oluşmaktadır. Kanser sıklıkla prostatın normal glandüler yapısını bozmakta ve içerdiği daha küçük glandüler yapılarıyla normal dokuyu işgal etmektedir. Kanserin malignite potansiyeli arttıkça glandüler doku oluşturma özelliği azalacak ve sonografik ekojeniteyi sağlayan gland sayısı da azalacaktır. Buna bağlı olarak kötü diferansiye tümörler hipoekoik yapıya sahip olacaktır. İyi diferansiye tümörler ise daha çok glandüler doku içereceğinden normal dokuya benzer arayüzler içerecek ve sonografik olarak izoekoik eko paternine sahip olacaktır. Prostat kanserinin büyüklüğününde ekojenitede önemli rolü olduğu bilinmektedir. Büyük tümörlerin daha hipoekoik olduğunu savunan görüşler bulunmakla birlikte, genel olarak küçük tümörlerin daha hipoekoik büyük tümörlerin ise daha ziyade hiper yada mikst ekojenitede oldukları öne sürülmektedir. Hipoekoik periferik zon lezyonlarının kanserin en sık görülme şekli olduğunun gösterilmesi, palpe edilemeyen kanserlerin TRUS ile teşhis edilebileceğine yönelik çalışmaların başlamasına öncülük etmiştir. Bir çalışmada Lee ve ark. 784 erkeği TRUS ile taramışlar ve TRUS’un kanser tespit etmede parmakla muayeneye kıyasla iki kat daha duyarlı olduğunu göstermişlerdir (105). Sonografik olarak tespit edilemeyen izoekoik tümörlerin oranı literatürde %12 ile %30 arasında değişmektedir. İzoekoik tümörlerin malignite potansiyelleri yönünden farklı sonuçlar bildirilmiştir. Shionara ve ark. izoekoik tümörlerin daha çok iyi ve orta dereceli diferansiye grupta yer aldığını ve hipoekoik tümörlere göre belirgin derecede daha benign olduğunu bulmuşlardır (104). Rifkin ve ark.’nın bulguları da benzerdir (103). Birçok araştırıcı sadece TRUS eşliğinde biyopsi alınan veya TRUS’un, serum PSA ve parmakla muayene ile kombine edildiği gruplarda kanser bulma oranları ile ilgili çalışmalar yapmışlardır. TRUS’un primer tarama testi olarak kullanıldığı çalışmalarda kanser yakalama oranları %1,7 ile %20 arasında değişmektedir. Her ne kadar bu farkın çalışmalara alınan vaka sayıları arasındaki farklılıklardan kaynaklanabileceği düşünülse de bu farklılığa TRUS işleminin özelliğinin de katkısı göz önüne alınmalıdır. Carter ve ark. (1989) ilk kez TRUS’un tek başına tarama amaçlı kullanıldığında göreceli olarak duyarlılığının az olabileceğine dikkat - 40 - çekmişlerdir. Çalışmalarında radikal prostatektomi yapılan hastalarda TRUS’un klinik olarak şüphelenilmeyen prostat lobundaki kanserlerin ancak %54’ünü yakalayabildiğini göstermişlerdir (106). Bunu takiben başka yazarlar da benzer sonuçlar bildirerek prostat kanserinin %20-40 olguda izoekoik yani ultrasonografik olarak görünmez olduğunu belirtmişlerdir. Ayrıca klasik kanser bulgularının bu hastalığa özgül olmadığı birçok çalışmada gösterilmiştir (121,107). Lee ve ark hipoekoik periferik zon lezyonunu patolojik incelemesinin, prostatik enfarkt veya prostatik intraepitelyal neoplazi olabileceğini göstermişlerdir. TRUS eşliğinde biyopsinin sistematik altı kadran alınmasıyla lezyona yönlendirilmiş biyopsiler alınması arasında kanser yakalama oranları arasında fark olup olmadığı da araştırma konusu olmuştur. Hodge ve ark. her iki şekilde biyopsi aldıkları 136 hastadan, kanser tespit edilen 83 hastanın sadece 3’ünde eğer lezyona yönelik biyopsi alınmasaydı kanserin atlanacağını göstermişlerdir (108). Bu bulgu, sadece anormal bölgeden örnek alınan, lezyona yönelik biyopsilerin değil, sistematik 6 kadran biyopsinin kanser yakalamada önemli olduğunu göstermiştir (106,109). 3) TRUS Biyopsi Teknikleri Prostat biyopsisi başlangıçta parmak eşliğinde lezyona yönelik yapılırken zamanla transperineal ve transrektal ultrasound eşliğinde uygulanır olmuştur. Parmak eşliğinde prostat biyopsisi tümörün sitolojik olarak derecelendirilmesine ve tanımlanmasına minimal komplikasyon riskleriyle olanak sağlasa da günümüzde kullanılmamaktadır (110). Ancak TRUS olmayan yerlerde, mobilizasyonu çok güç hastalarda, PRM’de bariz nodülü olan ve TRUS ile bu nodülü görüntülenemeyen hastalarda uygulanabilir. Transperineal prostat biyopsisinin de günümüzde kullanımı dramatik şekilde azalmıştır. Her ne kadar tanısal doğruluğu transrektal prostat biyopsilerden daha iyi olarak belirtilse de işlem süresinin uzun olması, konforsuz olması ve öğrenme sürecinin uzun olması gibi nedenlerden dolayı kullanımı sınırlıdır (111). Ancak özellikle abdominoperineal rezeksiyon geçiren hastalarda rektum olmadığından kullanılmaktadır. - 41 - Başlangıçta süpheli lezyonlardan 1 ile 5 kor sayısında hedefe yönelik biyopsiler yapılmıştır. Çoklu sayıda sistematik TRUS eşliğinde prostat biyopsilerinin parmak eşliğinde ya da TRUS eşliğinde hedefe yönelik yapılan biyopsilerden daha çok prostat kanserini tanımladığı saptanmıstır (112). Hodge ve ark. (113) 1989 yılında prostatın 6 ayrı kesiminden birer parça alınan klasik sekstant biyopsiyi tariflemişlerdir. Bu sistemde biyopsi odakları; parasagital düzlemde apeks, orta ve tabanda bilateral prostatın o tarafının orta kesiminden alınan biyopsiler olarak tanımlanmıştır. Daha sonra Stamey ve ark. (114) 1995 yılında klasik sekstant biyopsiyi laterale kaydıran tekniklerinde, altı kadran biyopsinin lobun orta kesiminden değil, 1/3 lateral kesiminden alınmasını önermişlerdir. Gore ve ark.’nın (115) 10 kor tekniği; klasik sekstant biopsiye ek olarak lateral tabanlı ve bilateral glandın orta ve taban kesimlerinden biyopsileri içermektedir. Yükselen PSA değerleri başta olmak üzere çesitli faktörler tekrar biyopsi gerekliliğine sebep olmaktadır. Tekrarlanan biyopsi sayısını azaltmak ve prostat kanseri yakalama yüzdesini artırmak için; 8,10,12, 21 kor ve üzeri kor içeren biyopsiler önerilebilmektedir (116,117,138140). Transizyonel zon spesifik biyopsilerin değeri tartışmalı olmakla birlikte, çalışmalar göstermiştir ki bu kesimden biyopsi alınması ilk defa planlanmış prostat biyopsisinde hedef olmamalıdır. Çünkü sadece bu kesimde kanser yakalama olasılığı %2’lerdedir (141,142). Şekil 6. Değişik sistemik biyopsi şemaları. A, Hodge ve ark. tarafınca sunulan orjinal Sextant Biyopsi şeması (Terries et al, 1989);B, Presti ve ark.’nın 10 kor biyopsi modeli (2000);C, 12 kor veya double sextant biyopsi. D, Eskew ve ark.’nın 13 kor “5 bölge biyopsi” modeli (1997). Biz Şişli Etfal 1.Üroloji Kliniğinde primer biyopsi şeması olarak Presti ve ark.’nın 10 kor modelini kullanmaktayız (Şekil 6). - 42 - D) TUR-P SONRASI İNSİDENTAL PROSTAT KANSERİ TUR-P günümüzde BPH cerrahi tedavisinde altın standarttır. BPH prostatın transizyonel zonundan kaynaklanır. Büyüyen adenomatöz doku, prostatik üretraya bası yaparak, obstrüktif işeme yakınmalarına neden olur. Açık prostatektomide, adenomatöz doku parmak yardımı ile enükle edilir. TUR-P’de ise, transüretral yoldan, parçalar halinde rezeke edilir. Her iki durumda da sıkışmış periferal zon (cerrahi kapsül), hastada kalır; anatomik kapsüle kadar rezeksiyon mümkün değildir. Bu nedenle, her iki yöntemde kanserin küratif tedavisi için uygun değildir. Preoperatif dönemde klinik ve laboratuvar yöntemleriyle değerlendirilerek BPH tanısı konan TUR-P spesimenlerinde insidental kanser saptanabilir. Bu olgular, saptanan tümörün hacmi, rezeke edilen sipesimenin hacminin %5’inden az olduğunda T1a, daha fazla olduğunda ise T1b olarak sınıflandırılır. Hacmi küçük olsa da iyi differansiye olmayan tümörler T1b olarak sınıflandırılmalıdır (118). T1a tümörlerde izlem iyi bir alternatifken, T1b tümörlerde radikal bir cerrahi girişim planlanması söz konusudur (119,120). Bu nedenle, özellikle küratif bir girişimden yarar görme adayı olan olgularda (10-15 yıllık yaşam beklentisi olan ko-morbiditesi olmayan hastalar) T1 tümörlerin evrelemesi büyük önem taşır. Rezeksiyon spesimenindeki tümör hacmi doğru bir evreleme için yeterli olmayabilir. Bu nedenle, rezeksiyon spesimeninde tümör bulunsa da, bulunmasa da geride tümör kalmış olma ihtimali vardır TUR-P sonrası radikal prostatektomi yapılan olguların spesimenlerinin incelendiği çalışmalarda, %20 olguda belirgin hacimde kanser saptanırken, %80 hastada minimal kanser saptandığı yada reziduel tümöre rastlanmadığı bildirilmiştir (120). Evrelemede belirleyici bir faktör de patolojik inceleme için doku hazırlanması tekniği ile ilgilidir. TUR-P ile prostat glandı, doku parçaları halinde rezeke edilir. Bu parçaların örnekleme yöntemi ile değilde tamamının incelenmesi ile, insidental prostat kanseri tanısının 2-3 kat fazla konabileceği rapor edilmiştir (119). Yine rezeksiyon materyalinin tamamının incelenmesi ile T1a olgularının bir kısmı T1b olarak saptanabilir. Rezeksiyonla, adenomatöz dokunun bir kısmı çıkarıldığından, postoperative PSA değerleri hakkında doğru bir yorum yapmak mümkün olmayabilir. Feneley ve ark.’ları PSA, PSAD, TRUS - 43 - ve PSAV değerlerinin biyopsi ile gösterilmiş rezidü tümör ile ilişkisini araştırmış (118) ve TUR-P sonrasında seri PSA ölçümlerinde yıllık %20’den fazla bir artışın reziduel tümör varlığı ile belirgin bir ilişki gösterdiğini saptamışlardır. İnsidental prostat kanserinin evrelemesinde “Re–TUR-P” önerilmektedir (118,119). Bunun nedeni TUR-P ile periferal zon, anterior prostat dokusu ve verumontanumun distalindeki apikal dokunun rezeke edilememesidir. TRUS eşliğinde periferal zon biyopsileri alınarak da rezidüel tümör araştırabileceği bildirilmiştir. Biyopside 3 örnekten fazlasında yada herhangi bir örneğin %50’den fazlasında tümör bulunması, Gleason grade 4-5 saptanması belirgin tümör yükü ile ilişkili bulunmuştur. MRI, yüksek maliyeti, kısıtlı duyarlılığı nedeni ile evre T1 prostat kanserli hastalarda önerilmemektedir (119). İnsidental prostat tümörlerinin davranışını belirlemede önerilen diğer bir yöntemde DNA ploid çalışmalarıdır. Aneuploid tümörlerin daha agresiv davranışlı olduğu bildirilmiştir. Rezidüel prostat kanseri saptanan hastalarda, uygulanan TURP’nin daha sonra yapılacak bir radikal retropubik prostatektominin sonuçları üzerinde olumsuz etkilerinin olmadığı, ancak TUR-P’nin daha sonra 1 ay içinde yapılan radikal perineal prostatektomi ve radyoterapinin komplikasyonlarını (inkontinans, mesane boynu darlığı) anlamlı oranda arttırdığı bildirilmiştir. Bu nedenle radyoterapi yapmak gerekiyorsa, TUR-P sonrası 6-8 hafta beklenmesi önerilmektedir (122). Sonuç olarak TUR-P ile insidental tümör saptananlarda izlenecek yöntem hasta yaşı ve yaşam beklentisi, rezeksiyon spesimeninin histopatolojik değerlendirilmesi, PSA artış hızı, takip döneminde anormal DRM bulgusunun çıkması ve TRUS eşliğinde alınacak biyopsi ile belirlenebilir ve hastaya göre planlanabilir (118,119,120). - 44 - MATERYAL VE METOD Nisan-2004 ile Eylül-2008 tarihleri arasında Şişli Etfal Hastanesi 1.Üroloji Kliniği’nde TRUS Biyopsi yapılan 282 hastadan patoloji sonuçları prostat adenocarcinoma saptanan 85 hastanın klinik, laboratuvar ve biyopsi patolojisi bilgileri retrospektif olarak değerlendirildi. Biyopsi sonucundaki perinöral invasyon’un, kanser pozitif korlar, korlardaki tümör yüzdesi ve klinik veriler ile (yaş, serum PSA değeri) ilişkisi araştırıldı. Biyopsi endikasyonu, genellikle PSA eşik değeri 60 yaş üstü hastalarda 4ng/dl, 60 yaş altında 2,5ng/dl kabul edilerek ve rektal muayene bulgularına göre koyuldu. Hastaya veya yakınına biyopsi için “onam formu” okutulup doldurtuldu, hem hasta hem de işlemi yapan hekim tarafınca imzalandı. Antikoagülan yada antiagregan ilaç kullanan hastaların bu tedavileri, ilgili branşların uzmanlarıyla konsulte edilerek biyopsiden bir hafta önce kesildi. Biyopsiden bir gün önce ve biyopsi günü profilaktik antibiyotik olarak ciprofloxasin 750mg tb, 1x1 pozolojisinde kullanıldı. Biyopsiden 1 saat önce Libalaks 10gr supp.lavman ile rektal temizlik yapıldı. Anestezik olarak Emla krem (lidocaine %2,5 ve prilocaine %2,5), 5gr.x5 tüp halinde lokal olarak rektal uygulandı ve 45 dakika beklendi. Sol lateral dekübit pozisyonunda, lokal antiseptik temizliğin ardından, Toshiba Diagnostic Equipment SSA-325A ultrasonografi cihazının 6 MHz PVG-600S model transrektal probu ile ilk önce TRUS yapıldı. Transvers ve sagital planlarda boyut ölçümleri yapıldı ve elipsoid yöntemle hacim hesaplandı. Hipoekoik alanlar görüntülendi ve tüm görüntülü veriler yazıcıdan çıkarılıp hastanın dosyasına eklendi. Daha sonra periferik zon’un Apex, Mid(Orta), Basis, Farlateral Anterior ve Farlateral Posterior olmak üzere 5 yerinden toplam 10 adet standart biyopsi alındı (Şekil 6. B şeması model alındı). Hipoekoik alanlardan ayrıca biyopsi alınmadı. Herhangi bir nedenle ikinci kez biyopsi endikasyonuyla biyopsi yapılan hastalardan Transizyonel zon dahil olmak üzere en az 12 kor biyopsi alındı. Ağrı yada tansiyon değişikliği (hipotansiyon, hipertansiyon, vaso-vagal senkop), anjina pektoris gibi beklenmedik durumlarda biyopsi işlemi sonlandırıldı ve bu sebeple 10 kordan daha az biyopsi alınan hastalar da çalışmaya dahil edildi. İğne - 45 - olarak Microvasive 18 G 21 cm otomatik atımlı iğne kullanıldı. Biyopsi spesmenleri, tek tek alındıkları korlara göre isimlendirilip %10’luk formalin içerisinde Eppendorf tüplerinde saklanarak patoloji laboratuvarına aynı gün gönderildi. Biyopside değerlendirilen diğer parametrelerin yanısıra herhangi bir korda gözlemlenen perinöral invasyon, raporda “PNI(+)” olarak rapor edildi. Patolojik değerlendirme Şişli Etfal Hastanesi Patoloji Kliniği’nde tek bir patolog tarafından yapıldı. Hastalar patoloji raporuna göre PNI(+) ve PNI(-) olmak üzere iki gruba ayrıldı. İki grup yaş, PSA, prostat hacimi, Gleason skoru, biyopsi alınan kor sayısı, kanser pozitif kor sayısı, pozitif kor lokalizasyonu, korlardaki tümör yüzdesi bulgularıyla istatistiksel olarak karşılaştırıldı. İstatistiksel değerlendirme için SPSS (Statistical Package For Social Sciences) 10.0 for Windows kullanıldı. Çalışma verileri değerlendirilirken tanımlayıcı istatistiksel metodların (ortalama, standart sapma) yanısıra, niceliksel verilerin karşılaştırılmasında normal dağılım gösteren parametrelerin gruplar arası karşılaştırmalarında Student T testi, normal dağılım göstermeyen parametrelerin gruplar arası karşılaştırmalarında Mann Whitney U testi kullanıldı. Niteliksel verilerin karşılaştırılmasında ise Ki-Kare testi kullanıldı. P<0.05 anlamlı olarak kabul edildi. - 46 - BULGULAR Çalışmamızdaki hastaların toplam sayısı 85 idi. Hastaların yaş ortalaması 68,31±8,36 (46-82), PSA median değeri 10,45ng/dl (11086ng/dl) (PSA değerleri nicelik bakımından normal dağılım göstermediğinden median değer belirtildi), Prostat hacimleri ortalama 44,82±23,25 (15-120), Gleason1 ortalama 3,29±0,48 (3-5), Gleason2 ortalama 3,56±0,70 (2-5), Gleason Skor ortalama 6,87±1,03 (5-10), Kor sayısı ortalama 10,14±1,39 (3-16), Pozitif kor sayısı ortalama 4,25±3,14 (1-10) olarak hesaplandı. Hastaların 64’üne serum PSA değerine göre ve 21’ine de rektal muayenedeki anormallik üzerine biyopsi yapıldı. Grafik 1’de tüm parametrelerin 85 hastadaki ortalama değerlerini görmekteyiz. 70 68,31 yıl 60 50 44cm 3 40 29,88 30 19,88 10,45 ng/dl 10 3,29 Yaş PSA 12,88 10,14 PV G1 3,56 G2 6,87 GS 4,25 KS 25,74 24,83 24,18 20,94 16,38 21,82 21,59 20,24 19,53 22,35 20 0 28,12 27,24 PKS 1,65 RA RM RB RFA RFP RT 1,26 0,88 LA LM LB LFA LFP LT Ap M B Grafik 1. TRUS biyopsi ile Prostat adenokarsinomu saptanan 85 hastanın yaş ortalaması, median PSA (ng/dl) değeri, ortalama Prostat hacmi (cm3) ve biyopsi sonucundaki kor sayısı, pozitif kor sayısı, Gleason skoru ve korlarda tesbit edilen tümör yüzde değerlerinin ortalamaları. (PV:Prostat volümü-cm3-, G1:Gleason1 skoru, G2:Gleason2 skoru, GS:Gleason toplam skoru, KS:Biyopsi alınan kor sayısı, PKS:Tümör pozitif kor sayısı, Korlarda tesbit edilen tümör yüzdelerinin ortalamaları sırasıyla RA:Sağ Apex, RM:Sağ Mid, RB:Sağ Basis, RFA:Sağ Farlat.Ant., RFP: Sağ Farlat.Post., RT:Sağ Transizyonel, LA:Sol Apex, LM:Sol Mid, LB:Sol Basis, LFA:Sol Farlat.Ant., LFP:Sol Farlat.Post., LT:Sol Transizyonel, Ap:Apex, M:Mid, B:Basis, FA:Farlat.Ant., FP:Farlat.Post., TR:Transizyonel). - 47 - FA FP TR Çalışmamızda perinöral invasyon pozitifliğini %49,4 olarak tesbit ettik. Hasta sayısı PNI(+) grupta 42 ve PNI(-) grupta ise 43 idi. PNI(+) grubun yaş ortalaması 69,90±7,64 ve PNI(-) grubun yaş ortalaması 66,74±8,81 idi. İki grup arasında yaş bakımından anlamlı farklılık yoktu (P:0,078>0,05). PNI(+) grubun PSA median değeri 17,77ng/dl (1-1047 ng/dl) ve PNI(-) grubun PSA median değeri 6,55ng/dl (2-1086ng/dl) olarak bulundu. İki grup arasında ortalama PSA değeri anlamlı derecede farklı bulundu (P:0,002<0,05). PNI(+) grubun prostat hacmi ortalaması 40,31±19,17 ve PNI(-) grubun prostat hacmi ortalaması 49,23±26,12 olarak bulundu ve anlamlı farklılık saptanmadı (P:0,17>0,05). Gleason 1 skoru ortalaması PNI(+) grupta 3,45±0,55 ve PNI(-) grupta 3,14±0,35 olarak bulundu ve fark anlamlıydı (P:0,003<0,05). Gleason 2 skoru ortalaması PNI(+) grupta 3,93±0,71 ve PNI(-) grupta 3,21±0,47 olarak hesaplandı ve anlamlı derecede farklıydı. (P:0,000<0,05). Gleason Toplam skoru ortalaması PNI(+) grupta 7,38±1,06 ve PNI(-) grupta 6,37±0,72 olarak hesaplandı ve istatistiksel olarak ileri derecede anlamlı farklılık bulundu (P:0,000<0,05). Biyopsi alınan kor sayısı ortalaması PNI(+) grupta 10,24±1,21 ve PNI(-) grupta 10,05±1,56 olarak bulundu ve anlamlı farklılık yoktu (P:0,781>0,05). Pozitif kor sayısı ortalaması PNI(+) grupta 6,21±2,88 ve PNI(-) grupta 2,33±1,97 olarak bulundu ve fark istatistiki olarak ileri derecede anlamlıydı (P:0,000<0,05). Apex’deki tümör yüzdesinin ortalama değeri PNI(+) grupta %27,14±4,87 ve PNI(-) grupta %5,87±2,43 olarak hesaplandı ve fark ileri derecede anlamlı bulundu (P:0,000<0.05). Mid’deki tümör yüzdesinin ortalaması PNI(+) grupta %43,04±5,42 ve PNI(-) grupta %6,45±2,55 olarak hesaplandı ve fark ileri derecede anlamlı bulundu (P:0,000<0,05). Basis’deki tümör yüzdesinin ortalama değeri PNI(+) grupta %41,31±5,44 ve PNI(-) olan grupta %10,52±3,02 olarak bulundu ve fark ileri dercede anlamlıydı (P:0,000<0,05). - 48 - Farlateral Anterior’daki tümör yüzdesinin ortalaması PNI(+) grupta %39,76±5,37 ve PNI(-) grupta %8,66±2,45 olarak bulundu ve fark ileri derecede anlamlıydı (P:0,000<0,05). Farlateral Posterior’daki tümör yüzdesinin ortalaması PNI(+) grupta %39,76±5,37 ve PNI(-) grupta %8,95±2,15 olarak bulundu ve fark ileri derecede anlamlıydı (P:0,000<0,05). Transizyonel Zon’daki tümör yüzdesinin ortalaması PNI(+) olan grupta %2,20±1,48 ve PNI(-) olan grupta %0,35±0,30 olarak hesaplandı ve istatistiki olarak anlamsız bulundu (P:0,217>0,05). Prostat hacmi, PSA, Gleason skoru, biyopsi alınan kor sayısı ve tümör pozitif kor sayısının PNI ile ilişkisi Grafik 2’de özetlenmiştir. 20 80 PV cm3 40 PSA 10 ng/dl PNI(-) 49,23 40,31 20 17,77 15 PNI(+) 60 5 0 6,55 0 A B 7 15 Alınan Kor Sayısı 6 13 11 9 7 6,21 5 10,24 Tümör pozitif kor sayısı 10,05 4 3 2 5 2,33 1 3 0 C D 10 9 8 7 Gleason skoru 7,38 6 6,37 5 4 3 2 3,45 3,93 3,14 3,21 1 0 G1 G2 GS E Grafik 2. A.PV:Prostat hacmi ortalamaları (cm3) B.Serum PSA ortalamaları (ng/dl) C.Biyopsi alınan kor sayısı ortalamaları D.Tümör pozitif kor sayısı ortalamaları E.G1:Gleason1, G2:Gleason2 ve GS:Gleason toplam skoru ortalamaları - 49 - PNI ile bilateral herbir korda tesbit edilen tümör yüzdelerinin (tümör hacimlerinin) ortalamalarının ilişkisi Grafik 3’de özetlenmiştir. 50 48,5 45,6 45 46,6 40 37,5 36,3 33,9 35 35,9 31,4 30,7 30 Tümör 25 22,8 yüzdesi 20 15 2,6 1,7 10 13,4 8,7 11 5 8,6 0,7 3,1 7,5 8,6 6,4 6,5 6,8 0 0 RA RM RB RFA RFP RT LA LM LB LFA LFP LT PNI(-) PNI(+) Grafik 3. Transizyonel zon’daki korlar hariç, diğer bütün korlardaki tümör yüzdelerinin ortalaması PNI(+) grupta PNI(-) gruba göre anlamlı derecede yüksekti. RA:Sağ Apex (P:0,001), RM:Sağ Mid(P:0,000), RB:Sağ Basis(P:0,000), RFA:Sağ Farlat.Ant. (P:0,000), RFP: Sağ Farlat.Post.(P:0,000) , RT:Sağ Transizyonel(P:0,384), LA:Sol Apex (P:0,003), LM:Sol Mid (P:0,000), LB:Sol Basis (P:0,000), LFA:Sol Farlat.Ant. (P:0,000), LFP:Sol Farlat.Post. (P:0,000), LT:Sol Transizyonel (P:0,217). Prostat bütün olarak değerlendirildiğinde; Apex, Mid, Basis, Farlateral Anterior, Farlateral Posterior ve Transizyonel zon’da saptanan tümör yüzdelerinin ortalamaları Grafik 4’de gösterilmiştir. PNI(+) grupta saptanan total tümör yüzdesi PNI(-) grubun 4 katıdır. 60 Tüm ör yüzdesi 40 43,04 41,31 33,51 27,14 39,76 2,1 20 5,87 0 Apex 6,45 Mid 10,52 8,66 Basis Farlat.Ant PNI(-) 8,95 Farlat.Post 0,35 Transizyonel PNI(+) Grafik 4. Apex, Mid, Basis, Farlat.Ant (Farlateral anterior), Farlat.Post (Farlateral posterior) ve Transizyonel zon’daki tümör yüzdelerinin (hacimlerinin) PNI grupları arasında dağılımı. - 50 - Biyopsideki PNI varlığının tümör pozitif korlar ile ilişkisi değerlendirildiğinde, PNI(+) grupta Transizyonel zon hariç (P:0,265) diğer tüm korlardaki tümör pozitifliğinin PNI(-) gruba göre anlamlı derecede yüksek olduğu tesbit edildi. Korlarda tümör pozitifliğinin her iki gruba dağılımı Grafik 5’de gösterilmiştir. Korların tümör pozitiflik yüzdesinin gruplar arasındaki öneminin istatistiksel değerlenirmesi KiKare ve Fisher’s Exact Test ile yapılmıştır. 90 80 88,1 85,7 83,3 85,7 70 60 Tüm ör 50 pozitif olma 40 yüzdesi 30 20 64,3 51,2 30,2 32,6 37,2 37,2 10 11,9 4,7 0 Apex Mid Basis PNI(+) Farlt.Ant. Farlt.Post. Transzynl PNI(-) Grafik 5. Biyopsi genelindeki PNI varlığının korlardaki tümör pozitifliğine etkisi. PNI(+) grupta, Apex’te tümör pozitifliği %64,3 olarak gözlendi ve bu PNI(-) gruba göre anlamlı derecede yüksekti (P:0,002). Diğer korlar için PNI(+) grupta tümör görülme yüzdeleri sırasıyla; Mid %85,7 (P:0,000), Basis %88,1 (P:0,000), Farlt.Ant. %83,3 (P:0,000), Farlt.Post. %85,7 (P:0,001) olarak saptandı ve hepsi PNI(-) gruba göre anlamlı derecede yüksekti. 85 hastanın sadece 7’sinde (%8,2) Transizyonel zon’da tümör gözlendi ve bunlardan 5’i PNI(+) grupta ve 2’si PNI(-) gruptaydı ve her iki grup arasında anlamlı farklılık yoktu (P:0,265). Biyopsideki korların tümör pozitif olma durumlarına göre biyopside PNI bulunma yüzdesinin değişimi ise Grafik 6’da belirtilmiştir. Biyopsi sonucunda Apex’de tümör saptananların %67’sinde biyopside PNI pozitifti. Bu durum sırasıyla Mid’de %72, Transizyonel’de %71, Basis’de %69,8, Farlateral anterior’da %68,6 ve Farlateral posterior’da %62 olarak gözlenmiştir. - 51 - 80 78 76 74 72 PNI Pozitifliği 70 yüzdesi 68 66 64 62 60 72 71 69,8 68,6 67 62 Apex Mid Basis Farlt.Ant. Farlt.Post. Transzynl Grafik 6. Korlardaki tümör pozitifliği ile biyopside PNI bulunma yüzdesinin ilişkisi. TARTIŞMA Perinöral invasyonun önemi ve tedavi planını etkileme noktasındaki mevcut literatür hemen hemen eşit şekilde ikiye bölünmüş durumdadır. Bir kısım yazarlar ekstakapsüler yayılımla ilişkisi olduğunu savunurken, başka yazarlar da bunun sadece spesifik hasta gruplarında savunulabileceğini rapor etmişlerdir. Yine bir kısım yazarlar lokalize hastalığın eksternal radyoterapi ile tedavisi sonrası PSA nüksünden PNI pozitifliğini sorumlu tutarken karşıt bir grup da sadece organa sınırlı hastalığı göstermede önemli olduğunu, biyokimyasal nüksü göstermede tek başına bir anlam ifade etmediğini rapor etmişlerdir. Passavanti ve ark. 2007 yılında 94 hastanın radikal prostatektomi sonuçlarında %53 PNI pozitifliği saptamışlardır, ilginç olarak radikal prostatektomi patolojisinde saptadıkları PNI’nun ancak %45’inin biyopsi patolojisinde saptanabildiğini rapor etmişlerdir, biz ise çalışmamızda biyopside PNI pozitifliğini %49,4 olarak bulduk. Bizim PNI pozitifliği sonucumuz daha yüksek görünmektedir, bunun nedeni biyopside alınan kor sayısının fazlalığı olabilir (Passavanti’nin çalışmasında biyopsilerde alınan kor sayısı belirtilmemiştir). Bir diğer neden de biyopsi alınan kor lokalizasyonları olabilir ki bu da biyopsi alınan kor lokalizasyonlarının PNI’u saptamadaki önemine işaret eder. Yine aynı çalışmada yaş ve PSA farkını PNI(+) ve PNI(-) grupları arasında anlamsız bulmuşlardır, bizim çalışmamızda iğne biyopside yaş farkı anlamsız ancak PSA farkı anlamlı çıkmıştır. Passavanti ve ark. PSA farkını, serum PSA seviyeleri 4ng/ml ile 20ng/ml arasında olan - 52 - hastalarda çalışmışlardır, fakat bizim çalışmamızda PSA aralığı çok daha geniştir. Aynı çalışmada PNI’nun yüksek Gleason skoruyla ilişkisine de değinmişlerdir, bizim çalışmamızda da bu bulgu doğrulanmıştır. Passavanti ve ark. çalışmalarının sonucunda biyopsideki PNI pozitifliğini tedavi planı için, radikal prostatektomi sonucundaki PNI pozitifliğini ise tümörün biyolojik davranışı ve progresyon için anlamlı bulmuşlardır (133). Harnden ve ark.’nın 2007 yılında internet tabanlı yapmış oldukları PNI ve prostat kanseri rekürrensi ilişkisinin sistematik review’inde Ocak 1990 ile Aralık 2005 arasındaki literatürü taramışlardır(127). Biyopsideki PNI pozitifliğinin radikal prostatektomi sonrası prostat kanseri rekürrensi ile ilişkisini araştıran 21 makale dokümante etmişlerdir ve bunlardan hiç bir çalışmanın watchful waiting grubu içermediğini rapor etmişlerdir. Harnden ve ark. bu araştırmadan yola çıkarak PNI pozitifliğinin özellikte PSA ve Gleason skoruyla birlikte prognostik bir indikatör olduğunu rapor etmişlerdir ve biyopside PNI saptanan hastaların watchful waiting için uygun olamayıp erken tedavi gerektirdiğini belirtmişlerdir (127). Bizim çalışmamızda da PNI(+) ve PNI(-) grupları arasında PSA ve Gleason skorunu anlamlı derecede farklı bulunması aynı öneriyi destekler niteliktedir (Grafik 2). Walsh ve Epstein 1993’de yapmış oldukları araştırmada iğne biyopsideki PNI pozitifliği ile prostatik kapsül penatrasyonu arasındaki ilişkiye bakmışlardır (127). PNI pozitifliğinin kapsül penatrasyonunu göstermedeki sensitivitesini %27 spesifitesini %96 olarak rapor etmişlerdir. Ancak bir taneden fazla sinir tutulumu veya tutulan sinir çapı 0,1mm’den fazla ise spesifitenin %99’a çıktığını ama sensitivitenin %9’a düştüğünü belirtmişlerdir. Sonuç olarak iğne biyopsideki perinöral invasyonun varlığının ve boyutunun bilinmesinin kapsüler penetrasyon bilgisi ve sinir koruyucu cerrahi için yardımcı olacağını rapor etmişlerdir (127). Bizim çalışmamızda patolojik incelemede sinir tutulumunun sayısı ve tutulan sinirin çapı değerlendirilmemiştir. PNI ile birlikte rapor edilen ekstra prostatik tümör ekstansiyonu literatürde yüksek oranda olduğu için bir kısım yazarlar PNI pozitif olan tarafta, cerrahi sınırın negatif olması için, nörovasküler demetin ipsilateral rutin rezeksiyonunu savunmaktadırlar. Fakat, Cannon ve ark. 2005 yılında 452 hasta ile yapmış oldukları çalışmalarında multivaryant analizde PNI pozitifliğinin pozitif cerrahi sınır ile az bir ilişkisinin olduğunu fakat - 53 - organa sınırlı hastalıkla anlamlı derecede ilişkili olduğunu rapor etmişlerdir. PNI pozitifliği yüksek oranda ekstra kapsüler ekstansiyonu predikte etmesine rağmen bilateral sinir koruyucu cerrahiyi ve pozitif cerrahi sınırı her hasta için predikte etmediğini belirtmişlerdir (128). Bizim çalışmamızdan yola çıkarak, PNI lokalizasyonlarını da içeren, radikal prostatektomi patoloji sonucuyla yapılacak çalışmalar bu konuda daha aydınlatıcı olacaktır. Bismar ve ark. 2003 yılında yapmış oldukları çalışmada iğne biyopsisindeki perinöral invasyonun, radikal prostatektomi spesmenindeki evreyi bağımsız olarak göstermediğini savunmuşlardır. PSA tabanlı yapmış oldukları toplum taramasında iğne biyopsideki histolojik grade, tümör ekstansiyonu ve perinöral invasyonun tüm prostatta bağımsız olarak patolojik evre ve cerrahi marjin durumunu öngörebilmesini araştırmışlardır. 215 hastaya sextant (6 kor) biyopsi ardından radikal prostatektomi yapmışlar ve iğne biyopside PNI %11 bulmuşlardır. PNI’nin ne varlığının ne de yokluğunun univaryant yada multivaryant değerlendirildiğinde patolojik evre ile ilişkisi gözlenmemiştir (135). Oysa biz çalışmamızda PNI(+) olanlarda korlardaki tümör yüzdesini anlamlı derecede fazla bulduk ve bunun tümör hacmini ve bunun da Algaba ve ark.’nın çalışmalarında belirttikleri gibi tümör ekstansiyonunu etkileyebileceğini düşündük (16). Ayrıca Algaba ve ark. 2005 yılında yapmış oldukları çalışmada PNI pozitifliğinin ekstaprostatik yayılımı 3,9 kat arttırdığını rapor etmişlerdir (16). Yine Epstein 1998 yılında yapmış olduğu çalışmada PNI varlığıyla birlikte 3 korda Gleason skor 7 kanser olmasının yüksek olasılıkla extraprostatik yayılıma işaret ettiğini belirtmiştir.Bununla beraber PNI’un radikal prostatektomi sonrası oluşan PSA rekürrensini, preoperatif Gleason skor, PSA ve klinik evreden bağımsız olarak etkilemediğini de belirtmiştir. Biyopsideki PNI pozitifliğinin genellikle yüksek biyopsi Gleason skoru, multiple kor tutulumu ve yüksek PSA ile birlikte olduğunu rapor etmiştir. Biyopsideki PNI pozitifliğinin, cerraha aynı tarafta nörovasküler demet (NVB) rezeksiyonu yapma hususunda fikir verebileceğini belirtmiştir. PNI pozitif olan tarafta NVB rezeksiyonu yapmanın pozitif margin oranını %17,5 azalttığını rapor etmiştir (136). Biz de çalışmamızda tutulan kor sayısı ve Gleason skorunu PNI(+) grupta anlamlı derecede yüksek bulmuş olmakla - 54 - birlikte cerrahi sonuçlarını nasıl etkilediği konusunda yorum yapamamaktayız. Bizim çalışmamızda PNI ile pozitif korlardaki tümör yüzdelerini ilişkilendirirsek; PNI(+) gruptaki tümör yüzdesi PNI(-) olanların yaklaşık 4 katıdır. Yani PNI pozitifliği muhtemelen tümör volümünü etkilemektedir. Tümör volümünün de ekstra prostatik yayılımla ilişkisi araştıran birçok yayın vardır (16). Ancak literatürde biyopsideki PNI pozitifliğini korlardaki tümör yüzdesiyle ve bunun cerrahi sonuçlara etkilerini araştıran çalışma yoktur. Bu konuda yapılacak çalışmalara ihtiyaç vardır. Yine çalışmamızda PNI pozitifliğini Perifereal zon’nun basis ve medialinden alınan biyopsilerdeki tümör pozitifliğiyle artmış ilişkili olarak gözledik. Bize göre, PNI pozitifliği ipsilateral NVB eksizyonunu predikte edebileceği için biyopside tesbit edilmesi önemlidir. Merrick ve ark. 2005 yılında brakiterapi sonrası biyokimyasal progresyonla PNI ilişkisini araştırmışlardır. 512 hastalık serilerinde (173 hasta düşük risk, 212 orta risk ve 127 yüksek risk) takip sürelerini ortalama 5,3 yıl ve PSA cutpoint değerini 0,4ng/ml veya nadir PSA olarak sunmuşlardır. Bu çalışmada PNI pozitifliğini %26 olarak saptamışlar ve brakiterapi sonrası biyokimyasal nüksle ilişkili olmadığını rapor etmişlerdir (130). Beard ve ark. 2006 yılında standart doz eksternal radyoterapi sonrası kanser spesifik survey ile PNI arasındaki ilişkiyi araştırmışlar ve 597 hastalık serilerinde radyoterapi esnasında ortalama doz olarak 70,5 Gy kullanmışlardır.Bu çalışmada radyoterapi sonrası prostat kanseri spesifik surveyi için PNI tek önemli prediktör olarak gösterilmiştir. Sonuç olarak düşük ve orta riskli prostat kanser vakalarının iğne biyopsilerinde PNI pozitifliği varsa standart doz radyoterapi sonrası kanser spesifik mortalitede PNI negatif olanlara göre anlamlı yükseklik gözlenmiş. PNI pozitif olan hastalara hormon tedavisi eklenmesi veya doz artırımı önerilmiştir (131). Lee ve ark. 1550 hastayı risk gruplarına ayırmışlar ve PNI pozitifliğinin pT3 hastalık için her grupta riski artırdığını sunmuşlardır. Ayrıca yüksek risk grubunda PNI pozitifliğini seminal vesikül ve lenf nod invasyonu için de artmış risk olarak göstermişlerdir. Yüksek risk grubundaki PNI(+) hastaların %80 oranında radikal prostatektomi sonrası radyoterapi ihtiyacı olduğunu rapor etmişlerdir (132). Yu ve ark. 2007 yılında external radyoterapi alan hastalarda PNI’nun prognostik - 55 - önemini araştırmışlardır. External radyoterapi alan 657 adet klinik lokalize prostat kanserli hastayı takip etmişler ve bu hastaların biyopsilerinde %19 PNI bildirmişlerdir. Hastalar, National Comprehansive Cencer Network kriterlerine göre risk gruplarına ayrıldığında yüksek riskli grupta PNI prevalansında artış gördüklerini belirtmişlerdir (%30). Kaplan-Meier’in analizinde PNI pozitifliği, düşük biyokimyasal rekürrens free ve düşük kanser spesifik survey ile ilişkili bulunmuştur. Univaryant ve multivaryant analizlerde PNI, biyokimyasal rekürrens için önemli prognostik faktör olarak belirlenmiştir. Lokalize prostat kanseri nedeniyle external RT alan hastalarda artmış biyokimyasal nüks için PNI bağımsız faktör olarak gösterilmiştir (134). Yukarıdaki çalışmalardan çıkarılacak ortak sonuç, PNI pozitifliğinin cerrahi tedaviler gibi radyoterapi sonuçlarını öngörmede de önemli bir prognostik faktör olduğudur. Pimer radyoterapide biyopsi dışında başka patolojik örnekleme olmadığı için PIN pozitifliğinin saptanması RT planlanan hastalarda prognostik faktör olarak daha da anlamlı hale gelmektedir. Stone ve ark. 1998 yılında 212 klinik lokalize prostat kanserli hastaya staging pelvik lenf nodu disseksiyonu yapmışlardır. Univaryant ve multivaryant analizleri sonucunda pelvik lenf nodu metastazını göstermede PNI’un, PSA, Gleason skoru ve klinik evreden daha iyi bir prediktör olduğunu rapor etmişlerdir. Hatta, brakiterapi veya external RT yapılacak olan klinik lokalize prostat kanserli hastaların iğne biyopsilerinde PNI var ise, bu hastalar için pelvik lenf nodu disseksiyonu üzerine olan tartışmaların güçlendiğini belirtmişlerdir (137). SONUÇ Üroonkologları asıl düşündüren konu prostat kanseri tanısını koymaktan ziyade tanı koyduktan sonra ne yapılacağıdır. PSA ve rektal muayene bulgularından sonra hastalığa dair ilk kanıtlar TRUS biyopsi ile elde edilmektedir ve bu bulgular hastalığın gerçek patolojik evresi ve progresyonu hakkında ip uçları taşımaktadır. Biyopsideki verilerden yapılabilecek güçlü analizlerle, gereksiz cerrahiler önlenebileceği gibi hastalığa bağlı surveyi kısaltacak izlemlerden de kaçınılabilecektir. Üzerinde durulan konulardan biri de biyopsideki perinöral invasyon - 56 - varlığı ve bunun tedavi ve takipteki önemidir. Sonuç olarak çalışmamızda, iğne biyopsi patolojilerinde PNI pozitifliği olan hastaların pozitif kor sayılarını ve biyopsi korlarındaki tümör yüzdelerini anlamlı derecede yüksek bulduk. Ayrıca periferal zonun basis ve medialinde tümör pozitif olması halinde PNI pozitifliğinin daha fazla saptandığını gösterdik. Bu bulguların tedavi seçimini, cerrahi ve takip sonuçlarını nasıl etkileyeceğini anlamak için, biyopsi bulgularının radikal prostatektomi, definitif diğer tedaviler ve izlem sonuçları ile karşılaştırılacağı daha ileri çalışmalara ihtiyaç vardır. ÖZET TRUS biyopsi yapılan hastaların patoloji sonucundaki, prostat kanserinin prognostik faktörlerinden biri olan perinöral invazyonun biyopsideki pozitif korlar ve korlardaki tümör yüzdesi ile ilişkisini araştırmayı amaçladık. Nisan 2004 ile Eylül 2008 tarihleri arasında kliniğimizde TRUS biyopsi yapılan 282 hastadan patolojisi prostat adenokanseri gelen 85 hastanın biyopsi sonuçlarını retrospektif olarak inceledik. PNI pozitifliğini 42 hastada (%49,4) tesbit ettik. Hastaları PNI(+) (n:42) ve PNI (-) (n:43) olmak üzere iki gruba ayırdık. Grupları PSA, yaş, prostat hacmi, Gleason skoru, biyopsi kor sayısı, pozitif kor sayısı, pozitif kordaki tümör yüzdeleri açılarından karşılaştırdık. Gruplar arasında yaş, prostat hacmi ve biyopside alınan kor sayısı bakımından farklılık yoktu. Ancak PSA, Gleason skoru, pozitif kor sayısı ve korlardaki tümör yüzdesi PNI(+) grupta anlamlı derecede yüksekti. Yine çalışmamızda PNI pozitifliğini Perifereal zon’nun basis ve medialinden alınan biyopsilerdeki tümör pozitifliğiyle artmış ilişkili olarak gözledik. Sonuç olarak yaptığımız çalışmada PNI pozitifliğinin, iğne biyopsi sonucundaki artmış pozitif kor sayısı ve artmış tümör yüzdesiyle ileri derecede ilişkili olduğunu, ayrıca periferal zonun posterior ve medialindeki tümörlerin de PIN pozitifliğiyle ilişkili olduğunu gösterdik. Bu bulgunun tedavi planı, cerrahi ve takip sonuçlarını nasıl etkilediğini anlamak için daha ileri çalışmalara ihtiyaç vardır. - 57 - KAYNAKLAR 1) 2) 3) 4) 5) 6) 7) 8) 9) 10) 11) 12) 13) 14) 15) 16) 17) 18) 19) 20) 21) 22) 23) Greenlee RT, Hill-Harmon MB, Murray T, et al. Cancer statistics, 2001. CA Cancer J Clin. 2001;51 (1):15-36. Reiter RE, deKernion JB. Carcinoma of the prostate. In: Walsh PC, Retik AB, Vaughan ED, eds. Campbells Urology. 8th ed. New York: Saunders, 2002;3003-3024. Buhmeida A, Pyrhönen S, Laato M, et al. Prognostic factors in prostate cancer. Diagnostic Pathology 2006;1:4. McNeal JE, Bostwick DG, Kindrachuk RA, et al. Patterns of progression in prostate cancer. Lancet 1986;1:60-63. Potosky AL, Miller BA, Albertsen PC, Kramer BS. The role of icreasing detection in the rising incidence of prostate cancer. JAMA 1995;273:548-52. Takahashi H, Ouchi T: The ultrasonic diagnosis in the field of urology. Proc. Jap.Soc. Ultrasonics Med. 3: 7, 1963. Partin AW, Stutzmann RE: Elevated prostatic specific antigen, abnormal prostate evaluation on digital rectal examination, and transrectal ultrasound and prostate biopsy. Urol Clin North America. 1998; 25: 581. Metllin C, Chesley AE, Murphy GP: Association of free PSA percent, total PSA, age, and gland volume in the detection of prostate cancer. Prostate. 1999; 39: 153. Lee, F. Torp-Pedersen, S.T. and Siders, D.B.: Use of transrectal ultrasound in diagnosis, guided biopsy, staging, and screening of prostate cancer. Urology. 1989; 33:7. Ross PL, Scardino PT, Kattan MW. A catalog of prostate cancer nomograms. J Urol. 2001;165 (5):1562-8. Di Blasio CJ, Rhee AC, Cho D, et al. Predicting clinical endpoints: treatment nomograms in prostate cancer. Semin Oncol. 2003;30 (5):567-86. Harnden P, Shelley MD, Clements H, Coles B, Tyndale-Biscoe RS, Naylor B, Mason MD. The prognostic significance of perineural invasion in prostatic cancer biopsies: a systematic review. Cancer. 2007 Jan 1;109(1):13-24. Baydar DE. Prostat kanserinin patolojisi. In: Özen H, Türkeri L, et al. Üroonkoloji Kitabı. First ed. Vol 1, 562. Bastacky SI, Walsh PC, Epstein JI. Relationship between perineural tumor invasion on needle biopsy and radical prostatectomy capsular penetration in clinical stage B adenocarcinoma of the prostate. Am J Surg Pathol. 1993;17 (4):336-41. Byar DP, Mostofi FK. Carcinoma of the prostate: prognostic evaluation ofcertain pathologic features in 208 radical prostatectomies. Examined by the step-section technique. Cancer 1972;30 (1):5-13. Algaba F, Arce Y, Oliver A, Barandica C, et al. Prognostic parameters other than Gleason score for the daily evaluation of prostate cancer in needle biopsy. Eur Urol. 2005;48 (4):566-71. Vargas SO, Jiroutek M, Welch WR, et al. Perineural invasion in prostate needle biopsy specimens. Correlation with extraprostatic extension at resection. Am J Clin Pathol. 1999;111 (2):223-8. Amin M, Boccon-Gibod L, Egevad L, et al. Prognostic and predictive factors and reporting of prostate carcinoma in prostate needle biopsy specimens. Scand J Urol Nephrol Suppl. 2005; (216):20-33. Alberto A. Antunes, Miguel Srougi, et al. Preoperative Determination of Prostate Cancer Tumor Volume: Analysis through Biopsy Fragments. International Braz J Urol. Vol. 33 (4): 477-485, July - August, 2007. Bostwick DG, Graham Jr SD, Napalkov P, Abrahamsson PA, di Sant’agnese PA, Algaba F, et al. Staging of early prostate cancer: a proposed tumor volume-based prognostic index. Urology 1993;41:403–11. Tanagho EA, Mc Aninch JW. (çeviri: Kazancı G, ed.). Smith Genel Üroloji.Ondördüncü baskı. Appleton &Lange / Nobel, 1999 ; 392-433. McNeal JE: Anatomy of the prostate: An historical survey of divergent views. Prostate. 1980,1:3. Sakul U, Bilencioglu B. Prostat bezi anatomisi. In: Balbay M.D.,Prostat., 1.baskı. Güneş Kitabevi, Ankara, 2008: (3)-35. - 58 - 24) 25) 26) 27) 28) 29) 30) 31) 32) 33) 34) 35) 36) 37) 38) 39) 40) 41) 42) 43) 44) 45) 46) 47) 48) 49) 50) 51) 52) 53) 54) 55) 56) Arıncı K.: Uygulamalı Anatomi. Türkiye Klinikleri Yayınevi., Ankara,1993. Tortora GJ.: Principles of Human Anatomy, 4.ed., Harper and Row Publishers, New York, 1986. Arıncı K., Elhan A.: Anatomi. 4. Baskı, Güneş Kitabevi, Ankara,2006. Elhan A.: İnsan Anatomi Atlası (Çeviri. Köpf-Maier, P: Wolf-Heidegger’s Atlas of Human). Elhan A.: Temel Klinik Anatomi (Çeviri. Moore, K.L.), İkinci baskı, Güneş Kitabevi, 2006. Gökmen F.G.: Sistematik Anatomi, İzmir, Güven Yayınevi, 2003. Şakul B.U.: TUS için Anatomi, Ankara Üniversitesi Basımevi, Ankara, 2001. Drake R.L., Vogl W., Mitchell A.W.M.: Gray’s Anatomy for Students. Churchill Livingstone, 2005. Standring S.: Gray’s Anatomy. The Anatomical Basis of Clinical Practice. 38.ed., Churchill Livingstone, New York, 2005. Erkoçak A.: Özel Histoloji. 4. Baskı, Ankara, Ankara Tıp Yayını, 1982. Tekelioğlu M.: Tıp Embriyolojisi. Er Ajans, Ankara, 1984. Vukovic M., Krivokuca D., Moljevic N., Veljkovic R.: Denonvlliers facia-Implication for the colorectal surgeon, 2000. Guyton A.C., Hall J.E.: Text Book of Medical Physiology.9.ed., W.B. Saunders and Com., 1996. Sullivan M.P., Yalla S.V.: Physiology of female micturation. Urol. Clin. N. Am.29:499514,2002. Vaalasti A, Hernoven A. Innervation of the ventral prostate of the rat. Am J Anat 1979; 154: 231-244. Davies MRQ. Anatomy of the nevre supply of the rectum, bladder and internal genitalia in anorectal dysgenesis in male. J Ped Surg 1997, 32(4): 536-541. Benoit G, Gillot C, Jardın A. Reflection et proposition sur la nomenclature de la prostate. Surg Radiol Anat, 1992;15:325-332. Brooks JD. Anatomy of the lower urinary tract and male genitalia . IN: Walsh PC, Retik AB, Vaughan EDJ et al. Campbell’s Urology. Philadelphia, Saunders, 1998. p. 89-128. Hervonen A, Vaalasti A, Vaalasti T, et al. Paraganglia in the urogenital tract of man. Histochemistry 1976; 46: 307-313. Benoit G, Merlaud L, Meduri G, et al. Anatomy of the prostatic nerves. Surg Radiol Anat 1994; 16: 23-29. Walsh PC, Donker PJ. Impotence following radical prostatectomy: Insight into etiology and prevention. J Urol 1982; 128: 492-497. Lepo H, Gregerman M, Crosby R et al. Precise localization of the autonomic nerves from the pelvic plexus to the corpora cavernosa: a detailed anatomical study of the adult male pelvis. J Urol 1985; 133: 207-212. Paick JS, Donatucci CF, Lue TF. Anatomy of cavernous nerves distal to prostate: Microdissection study in adult male cadavers. Urology 1993; 42(2): 145-149. Davies MRQ. Anatomy of the nevre supply of the rectum, bladder and internal genitalia in anorectal dysgenesis in male. J Ped Surg 1997, 32(4): 536-541. Lue TF, Zeıneh SJ, Schmidt RA et al. Neuroanatomy of penil erection: Its relevance to iatrogenic impotence. J Urol 1992; 131: 273-280. Breza J, Aboseif SR, Orvis BR. Detailed anatomy of penil neurovascular structures: Surgical significance. J Urol 1992; 148: 1190-1194 Whitmore WF Jr. Hormone therapy in prostatic cancer. Am J Med. 1956;21:697-713. Prout GR Jr. Diagnosis and staging of prostatic carcinoma. Cancer 1973;32:1096-1103. Jewett HJ. The present status of radical prostatectomy for stages A and B prostatic cancer. Urol Clin North Am. 1975;2:105-124. Prostate In. Sobin LH, Wittekind Ch. (Eds.). International Union Against Cancer: UICC Classification of malignant tumors, 6th. Ed. New York: Willey-Liss, 2002;184-187. Greene FL, Page D, Morrow M, Eds. Prostate In. American Joint Committee on Cancer: AJCC Cancer Staging Manuel, 6th.Ed. New York: Springer,2002;309-316. Dillioğlugil Ö, Çevik İ.:Prostat Kanserinde Tanı ve Evrelendirme. In: Üroonkoloji Kitabı. Üroonkoloji Derneği. 1st Ed. 2007:614-617. Lui, PD., Terris, MK., Mc Neal, JE., Stamey, TA.: Indications for Ultrasound Guided Transition Zone Biopsies in the Detection of Prostate Cancer. Int. J. Urol.;4(6): 567-571, 1997 - 59 - 57) 58) 59) 60) 61) 62) 63) 64) 65) 66) 67) 68) 69) 70) 71) 72) 73) 74) 75) 76) 77) 78) 79) Narayan, P. : Neoplasm of the Prostate Gland. Smith’s Urology, Tanagho, EA. Mc Aninch, JW. , 14. Edition, Connecticut-San Mateo, Lange, : 392-433 , 1995. Pienta, KJ. : Etiology, Epidemiology and Prevention of carcinoma of the Prostate. Campbell’s Urology. Walsh, PC. , Retic., Vaughan Jr, ED., Wein, AJ., Seventh Edition Vol 3; 2489-2496 , 1998. Smith JR, Freije D, Carpten JD.: Major susceptibility locus for Prostate Cancer on Cromosome 1 suggested by a genome-widee search. Science 1996; 274:1371 Carter BS, Bova GS. Beaty TH: Hereditary Prostate Cancer Epidemiologic and Clinical Features. J Urol 1993; 797-802 Bangma, CH. , Kranse, R., Blijenberg, BG.: The Value of Screening Tests in the Detection of Prostate Cancer : Part 1. Results of a Retrospective Evaluation of 1726 Men. Urology 46 : 773778 , 1995 Pentyala SN, Lee J, Hsieh K : Prostate Cancer : A Comprehensive Reviev Medical Oncology (2000) 85 – 105 Hankey BF, Feuer EJ, Clegg LX : Cancer surveillance series : interpreting trends in prostate cancer: Evidence of the effects of screening in recent prostate cancer incidence , mortality and survival rates . J Natl Cancer Inst 1999 , 1017 Landis SH, Murray T, Bolden S, Wingo PA : Cancer Statistics 1998 , CA Cancer J Clin 1998 ; 48 192 and 329 Kirby RS, Brawer MK, Denis LJ: Epidemioloji and pathophysiology , Health Press Limited, Oxford 1998, 7 Demers RY, Swanson GM, Weiss LK, Kau TY: Increasing incidence of prostate cancer . Arch Intern Med 1994; 154: 1211-1216 Brasso K, Friis S, Kjaer SK: Prostate cancer in denmark: A 50 year population- based study . Urology 1998; 51:590 Barry MJ: Prostate spesific antigen testing for early diagnosis of prostate cancer. N England J Med 2001; 344:18, 1373-1377 Greenlee RT et al.: Cancer Statistics. CA Cancer J CLIN 2001 ;51:15-36 Barry MJ, Fleming C, Caley CM ve ark.: Should medicare provide reimbursement for prostate spesific antigen testing for early detection of prostate cancer. Urology 1995; 2-13 Cooner WH, Masley BR, Rutherford CL Jr ve ark: Prostate cancer detection in a clinical urological practice by ultrasonography , digital rectal examination and prostate spesific antigen. J Urol 1990 : 143; 1146-1154 Yuan JJJ, Caplan DE , Petros JA ve ark.: Effects of rectal examination, prostatic massage, ultrasonography and needle biopsy on serum prostate spesific antigen levels. J Urol 1992 : 147 ; 810-814 Oesterling JE, Jacobsen SJ, Chute CG ve ark.: Serum Prostate Spesifik Antigen in a community based population of healthy men: Estabilishement of age spesific referance ranges . JAMA 1994 ; 271: 368-371 Epstein JI, Walsh PC, Carmichael B, Brendler CB: Pathologic and clinical findings to predict tumor extend of non palpabl prostate cancer. JAMA 1994; 271: 368-371 Sun L, Gancerzyk K, Paquette EL ve ark.: Introduction to department of Defence Center for Prostate Disease Research Multicenter National Prostate Cancer Database and analysis of changes in the PSA. Urol Oncol 2001; 6, 203 Dalton DL:Elevated serum prostate spesific entogen due to acute bacterial prostatits: Urology 1989:33,465 Carter HB,Partin AW: Diagnosis and staging of prostate cancer, ‘Campbell Urology’ 1997: 2519-2533 Özen H , Aygün C, Ergen A, Sözen S, Aki FT, Uygur MC. Combined use of prostate spesific antigen derivatives decreases the number of unnecessary biopsies to detect prostate cancer. Am J Clin Oncol 2001 ; 24(6) : 610-613 Babaian J, Johnston DA, Naccarato W ve ark.: The incidence of prostate cancer in a screening population with a serum prostate spesific antigen between 2,5 – 4,0 ng/ml: relation to biopsy strategy . J Urol 2001; 165 , 757-760 - 60 - 80) 81) 82) 83) 84) 85) 86) 87) 88) 89) 90) 91) 92) 93) 94) 95) 96) 97) 98) 99) 100) 101) 102) 103) Kwiatkowski M, Recker F, Piironen T ve ark.: In prostatism patients the ratio of human glanduler kallikrein to free PSA improves the discrimination between prostate cancer and benign hyperplasia within the diagnostic ‘gray zone’ of total PSA 4 to 10 ng/ml. Urology 1998 ; 52:360 Becker F, Kwiatkowski M, Piironen ve ark.: The importance of human glanduler kallikrein and its correlation with different prostate spesific 51 antigen serum forms in the detection of prostate carcinoma. Cancer 1998;83:2540-2547 Jung K, Elgeti U, Lein M ve ark.: Ratio of free or complexed prostate spesific antigen to total PSA : Which ratio improves differentiatiation between benign prostatic hyperplasia and prostate cancer ? Clin Chem 2000 ; 46-55 Okegawa T, Kinjo M, Watanabe K ve ark.: The significance of the free to complexed prostate spesific antigen (PSA) ratio in prostate cancer detection in patients with a PSA level of 4,1-10,0 ng/ml. BJU Int 2000 ;85 :708 Stamey TA, Yemeto C: Examination of the 3 molecular forms of serum prostate spesific antigen for distinguishing negative from positive biopsy: Relationship to transition zone volume. J Urol 2000b ;163 :119. Littrup PJ, Kane RA, Mettlin CJ ve ark.: Cost effective prostate cancer detection . Cancer 1994 ; 74 : 3146-3158 Catalona WJ, Hudson MA, Scardino PT ve ark. : Selection of optimal prostate spesifik antigen cutoffs for early detection of prostate cancer: Receiver operating characteristics. J Urol 1994a ; 152 : 2037-2042. Catalona WJ, Richie JP, De Kernion JB ve ark.: Comparison of prostate spesific antigen concentration versus prostate spesifik antigen density , in the early detection of prostate cancer : Receiver operating characteristics curves . J Urol 1994b; 152 :2031-2036. Benson MC, Whang IS, Olsson CA ve ark.: Use of prostate spesific antigen density to enhance predictive value of intermediate levels of serum prostate spesific antigen. J Urol 1992 ; 147 : 817-821. Brawer MK, Aramburu EAG, Chen GL ve ark. : the inability of prostate spesific antigen index to enhance the predictive value of prostate spesific antigen in the diagnosis of prostatic carcinoma. J Urol 1993; 150: 369-373. Lepor H, Wang B, Shapiro E: Relationship between prostatic epitelial volume and prostate spesific antigen levels. Urology 1994 ; 44 :199-205. Kalish J, Cooner WH, Graham SD: Serum PSA adjusted for volume of transition zone is more accurate than PSA adjusted for total volume of the prostate. Urology 1994 ; 43 : 601-606. Carter BH, Pearson JD , Morrell CH ve ark. : Longitudinal evaluation of in men with and without prostate disease: JAMA 1992b ; 267 :2215-2220. Christensson A, Bjork T, Nilsson O ve ark.: Serum PSA complexed to alpha 1 antichimotrypsin as an indicator of prostate cancer. J Urol 1993; 150 : 100-105. Catalona WJ, Smith DS, Wolfert RL ve ark. : Evaluation of percentage of free serum PSA to improve spesificity of prostate cancer screening. JAMA 1995; 274:1214-1220. Clements R: The Chanching role of Transrectal Ultrasound in the diagnosis of prostate cancer. Clinical Radiology 1996 ;51 :671-676. Aarnink RG, Beerlage HP, Dela Rosette, Debruyne FJM et al. : Transrektal Ultrasound of the Prostate: Innovations and Future Applications. J Urol 1998; 159:1568-1579. Littrup PJ, Kane RA, Williams CR ve ark. : Determination of prostate volume with TRUS for cancer screening: Part 1: Comparison with PSA assay. Radiology 1991; 178 : 537-542. Terris MK Vve Stamey TA: Determination of prostate volume by transrectal ultrasound. J Urol 1987 ; 145 :984. Watanabe H : Transrectal sonography : A personal review and recent advances. Scand J Urol Nephrol 1991 ; 137 : 75-78. Rifkin MD : Prostate imaging . Radiology 1987 ; 165 :200. King WW , Wilkiemeyer RM , Boyce WH , Mc Kinney WM : Current status of prostatic sonography. JAMA 1973 ; 226 : 444-447. Resnick MI , Willard JW , Boyce WHY : Recent progress in ultrasound of bladder and prostate. J Urol 1977 ; 4 : 444-446. Rifkin MD , Friedland GW , Shortliffe L : Prostatic evaluation by transrectal ultrasonography : Detection of carcinoma. Radiology 1986;158 : 85-90 - 61 - 104) Shinohara K , Scardino PT , Carter SC , Wheeler TM : Pathologic basis of the sonografic apperance of normal and malignant prostate. Urol Clin North Am 1989 ; 16 : 675-691. 105) Lee FR , Gray JM , Mcleary RD ve ark. : Prostatic evaluation by transrectal sonography : Criteria for diagnosis of early carcinoma. Radiology 1986 ; 158 : 91-95. 106) Carter HB , Hamper UM ve ark. : Evaluation of transrectal ultrasound in early detection of prostate cancer. J Urol 1989 ; 142 : 1008-1010. 107) Lange PH , Brawer MK : Prostatic acid phosphatase and PSA in the era of transrectal ultrasonography. Diagnostic ultrasound of prostate. Elsevier Science Publishing Co , 1989. 108) Hodge KK, Mc Neal SE, Stamey TA: Ultrasound guided transrectal core biopsies of the palpably abnormal prostate. J Urol 1989; 142 : 66-74. 109) Salo JO, Ranniko S, Makinen J, Lethonen T: Echogenic structure of prostatic cancer imaged on radical prostatectomy specimens.Prostate 1987;10:1-9. 110) Esposti PL, Elman A, Norlen H. Complications of transrectal biopsy of prostate. Scand J Urol Nephrol 1995; 9: 208-213. 111) Emilliozzi P, Corsetti A, Tassi B, Federico G, Martini M, Pansadoro V. Best approach for prostate cancer detection: a prospective study on transperineal versus transrectal six core prostate biopsy. Urol: 2003; 961-966. 112) Hodge KK, McNeal JE, Stamey TA: Ultrasound guided transrectal core biopsies of the palpably abnormal prostate. J Urol 1989; 142: 66-70. 113) Hodge KK, McNeal JE, Stamey TA: Random systematic versus directed ultrasound guided transrectal core biopsies of the prostate. J Urol 1989; 142: 71-75. 114) Stamey TA. Making the most out of six systemic sextant biopsies. Urology 1995; 45:2-12. 115) Gore JL, Shariat SF, Miles BJ, Kadmon D, Jiang N, Wheeler TM: Optimal combinations of systematic sextant and laterally directed biopsies for the detection of prostate cancer. J Urol 2001; 165: 1554-1559. 116) Presti JC Jr, Chang JJ, Bhargava V, Shinohara K. The optimal systematic prostate biopsy scheme should include 8 rather than 6 biopsies: results of a prospective clinical trial. J Urol 2000;163:163-166. 117) Babaian RJ, Toi A, Kamoi K, Troncoso P, Sweet J, Evans R, et al : A comparative analysis of sextant extended 11 core multisite directed biopsy strategy. J Urol 2000; 163:152-157 118) Feneley MR, Weeb JAW, Mc lean A, Kirby RS : Postoperative serial prostate spesific antigen and transrectal ultrasound for staging incidental carcinoma of the prostate. Br J Urol 1995; 75:14-20 119) Griebling TL, Williams RD : Stating of incidentally detected prostate cancer: Role of repeat resection , PSA, Needle biopsy and Imaging. Urol Oncol 1996; 14 : 156-164. 120) Lowe BA: Management of stage T1a Prostate Cancer. Urol Oncol 1996; 14 :178-182. 121) Lee, F., Torp – Petersen, ST.: Transrectal Ultrasound in the diagnosis and Stating of Prostatic Carcinoma. Radiology ; 170 : 609-615 , 1989. 122) Mansfield JT, Stephenson RA: Does Transuretral resection of the prostate compromise the radical treatment of prostate cancer. Urol Oncol 1996;14:174-177. 123) McNeal JE, Bostwick DG, Kindrachuk RA, et al. Patterns of progression in prostate cancer. Lancet 1986;1 (8472):60-3. 124) Epstein JI, Carmichael M, Partin AW, Walsh PC.:Is tumor volume an independent predictor of progression following radical prostatectomy? A multivariate analyses of 185 clinical stage B adenocarcinomas of the prostate with 5 years of followup. J Urol. 1993;149(6):1478-81. 125) Zietman AL, Edelstein RA, Joen JJ, et al. Radical prostatectomy for adenocarcinoma of the prostate: the influance of preoperative and pathologic findings on biochemical disease-free outcome. Urology 1994;43 (6) 828-33. 126) Harnden P, Shelley MD: The prognostic significance of perineural invasion in prostatic cancer biopsies: a systematic review. : Cancer. 2007 Jan 1;109(1):13-24. 127) Bastacky SI, Walsh PC, Epstein JI: Relationship between perineural tumor invasion on needle biopsy and radical prostatectomy capsular penetration in clinical stage B adenocarcinoma of the prostate. Am J Surg Pathol. 1993 Apr;17(4):336-41. 128) Cannon GM Jr, Pound CR: Perineural invasion in prostate cancer biopsies is not associated with higher rates of positive surgical margins. Prostate. 2005 Jun 1;63(4):336-40. - 62 - 129) Ali TZ, Epstein JI: Perineural involvement by benign prostatic glands on needle biopsy. Am J Surg Pathol. 2005 Sep;29(9):1159-63. 130) Merrick GS, Butler WM: Prognostic significance of perineural invasion on biochemical progression-free survival after prostate brachytherapy. : Urology. 2005 Nov;66(5):1048-53. 131) Beard C, Schultz D: Perineural invasion associated with increased cancer-specific mortality after external beam radiation therapy for men with low- and intermediate-risk prostate cancer. Int J Radiat Oncol Biol Phys. 2006 Oct 1;66(2):403-7. Epub 2006 Jun 9. 132) Lee IH, Roberts R: Perineural invasion is a marker for pathologically advanced disease in localized prostate cancer. Int J Radiat Oncol Biol Phys. 2007 Jul 15;68(4):1059-64. Epub 2007 Mar 29. 133) Passavanti G, Pizzuti V: Perineural invasion in prostatic carcinoma treated with radical prostatectomy: the role of TR systematic biopsy. Arch Ital Urol Androl. 2007 Mar;79(1):23-5. 134) Yu HH, Song DY: Perineural invasion affects biochemical recurrence-free survival in patients with prostate cancer treated with definitive external beam radiotherapy. Urology. 2007 Jul;70(1):111-6. 135) Bismar TA, Lewis JS Jr: Multiple measures of carcinoma extent versus perineural invasion in prostate needle biopsy tissue in prediction of pathologic stage in a screening population. Am J Surg Pathol. 2003 Apr;27(4):432-40. 136) Epstein JI: The role of perineural invasion and other biopsy characteristics as prognostic markers for localized prostate cancer. Semin Urol Oncol. 1998 Aug;16(3):124-8. 137) Stone NN, Stock RG, Parikh D, et al: Perineural Invasion and Seminal Vesicle Involvement Predict Pelvic Lymph Node Metastasis in Men With Localized Carcinoma of the Prostate. Stone NN, Stock RG, Parikh D, et al. J Urol. 1998;160:1722-1726. 138) Eskew L, Bare RL, McCullough DL : Systemic 5 region prostate biopsy is superior to sextant method for diagnosing carcinoma of the prostate. J Urol 1997; 157: 199-203 139) De la Taille A, Antiphon P, Salomon L, Cherfan M, Porcher R, Hoznek A, et al. Prospective evaluation of a 21- sample needle biopsy procedure designed to improve the prostate cancer detection rate. Urology 2003; 61: 1181-1186 140) Stewart CS, Leibovich BC, Weaver AL, and Lieber MM. Prostate cancer diagnosis using saturation needle biopsy technique after previous negative sextant biopsies. J Urol 2001; 166: 86-92 141) Morote J, Lopez M, Encabo G, de Torres I. Value of routine transition zone biopsies in patients undergoing ultrasound-guided sextant biopsies for the first time. Eur Urol 1999; 35: 294-297 142) Terris MK, Pham TQ, Issa MM, Kabalin JN. Routine transition zone and seminal vesicle biopsies in all patients undergoing transrectal ultrasound guided prostate biopsies are not indicated. J Urol. 1997; 157 :204-206. - 63 -