T.C. SAĞLIK BAKANLIĞI
KARTAL KOġUYOLU YÜKSEK ĠHTĠSAS EĞĠTĠM VE ARAġTIRMA
HASTANESĠ
KOġUYOLU KALP MERKEZĠ
KARDĠYOLOJĠ KLĠNĠĞĠ
KALICI KALP PĠLĠ UYGULANMIġ HASTALARDA ARTAN KALP
HIZLARI ĠLE DĠSSENKRONĠDEKĠ DEĞĠġĠMĠN DOKU
SENKRONĠZASYON GÖRÜNTÜLEME VE TĠSSUE TRACKĠNG ĠLE
DEĞERLENDĠRĠLMESĠ VE BUNUN SOL VENTRĠKÜL HEMODĠNAMĠK
PARAMETRELERLE ĠLĠġKĠSĠ
Dr.Taylan AKGÜN
UZMANLIK TEZĠ
ĠSTANBUL
2007
TEZ DANIġMANI: Doç.Dr.Cihangir KAYMAZ
1
ĠÇĠNDEKĠLER
1-ÖZET
2
2-GĠRĠġ VE AMAÇ
5
3-PACEMAKER GENEL ÖZELLĠKLERĠ
6
Tanımlamalar
Pacemaker modları
Tek odacıklı pacemakerlar
Ġki odacıklı pacemakerlar
4-ASENKRON PACĠNG
12
5-FĠZYOLOJĠK PACE ĠġLEMĠ
13
6-SAĞ VENTRĠKÜL UYARIMININ OLUMSUZ SONUÇLARI
14
7-ALTERNATĠF BÖLGELERDEN VENTRĠKÜLER PACĠNG
20
Sağ ventrikül çıkımyolu pacingi
His demeti, sağ ventriküler septal pacing yada bifokal sağ ventriküler pacing
Biventriküler yada sol ventrikül pacingi
Triventriküler pacing
8-NORMAL MĠYOKARDĠYAL ELEKTRĠKSEL ĠLETĠM
29
9- ANORMAL MĠYOKARDĠYAL ELEKTRĠKSEL ĠLETĠM
29
10-MĠYOKARDĠYAL DĠSSENKRONĠNĠN DEĞERLENDĠRME
32
YÖNTEMLERĠ
M-MOD ĠNCELEME
DOKU DOPPLER GÖRÜNTÜLEME
TĠSSUE TRACKING
STRAIN VE STRAIN RATE
SPECKLE TRACKING
DOKU SENRONĠZASYON GÖRÜNTÜLEMESĠ (TISSUE
SYNCHRONISATION IMAGING)
11-EGZERSĠZLE DĠSSENKRONĠ DEĞĠġĠMĠ
41
12-ÇALIġMA
42
MATERYAL VE METOD
BULGULAR
TARTIġMA
13-KAYNAKLAR
57
2
ÖZET
Amaç:
Kalıcı kalp pili takılmıĢ hastalarda artan kalp hızları ile birlikte intravenriküler
dissenkroninin değiĢimini ve bunun sol ventrikül hemodinamik parametrelerle
iliĢkisini incelemek
Materyal ve metod:
ÇalıĢmaya pacemaker implantasyonu yapılmıĢ 24 hasta dahil edildi( erkek:11
kadın:13). Sol ventrikül volümleri, ejeksiyon fraksiyonu ve kardiyak output ölçümü
apikal 4 boĢluk ve 2 boĢluk görüntülerden biplane simpson yöntemi ile yapıldı.
Doku senkronizasyon görüntüleme(TSI) ve tissue tracking (TT) ölçümleri için
EchoPAC‘e kaydedilen TVI dataları kullanıldı. TSI ile Septal-lateral gecikme,
septal-posterior gecikme, bazal segmentler arası maksimum gecikme, bazal
segmentler arası standart sapma, tüm segmentler arası maksimum gecikme ve tüm
segmentler arası standart sapma değerleri ölçüldü. TT ile yapılan değerlendirme
sonucunda 6 bazal ve 6 mid segmente örneklem yerleĢtirilerek QRS baĢından
miyokardiyal pik sistolik yer değiĢime(displacement) kadar geçen zaman ölçüldü
ve elde edilen değerlerin standart sapması alındı.
Hastaların bazal görüntüleri kaydedildikten sonra kalp hızı 20 vuru/dk periyodlarla
artırıldı. Her periyodda 10 dakikalık bekleme süresinden sonra ölçümler tekrarlandı
ve bir sonraki kalp hızına geçildi. Maksimum hız hastanın toleransına göre
belirlendi.
Bulgular:
Tissue tracking ile yapılan değerlendirmede hastaların %48‘inde artan pacemaker
hızları ile asenkroni değerleri azalmıĢ,%8 hastada değiĢmemiĢ, %44 hastada ise
artıĢ göstermiĢtir. TSI ile değerlendirildiğinde, kullanılan yöntemlere göre farklılık
göstermekle birlikte hastaların %52-65‘inde dissenkronide azalma, %0-34 ünde
değiĢmeme, %10-35‘inde artma izleniyordu. Ayrıca bir hastada tüm TSI yöntemleri
ile aynı yönde değiĢim yalnızca %34 hastada izlendi. Geri kalan hastalarda bazı TSI
kaynaklı yöntemlerle dissenkroni artarken, bazılarıyla azalma yada değiĢmeme
izlenmekteydi.
3
Artan hızlarla birlikte sol ventrikül ejeksiyon fraksiyonunun değiĢmediği, sol
ventrikül diyastol sonu çap (p:0,031), diyastol (p:0,001) ve sistol sonu
volüm(p:0,05) ile aortik hız zaman integralinin(p:0,001) anlamlı ölçüde azaldığı,
kardiyak outputun ise anlamlı ölçüde arttığı(p:0,001) saptanmıĢtır. Ancak sol
ventrikül ejeksiyon fraksiyonu normal yada azalmıĢ olan gruplar arasında, ya da sol
ventrikül dissenkronisi artan yada azalan gruplar arasında bu bahsedilen
parametreler de anlamlı bir fark izlenmemiĢtir.
Sonuç:
Sağ ventrikül apikal pacing uygulanmıĢ olan hastalarda artan pacemaker hızları ile
birlikte
bazı
hastalarda
dissenkroni
değerleri
artarken,
bazı
hastalarda
değiĢmemekte bazı hastalarda ise tam tersine azalmaktadır. Bunun yanında , doku
senkronizasyon görüntüleme ile yapılan incelemede, aynı hastada farklı
parametrelere
göre
dissenkronide
artma,
azalma
yada
değişmeme
görülebilmektedir. Sol ventrikül volümleri, ejeksiyon fraksiyonu, aortik hız zaman
integrali ve kardiyak output, sol ventrikül ejeksiyon fraksiyonu düĢük veya normal
olan gruplarda yada dissenkronisi artan yada azalan gruplar arasında benzer değişim
göstermektedir.
4
GĠRĠġ VE AMAÇ
Ventriküllerin normal aktivasyonu, elektriksel impulsun atriyoventriküler
noddan his demetine iletimi ile baĢlar. Daha sonra his demeti sağ ve sol ana dallara
ayrılır ve bu dallar birkaç major fasikül vererek, subendokardiyal bölgede lokalize
purkinje lifleri ağı halinde sonlanırlar.Purkinje lifleri içerisindeki impuls iletimi
bazalden apikale doğrudur ve çok hızlı gerçekleĢir (3-4 m/sn) (17-20). Bu hız
normal miyokard dokusu içerisindeki iletime kıyasla dört kat daha hızlıdır.
Ġmpulslar purkinje sistemini sağ ventrikülün alt ¼ ‗ünde , sol ventrikülü ise
alt 1/3 ‗ ünde terkeder( 17). Bu nedenle interventriküler septumda aktivasyon
apeksden bazale doğru meydana gelir(23-25). Sağ ve sol ventrikülde de aktivasyon
apeksden bazale ve endokarddan epikarda doğru olur( 23,26,27).
Pacemaker ile bradikardik epizodların önlenmesinde önemli terapötik
faydalar elde edilirken, ventriküllerin farklı bir yoldan uyarılması ve kardiak
sistemi oluĢturan yapıların birbirinden farklı elektrofizyolojik özellikleri nedeni ile
fizyolojik olmayan bir impuls iletimi meydana gelir. Bu anormal aktivasyon paterni
sol ventrikülde homojen olmayan bir kontraksiyona, miyokard perfüzyon
defektlerine, sempatik aktivitede artmaya, fibrosise ve netice olarak yeniden
Ģekillenmeye neden olur. Sağ ventrikül pacinginin orta ve uzun dönem etkilerini
araĢtıran çalıĢmalarda ejeksiyon fraksiyonunda ve diğer sol ventrikül fonksiyon
belirteçlerinde değiĢimler gösterilmiĢtir. Bu değiĢimler temel olarak ventriküllerin
anormal yoldan uyarılması sonucu oluĢan interventriküler ve intraventriküler
asenkroniye bağlanmıĢlardır. Asenkroni nedeni ile miyokardiyal duvarlardaki
eĢzamanlı olmayan kontraksiyon ventrikülde volüm hapsine ve basıncın yeterince
yükselememesine, miyokardiyal kontraksiyonun boĢa harcanmasına yol açarak
global ventrikül fonksiyonu üzerinde olumsuz etkilere neden olmuĢtur. Özellikle
sağ ventrikülün apikal pacinginin miyokardın farklı segmentlerinde farklı önyüke
yolaçtığı ve pace edilen segmentde, pace edilen yerin uzağındaki segmente kıyasla
daha düĢük straine, daha düĢük oksijen ve glikoz kullanımına ve netice olarak daha
zayıf bir kontraksiyona neden olduğu saptanmıĢtır. Hatta erken aktive olan
bölgelerin kalınlığında zamanla azalma meydana geldiği buna karĢın geç aktive
olan bölgelerde miyokardiyal hipertrofi geliĢtiği izlenmiĢtir.
5
Ayrıca son zamanlarda sol ventrikül sistolik disfonksiyonu olan hastalarda
bazal intraventriküler asenkroninin egzersiz
ile birlikte nasıl değiĢtiğini
değerlendiren çalıĢmalar yapılmıĢtır. Ennezat ve arkadaĢlarının yaptığı bir
çalıĢmada egzersizle sol ventrikül asenkronisi bazı hastalarda artarken bazılarında
değiĢmemekte veya tam tersine azalmaktadır. Lafitte ve arkadaĢları tarafından
yapılan bir baĢka çalıĢmada da benzer bulgular izlenmiĢtir.
Bu çalıĢmada sağ ventrikül apikal pacingi yapılan hastalarda bazal
ventriküler dissenkronin artan pacemaker hızları ile değiĢimi, bu değiĢimi
değerlendirmede
doku
senkronizasyon
görüntüleme
ve
tissue
tracking
yöntemlerinin kullanımı ve değiĢimin sol ventrikül hemodinamik göstergeleri ( sol
ventrikül diyastol ve sistol sonu çap ve volümleri, kardiyak output, % ejeksiyon
fraksiyonu, % fraksiyonel kısalma), aortik hız zaman integrali üzerine etkisi
araĢtırıldı.
PACEMAKERLARIN GENEL ÖZELLĠKLERĠ
Tanımlamalar:
Pacemaker
sistemleri
geliĢtikçe
kuzey
amerika
pacing
ve
elektrofizyoloji grubu(NASPE) ile ingiliz pacing ve elektrofizyoloji birliği
(BPEG) , pacemaker fonksiyonlarını tarif etmek için beĢ kodlu bir sistem
geliĢtirmiĢlerdir(1).
Bu beĢ kodlu sistemde birinci kod pace edilen odacığı( atriyum (A),
ventrikül(V), her ikisi( D), yada hiçbiri ( O ) belirtir. Ġkinci kod pacemakerin
kardiyak elektriksel aktiviteyi sense ettiği yeri (A,V,D,O) belirtir. Üçüncü kod
pacemakerın sensinge cevabını kodlar. Tetiklenme (T), inhibisyon (I) , her
ikisi (D), yada hiçbiri (O). Eski sistemlerde temel olarak bu üç özellik
bulunur ve pacemakerlar genel olarak bu üç kod ile ifade edilirler. Dördüncü
kod
pacemakerın
hızını
bazı
sensörler
aracılığıyla
adapte
edebilmesini
gösterir. Bu koddaki R harfi adaptiv hız yanıtını ifade eder.Yani hastanın
kalp hızı hastanın aktivitesine göre değiĢir. ― O‖ ise hız modulasyonu
özelliğinin olmadığını gösterir. Pratik olarak bu pozisyonda sadece R kodu
6
kullanılır. ― O‖ kullanılmaz.(DDD ile DDDO aynıdır.) BeĢinci kod ise
pacemakerdaki antitaĢidisritmi özelliğini ifade eder. ( antitaĢidisritmi pacing(P)
yada antitaĢidisritmi schoking(S) ). Fakat bu kod bu özelliğin nasıl aktive
edildiğini belirtmez.
Örneğin VVIPP, pacemakerin ventrikülü uyardığını,ventrikülü sense
ettiğini,
algılanan
programlanabilir
ventiküler
olduğunu
ve
aktivite
oluğunda
antitaĢidisritmi
pacing
inhibe
edildiğini,
özelliğinin
mevcut
olduğunu ifade eder. VVIMD , ilk üç özellik yukarıdakiyle benzer olmak
üzere , pacemakerın programlanabilir olduğunu ve bir taĢidisritmi durumunda
pacing ve schoking özelliğinin olduğunu ifade eder.VOOOO sadece asenkron
ventriküler pacing özelliğinin olduğunu ifade eder.
Bu kadar değiĢik çeĢit olmasına rağmen klinik kullanımda en
yaygın olarak AAIR, VVIR, DDD, DDDR ve backup pace özelliği bulunan
cardioverter defibrilatörler kullanılır. Bu temel pacing modlarına ilaveten
,modern
pacemakerlarda
çeĢitli
klinik
durumlarda
pacemakerların
performansını artırmak için ek özellikler bulunur.Otomotik mod değiĢimi ve
adaptiv hız cevabı bir çok modern pacemakerda bulunur.
Otomotik mod değişimi:
Ġki odacıklı pacemaker sistemlerinde ( DDD/DDDR ve daha az
sıklıkla VDD/VDDR ), ventrikül sense edilen her atriyal vurunun ardından,
programlanan maksimum hız limitine kadar, ventrikül pace edilir.Paroksismal
atriyal taĢikardi durumunda ,taĢikardi süresince, ventrikül maksimum limitte
uyarılacak ve istenmeyen bir durum meydana gelecektir. Mod değiĢimi
özelliği bu durumlarda pacemakerın otomotik olarak yeniden programlanması
ve intrinsik atriyal hızı takip etmemesini sağlar.Pacemaker otomotik olarak
VVI yada VVIR özelliğine geçer. Sens edilen atriyal hız mod değiĢim
limitinin altına indiğinde ve fizyolojik ritm tekrar algılandığında, pacemaker
tekrar programlandığı bazal moda döner.
7
Adaptiv hız cevabı:
Bu özellik , pacemakerın programlanmıĢ hızının hastanın fiziksel
aktivitesine göre değiĢimini ifade eder.Pacemakerın, hastanın fiziksel olarak
aktif olduğunu saptaması için çeĢitli sensörler geliĢtirilmiĢtir. (vibrasyon,
dakika ventilasyon, oksijen saturasyonu vb).
Hız düşmesi (rate drop):
Hız düĢmesi
özelliği,
nörokardiyojenik
senkop
tedavisi
için
geliĢtirilmiĢtir.Hastanın kalp hızı hızlı bir Ģekilde belirlenen limitin altına
düĢerse, pacemaker tetiklenir ve hızlı bir Ģekilde birkaç dakika boyunca
ventrikülü
uyarır.
Nörokardiyojenik
senkop
genelde
bradikardik
ve
vazodepresör komponentten oluĢtuğu için, pacemaker bu Ģekilde geçici hız
artmasıyla kardiyak outputu arttırır.
Managed ventriküler pacing:
Sağ ventrikül uyarımı, sağ ventrikülün sol ventrikül lateral duvarından
önce kontraksiyonuna neden olarak sol dal bloğunun etkilerini taklid eder. Bu
fenomen
ventriküler
dissenkroni
yada
asenkroni
olarak
adlandırılır.
Dissenkroni kalp yetersizliğine yada varolan kalp yetersizliğinin alevlenmesine
neden olabilir. Bu nedenle pacemakerı olan hastalarda , sağ ventrikül
uyarımını minimuma indirmek için bazı modlar geliĢtirilmiĢtir. Ġki odacıklı
pacemaker AAI modunda programlanır, AV iletimin kaybolduğu saptanırsa
pacemaker bir süre için tekrar DDD moduna geçer. AV iletimin tekrar
saptandığı zamanda da yeniden AAI moduna geçiĢ olur. 181 hastanın dahil
edildiği ―managed ventriküler pacing‖ özelliği bulunan iki odacıklı ICD
hastalarında, konvansiyonel DDD pacemakerlı hastalara kıyasla ventrikülün
direkt olarak uyarım yüzdesi 74‘den 4‘e düĢmüĢtür.
8
PACĠNG MODLARI:
Ġdeal pace modunu seçmek için, hastanın genel fiziksel durumu,
iliĢkili tıbbi sorunları, egzersiz kapasitesi ve egzersize kronotropik yanıtı karar
vermede önemlidir.
Tek odacıklı pacemakerlar:
Eski tip pacemakerlar sadece tek bir kalp odacığını sense yada pace
etmek için tasarlanmıĢlardır. Ventrikül uyarımı, ventriküler bradikardi ve
asistolleri önlerken, atriyal pacing izole olarak sinus nod disfonksiyonu yada
AV iletimin sağlam olduğu hasta sinus sendromlarında kullanılır.
VVI yada VVIR: halen en çok kullanılan pace modudur. Ventrikül
pace
ve
sense
edilir,
ventrikül
sense
edilen
vuru
nedeni
ile
inhibe
olur.Avantajı sadece tek bir lead gerektirmesidir. Buna karĢın AV senkroninin
devam ettirilememesi dezavantajıdır. VVIR genelde yavaĢ ventrikül cevaplı
atriyal fibrilasyonlarda endikedir. Eğer sinus nod fonksiyonu intakt ise, iki
odacıklı pacemaker AV senkroniyi sağlamasından dolayı tercih edilmelidir.
AAI yada AAIR: Atriyum pace edilir, atriyum sense edilir ve sense
edilen atriyal vuru sonrası pacemaker inhibe olur. Bu pacemaker modu sinus
nod disfonksiyonu olan ve AV nod fonksiyonları normal olan hastalarda
idealdir. Semptomatik sinus bradikardisi yada sinusal duraklaması olan ancak
egzersizle
kalp
hızı
artabilen
hastalarda
pacemaker
AAI
modunda
prgramlanmalıdır. Egzersize kalp hızı yanıtı yetersiz ise adaptiv hız cevabı(R)
özelliği olmalıdır.
VVI pacemakerlarda olduğu gibi yine tek lead yeterlidir. Fakat VVI
ların
tersine,
bradiaritmilerden
hastaları
AV
korumazlar.Bu
iletim
nedenle
bozulmasına
AAI
bağlı
ventriküler
pacemakerlar
sıklıkla
kullanılmazlar. Birçok klinisyen sinus nod disfonksiyonu olan hastalarda bir
süre sonra AV nod disfonksiyonunun da geliĢeceğine inanır. Bu hastalarda
atriyoventriküler
iletim
sistemi
hastalığı
yavaĢ
geliĢeceği
için
AAI
pacemakerlar iki odacıklı pacemakerlara yükseltilebilir ancak bu iĢlem iki
odacıklı pacemakerın takılmasından daha zordur.
9
Hayes ve arkadaĢlarının yaptığı bir çalıĢmada , 1967 den 1982 ye
kadar takılan tek odacıklı atriyal pacemaker vakalarının (ortalama takip süresi
33 ay) yalnızca 2 sinde (toplam 70 hasta) atriyoventriküler blok geliĢmiĢtir.
AAI pacemaker takılırken artan atrial pacing hızlarında ventriküler iletim
değerlendirilmeli ve ortalama 120-140 vuru/dk hızında 1:1 AV iletimin
korunuduğu
görülmelidir.
Ayrıca kronotropik
yetersizliği olan hastalarda
AAIR modu seçilmelidir.
İki odacıklı pacemakerlar:
DDD yada DDDR: Ġki odacıklı pacemaker sistemleri atriyum ve
ventrikülün her ikisini de sense ve pace edebildiklerinden fizyolojik pacing
özelliği sağlarlar. Sinus ritmi ve normal AV iletim varlığında, sinus hızı
programlanan en düĢük pace hızından fazla ise ve intrinsik AV iletim de
programlanan AV iletimden daha hızlı ise pacemaker total olarak inhibe
olabilir. Sinus bradikardisi ve normal AV iletim varlığında, AV interval
programlanan AV iletim süresinden hızlı ise, atriyal pacemaker vurusu ve
devamında
intrinsik
ventriküler
vuru
gelecektir.
Sinus
bradikardisi
ve
gecikmiĢ yada tamamen kaybolmuĢ AV iletim varlığında hem atriyum hemde
ventrikül pace edilir. Normal sinus ritmi ve gecikmiĢ yada kaybolmuĢ AV
ileti varsa Ventrikül atriyumla senkron bir Ģekilde uyarılır.Sonuç olarak,
norml fonksiyone eden bir DDD pacemakerda dört farklı ritm çeĢidi
görülebilir.
Normal sinus ritmi
Atriyal pacing, ventriküle normal iletim ve normal intrinsik QRS
dalgası
Atriyum ve ventrikülün ardıĢık pacingi
Atrial sensing ve ventriküler pacing
DDD modu normal sinus ritmi olan AV bloklu hastalar için
endikedir.Ayrıca DDD, bazı yazarlar tarafından kardiyoinhibitör komponentli
karotid sinus hipersensitivitesinde de endike olarak kabul edilir
10
DDDR modu için ideal hasta grubu ise sinus nod disfonksiyonu ile
beraber AV nodal disfonksiyonu olan hastalardır.Bu hastalarda AV senkroni
ve aynı zamanda adaptiv hız cevabı özelliği sağlanır . DDDR modu aynı
zamanda sinus nod disfonksiyonu ve normal AV iletimi olan hastalardada
kullanılır. Bunun nedeni AAIR pacing moduna, daha önce de belirtildiği gibi,
zamanla geliĢecek olan AV iletim hastalığı nedeni ile güvenilmemesidir.
DDI modu: bu moddaki pacemakerlar ,atriyal ve ventriküler sensing
ve
pacing
özelliğine
göre
aktiviteye
sahiptir.
ventrikülü
Buna karĢın
pace
etmez.
pacemaker
Herhangi
bir
intrinsik
atriyal
atriyal
aktivite
durumunda, pacemakerın atriyal ve ventriküler outputu susar
uyarının
ventriküle
iletimine
izin
verir.
AV
blok
meydana
ve nativ
gelirse,
programlanan hızda ventriküler vuru meydana gelir. Örneğin pace DDI
modunda ve bazal hız 50 vuru/dk ya programlı , hasta sinus ritminde, kalp
hızı 60 ve 1:1 iletim varsa pacemaker tamamıyla inhibe olur. AV blok
geliĢirse , pacemaker programlanan hızda yani 50 vuru/dk hızında ventrikülü
pace eder.Eğer sinus bradikardisi geliĢirse , pacemaker hem atriyumu hemde
ventrikülü 50 vuru/dk hızında ardıĢık olarak pace eder.
DDI modunun avantajı, bu pacemaker modunun atriyal uyarıları
―track‖ edememesi nedeni ile atriyal taĢiaritmi durumlarında ventrikülü
istenmeyen yüksek hızlardan korumasıdır. Ancak ―otomotik mod değiĢimi‖
özelliği bulunan pacemakerlar nedeni ile DDI modunun bu avantajı ortadan
kalkmıĢtır.
Daha nadir modlar:
VDD ve DVI modları hala birçok pacemakerda vardır ancak sıklıkla
kullanılmaz.
VDD modu— VDD modu normal sinus nodu fonksiyonlu Av nod
iletim sistemi hastalıklarında tercih edilebilir.iki leadli VDD pacemaker
sistemleri artık yerini DDD pacemakerlara bırakmıĢtır. Buna karĢın tek leadli
VDD pacemakerlar hala kullanımdadır ve ana endikasyonunu normal sinus
nod fonksiyonlu AV bloklu hastalar
teĢkil etmektedir.Bu sistemlerde atrial
11
sensing ventriküler leadin atrium içerisindeki kısmında bulunan sensörler
aracılığıyla sağlanmaktadır.
Tek leadli VDD pacemakerların bir dezavantajı, baĢlangıçta normal
sinus nod fonksiyonlu hastalarda sinus nod disfonksiyonu geliĢmesidir. Bu
durum daha sonraları AV senkroniyi ve cronotropik kompetansı sağlamak için
ek bir atriyal lead yerleĢtirilmesini gerektirir. Fakat bu sık karĢılaĢılan bir
durum değildir.
DVI pacemakerlar (atriyum ve ventrikül pace edilir, ventrikül sense
edilir ve sense edilen ventriküler atımlarda pacemaker inhibe olur) bir dönem
sık kullanılmıĢlardır. Ancak, atriyal vuruları sense edememesi kronotropik
yanıtı
eterli
olan
hastalarda
hız
adaptiv
yanıtı
(R)
özelliğinin
kulanılamamasına neden olur. Ayrıca atrial sensing olmaması gereksiz atriyal
pacinge neden olur ve istenmeyen atriyal ritm sorunları meydana gelir. Bu
nedenlerden dolayı artık DVI modu nadiren kullanılmaktadır.
ASENKRON PACING:
Asenkron
pacemakerlar
herhangi
bir
odacığı
sense
etmeden,
programlanmıĢ sabit bir hızda uyarı çıkarırlar.
AOO, VOO, yada DOO mod — Bu üç modda pacemaker atriyumu,
ventrikülü
yada
heriki
odacığı
birden
herhangi
bir
sense
fonksiyonu
olmaksızın belirlenen hızda pace ederler.
Asenkron pacemakerlar artık çok nadiren kullanılırlar. Bu mod,
pacemaker bağımlı hastalarda geçici olarak
cerrahi giriĢim uygulanırken
kullanılırlar. Nedeni de, elektrokoter uygulanımı esnasında pacemakerların
bunu yanlıĢlıkla intrinsik kardiyak aktivite zannetmesi ve outputlarını inhibe
etmesindendir. Bu ise pacemaker bağımlı hastalarda ciddi bradiaritmi ve
asistollere
neden
olabilmektedir.
Bundan
dolayı,
cerrahi
öncesinde
pacemakerların sensing özelliği kapatılmalı ve asenkron moda alınmalıdır.
Asenkron modda pace iĢlemi,
hastanın nativ kardiyak atımları ile
pacemaker arasında yarıĢmaya neden olabilir ve pace uyarısı nativ T dalgası
gibi karasız bir bölgeye gelerek ciddi ventriküler aritmilerin oluĢmasına neden
12
olabilir. Bu riski düĢürmek için pacemakerın hızı görece yüksek bir değerde
tutulmalı( örn: 80 vuru/dk)
ve cerrahi iĢlem sonrası yenide bazal duruma
uygun programlanmalıdır.
FĠZYOLOJĠK PACE ĠġLEMĠ:
―Fizyolojik pacing‖ tabiri, normal kardiyak uyarı mekanizmasını en
iyi taklid eden anlamında kullanılır ve genelde AV senkroniyi koruyan (AAI
veya DDD) ve aynı zamanda adaptiv hız cevabı(R) olan sistemleri anlatır.
Avantajları:
Fizyolojik
pacingin VVI
moduna kıyasla
çok
pek
hemodinamik ve klinik vantajları vardır. Bunlar:
Atriyal
fibrilasyonun
oluĢumunda
azalma:
atriyal
taĢiaritmiler
ve
özellikler atriyal fibrilasyon sıklığı VVI moduna kıyasla azalır.Bunun birkaç
potansiyel nedeni, AV senkroninin korunması ve bu Ģekilde atriyal elektriksel
ve mekanik yeniden Ģekillenmenin önlenmesi,atriyal refraktörlük sürelerindeki
farklılıkların ve atriyal erken vuruların azalmasıdır.
Tromboembolik olay sıklığında azalma: AF insidansındaki azalmaya
paralel olarak tromboembolik olay insidansınında azaldığı düĢünülür.
AV senkroninin devamı ve ―atriyal kick‖ kardiyak outputta, arteriyel
basınçta ve koroner kan akımında artmaya neden olur
Bu artmanın miktarı ve klinik önemi düĢüktür ancak nielsen ve
arkadaĢlarının
yaptığı
bir
çalıĢmada
fizyolojik
pacing
iĢleminin
kalp
yetmezliği insidansını azalttığı saptanmıĢtır.
Pacemaker sendromunun önlenmesi: VVI modu ,
olmamasından
kaynaklanan
―pacemaker
sendromu‖
için
AV senkronin
risk
teĢkil
eder.Fizyolojik pacing ile bu önlenir.
13
SAĞ VENTRĠKÜL PACĠNGĠNĠN OLUMSUZ SONUÇLARI
Sağ ventrikül pacinginin sol ventrikül fonksiyonları üzerinde yarattığı olumsuz
etkiler yeni değildir.1920 li yıllarda Carl Wiggers, atriyal pacinge kıyasla
ventriküler pacingin kardiyak fonksiyonlarda bir azalmaya neden olduğunu
saptamıĢtır ve bunu sofistike bazı basınç-volüm iliĢkilerini gösteren deneysel
çalıĢmalarla desteklemiĢtir. Fakat bunlara rağmen , intravenöz yolla sağ
ventrikül apikal lead yerleĢtirilmesinin, epikardiyal leade göre relatif olarak
kolay olması ve daha stabil olması nedeniyle pacemaker sistemleri bu Ģekilde
geliĢmiĢtir.
Son
on
yılda
yapılan
bazı
çalıĢmalar
intraventriküler
ileti
gecikmesinin ve özellikle sol dal bloğunun yarattığı olumsuz sonuçları
göstermek açısından faydalı olmuĢtur(2-11). Sol dal bloğu varlığı ventriküler
dissenkroniye neden olmakta ve buna bağlı olarak geliĢen strok volüm ve
kardiyak atımdaki azalma hemodinamik bozulmayı meydana getirmektedir.Bu
durum özellikle sol ventrikül disfonksiyonu olan hastalarda klinik kötüleĢmeye
neden olmaktadır. Konjestif kalp yetersizliği olan hastaların %20 veya 30
ununda ventriküler dissenkroni bulunduğu(2,10) ve bu hastaların özellikle
QRS süresi 120 ms den büyük ve LBBB li hastalar olduğu bilinmektedir.
Sağ ventrikül apikal pacinginin olumsuz etkileri
Ġatrojenik olarak yapılmıĢ intraventriküler ileti
gecikmesi
sol ventriküler elektriksel ve mekanik dissenkroni
sol ventrikül yeniden Ģekilenmesi
miyokardial histopatolojide anormallik
sol ventrikül sistolik disfonksiyonu( sistolik ve diastolik)
konjestif kalp yetmezliği
miyokardial perfüzyon defektleri ve bölgesel duvar hareket
anormallikleri
fonksiyonel mitral yetersizlik
14
artmıĢ atriyal fibrilasyon riski( sinus nod disfonksiyonu ve
normal baseline QRS süresi varlığında)
sol atriyal geniĢleme
ventriküler aritmilerin tetiklenmesi
Sempatik sinir sitemi aktivasyonu
Kardiyak resenkronizasyon tedavisi( biventriküler yada sol ventrikül
pacing teknikleriyle uygulanan) son yıllarda tıbbi tedaviye dirençli orta ve
ileri kalp yetersizliği olan hastalarda uygulanmaktadır(12-22). Son yapılan bir
metaanalizde ve iki büyük çalıĢmada bu tedavinin, özellikle defibrilasyon
desteğiyle kullanıldığında hayat süresini uzattığı gösterilmiĢtir(23-26).
Aynen spontan sol dal bloğunda olduğu gibi sağ ventrikül uyarımı
sonucunda oluĢan sol dal bloğu da zararlı etki gösterir(27-33). Bu yüzden
tüm
vakalarda
olmasada
bazı
vakalarda
standart
sağ
ventrikül
apeks
uyarımının yeniden değerlendirilmesi ve sorgulanması gerekmektedir.
SAĞ VENTRĠKÜL APĠKAL UYARIMI
KLĠNĠK ÇALIġMALAR
Tantengco ve arkadaĢlarının yaptığı bir çalıĢmada sağ ventriküler apeks
bölgesinden pacingin
uzun dönem etkileri araĢtırılmıĢtır. Bu çalıĢmaya
konvansiyonel yöntemle kalıcı
ortalama
yaĢ:
19,5
yıl)
pace takılmıĢ 24 genç hasta dahil edilmiĢ(
ve
hastalar
ortalama
9,5
yıl
takip
edilmiĢlerdir.Ortalama sağ ventrikül uyarımı süresi 0,7 yıldan 18,9 yıla kadar
değiĢmekteydi. Bu çalıĢmada sağ ventriküler pacinging uzun dönemde geri
dönüĢümsüz sol ventrikül disfonksiyonuna neden olduğu gösterilmiĢtir(29). 33
sağlıklı kontrol hastasıyla karĢılaĢtırıldığında hem sistolik hemde diastolik
parametrelerde bozulma meydana gelmiĢtir. YaĢ ve pace vurusu sonrası
oluĢan QRS dalgasının süresinin global sol ventrikül fonksiyonları üzerinde
etkili olduğu gösterilmiĢtir.
15
Aynı araĢtırıcıların yaptığı bir diğer çalıĢmada 14 konjenital tam
AV bloklu hastada ( baĢka kardiyak patolojisi olmayan) 8 pacemaker
yerleĢtirilmesi öncesi ve 8 de pacemaker yerleĢtirildikten sonra olmak
üzere(3-12 yıl sonra, ortalama 5,5 yıl) 16 kardiyak biyopsi uygulanmıĢ ve
her iki biyopsi grubu arasında histolojik olarak fark saptanmıĢ ve sol
ventrikül
fonksiyonlarındaki
klinik
bozulma
bu
değiĢikliklerle
histolojik
iliĢkilendirilmiĢtir(30).
Yine DDD pacemaker yerleĢtirilen doğumsal tam AV bloklu
23
hastanın ( ortalama yaĢ:24±3 yıl), pacemaker implantasyonu öncesinde ve en
az 5 yıl sonrasında ekokardiyografileri ve egzersiz testleri yapılmıĢ. Ortalama
10
yıllık
kardiyak
pacingden
sonra,
sağlıklı
30
kontrol
grubuyla
karĢılaĢtırıldığında, pacemaker hasta grubunda daha fazla intraventriküler
dissenkroni, sol ventriküler yeniden Ģekillenme, dilatasyon, hipertrofi ve daha
düĢük kardiyak atım ve egzersiz toleransı bulunmuĢtur(31).
Koroner arter hastalığı olmayan, tam AV bloklu ve iki odacıklı
pacemaker
takılan 12
hastada,
implantasyondan 6
ay sonra
vntriküler
sitimülasyon bölgesinde bölgesel miyokardiyal perfüzyon ve duvar hareket
anormallikleri saptanmıĢtır. Ve bu tespit edilen bulgular 18.ayda daha da
belirginleĢmiĢtir(32).
Bu
sağ
ventrikül
apeksinin
uyarımı
ile
oluĢan
fonksiyonel
anormallikler sol ventrikül diastolik fonksiyonlarında bozulmaya ve ejeksiyon
fraksiyonunda
zamanla
azalmaya
neden
olmaktadır.Ġlginç
olarak,Tse
ve
arkadaĢlarının yaptığı bir çalıĢmada sağ ventrikül çıkım yolundan uyarımın
yapıldığı 12 pacemaker hastasında, bu olumsuz etkiler izlenmemiĢtir(31).
Miyokarddaki
sempatik
sinir
aktivitesinin
mikronörografi
yöntemi
ile
değerlendirildiği bir çalıĢmada, sağ ventriküler, sol ventriküler ve biventriküler
uyarımın etkileri değerlendirilmiĢ ve en yüksek doku sempatik sinir aktivitesi
sağ ventrikül apikal uyarımı sonucunda geliĢmiĢtir(33).
16
Kronik atriyal fibirilasyona bağlı taĢikardiyomiyopatili bir olguda his
demeti ablasyonu yapılmıĢ ve VVIR pacemaker implante edilmiĢ(34). Kalp
hızı artık kontrol edilebilmesine rağmen, sağ ventrikül pacinginin ilk yılı
içerisinde mitral yetersizliğin Ģiddetinde artma ve sol ventrikül ejeksiyon
fraksiyonunda
azalma
edilmiĢ.
tespit
Pacemaker
sistemi
biventrikülere
yükseltilmiĢ ve 6.ayda sol ventrikül diastol sonu çapı 69 mm den 62 mm ye
gerilemiĢ, sol ventrikül ejeksiyon fraksiyonu yükselmiĢ, mitral yetersizliği
ileriden orta dereceye gerilemiĢ, ve pulmoner arter basıncı 40 mmHg dan 22
mmHg ya düĢmüĢtür.
çalıĢması
DAVID
sağ
ventrikül
pacinginin
olumsuz
etkileri
konusunda önemli kanıtlar sağlamıĢtır(35). Bu çalıĢmada ICD implante edilen
256 hastalık gruba backup olarak VVI modunda (40 vuru/dk hız), 250
hastalık diğer gruba da
sağlanmıĢ
ve
değerlendirmede
DDDR modunda( 70 vuru/dk hız) pace backup ı
hastalar
DDDR
1
grubu
yıl
sonunda
VVI
grubu
değerlendirilmiĢlerdir.
Bu
karĢılaĢtırıldığında
kalp
ile
yetersizliği nedeni ile hastaneye yatıĢ ve ölüm için hazard oranı 1,61 ,
sadece kalp yetersizliği nedeni ile hastane yatıĢı için 1,54 ve sadece ölüm
için
1,61
hazard
oranı
saptanmıĢtır.
DAVID
çalıĢmasına
dahil
edilen
hastaların hepsinde ejeksiyon fraksiyonu %40 ın altındaydı. DDDR pace
grubundaki daha fazla hastaneye yatıĢ ve ölümün nedeni incelendiğinde,
DDDR grubunda 3.aydaki pace oranının %50, 12.ayda %61 olduğu, buna
karĢın VVI modunda 12.aydaki pace oranının %3 ün altında olduğu görülür.
DAVID
çlıĢmasında
DDDR
pace
grubundaki
hastaların
temel
hızları,
günümüzde programlanan standart hızlardan oldukça yüksekti.
MADIT II çalıĢması da sağ ventrikül pacinginin olumsuz etkilerine
dikkat çekmiĢtir(36).Bu çalıĢmaya 567 hasta dahil edilmiĢ ve 20 aylık takip
boyunca %50 nin üzerinde sağ ventrikül pacingi olan grupta (n:369), nadir
sağ ventrikül pacingi olan gruba kıyasla (n:198) daha fazla yeni yada
kötüleĢmiĢ kalp yetersizliği (%30‘ e karĢın %17, p:0.002, hazard oranı: 1.9)
ve kalp yetersizliği ve ölüm (%50 ye karĢın %20, p:0.004, hazard oranı: 1.8)
saptanmıĢtır. Subgrup analizlerinde özellikle ejeksiyon fraksiyonu %30 un
altında olan hastalarda kalp yetersizliği nedeniyle hastaneye yatış daha
17
yüksektir. Ayrıca bu çalıĢmada daha faza sağ ventrikül pacingi olan grupta
şok yada antitaşikardi acing (ATP) gerektiren
ventriküler taşikardi atağı
daha fazla saptanmıĢtır.
PAVE çalıĢması: Atrial fibrilasyon nedeni ile AV nod ablasyonu
yapılan ve akabinde pacemaker takılan (ablate-and-pace) 184 hastaya standart
sağ ventrikül apikal pacing ve biventrikül pacing uygulanmıĢ ve bu iki grup
hasta karĢılaĢtırılmıĢtır(37-38). Birincil sonlanım noktası olarak 6 dakika
yürüme testi, ikincil sonlanım noktası olarak da yaĢam kalitesi anketi ve sol
ventrikül ejeksiyon fraksiyonu belirlenmiĢtir.Bu çalıĢma mortaliteyi sonlanım
noktası olarak almamıĢtır.6 dakika yürüme testi ve LVEF biventriküler pace
grubunda daha iyi bulunmuĢ ancak hayat kalitesi skorunda anlamlı fark
saptanmamıĢtır. Subgrup analizlerinde, biventriküler pace takılan ve LVEF %
45 in altında olan grupta standart RV pacing grubuna kıyasla 6 dakika
yürüme testindeki mesafe %73 daha fazladır. Yine hastalar NYHA sınıfına
göre alt gruplara bölündüğünde,NYHA sınıf 2 ve 3 de biventriküler pacing,
sağ ventrikül pacingine kıyasla yürüme mesafesinde %53 oranında artıĢa
neden olmuĢtur.
disfonksyonu
olan
ÇalıĢma sonuçları incelendiğinde
hastaların
biventriküler
sol ventrikül sistolik
pacingden
daha
dazla
fayda
gördükleri saptanmıĢtır.
Bu
iki grup
arasındaki
farklılığın
grubunun LV fonksiyonlarını zamana karĢı
nedeni
biventriküler
pacing
daha iyi koruyabilmeleri buna
karĢın RV pacing grubunun daha çabuk bozulmasıdır. 6.ayda sol ventrikül
ejeksiyon fraksiyonu biventriküler pacing grubunda aynı kalırken, standart sağ
ventrikül pacingi yapılan grupta %3,7 oranında azalmıĢtır.
Bu çalıĢmada bize göstermiĢtir ki hiç değilse kalp yetersizliği
grubunda RV pacingine karĢı dikkatli olunmalıdır.
Pacemaker takılmıĢ 307 hastanın dahil edildiği bir çalıĢmada (
hastaların yarısı iki odacıklı, yarısı tek odacıklı pacemaker sistemine sahipti)
hastaların yaklaĢık yarısında (%54) kalp yetersizliği semptomları mevcuttu (
tek odacıklı pacemakerı olan hastaların %57 sinde, iki odacıklı pacemaker
18
sistemleri olan hastaların %50 sinde)(39). Kalp yetersizliği semptomları olan
hastaların yaklaĢık yarısında LVEF< %40 idi. Bu çalıĢmada göstermiĢtir ki,
pacing süresi ne kadar uzunsa, sol ventrikül sistolik disfonksiyonu ve atriyal
fibrilasyon sıklığıda o kadar fazladır.10 yıldan sonra kalp yetersizliği sıklığı
%24 den % 38‘e, atriyal fibrilasyon sıklığı da %26 dan %45‘e çıkmıĢtır. Bu
çalıĢmada sonuç olarak DDD pacemakerlarında sağ ventrikül pacinginin
olumsuz sonuçları açısından VVI lardan iyi olmadığını göstermiĢtir.
Bir baĢka randomize çalıĢmaya, ortalama yaĢı 74±9 yıl olan sinus
nod disfonksiyonlu ve normal AV iletimi olan 177 hasta dahil edilmiĢ ve üç
farklı modda pacing uygulanmıĢ(43). AAIR (n:54), kısa AV gecikmeli
DDDR(n:60),
uzun
AV
gecikmeli
DDDR(n:
63).
Pacemaker
implante
edilmeden önce ve takiplerde sol atriyum ve sol ventrikül boyutlarını
değerlendirmek için M-mod ekokardiyografi yapılmıĢtır. Ortalama 2,9±1,1 yıl
takip sonucunda,sağ ventrikül apikal pacingi yapılan her iki DDDR grubunda
sol atriyum ve sol ventrikül sistol sonu çaplarında artıĢ, daha sık atriyal
fibrilasyon saptanmıĢtır. Kısa AV gecikmeli DDDR pacing grubunda sağ
ventrikül pacing yüzdesi en fazla olmuĢ(%90) ve bu grupda AAIR grubuna
kıyasla sol ventrikül fraksiyonel kısalmada istatistiksel olarak anlamlı azalma
meydana
gelmiĢtir.
açısından
gruplar
Ölüm,
arası
tromboemboli
anlamlı
fark
ve
konjestif
saptanmamıĢtır.
kalp
Bu
yetersizliği
çalıĢma,
sağ
ventriküler pacingin olumsuz etkilerinden korunma anlamında , hasta sinus
sendromlu ve atriyoventriküler iletisi sağlam olan hasta grubnda atriyal
pacingin, sağ ventrikül apikal pacinge tercih edilmesi gerektiğini ortaya
koymuĢtur.
Bu
Ģekilde
atriyal
fibrilasyon
sıklığı
ve
sol
ventrikül
disfonksiyonu azalacaktır.
Sağ ventrikül apikal pacingi nedeniyle ritim regülasyonu sağlanırken,
apikal
pacingin
getirmiĢ
olduğu
asenkron
ventrikül
aktivasyonu
sorun
oluĢturmaktadır. Bu nedenle alternatif bölgelerden pacing yapılması gündeme
gelmiĢtir.
19
ALTERNATĠF BÖLGELERDEN VENTRĠKÜLER PACĠNG
Sağ ventrikül pacinginin bu olumsuz etkileri nedeni ile alternatif
pacing bölgeleri aranmıĢtır. Bu alternatif bölgeler, sağ ventrikülün diğer
kısımları ( septum yada çıkıĢ yolu), sol ventriküler bölgeler yada her iki
ventrikül
birdendir.
ventrikülde
Tek
unifokal
yada
bifokal
pacingde
düĢünülmüĢtür.(40-60)
ġu anki literatürde sol ventrikül pacinginin ( biventriküler pacingin bir
parçası olarak yada yalnızca) özellikle orta yada ağır derecede sol ventrikül
sistolik disfonksiyonu ve dirençli kalp yetersizliği olan hastalarda faydalı
olduğu
gösterilmiĢtir(12-26).
Daha
eski
dönemlerde
özellikle
dilate
kardiyomiyopati hatalarında AV senkroniyi sağlayarak semptomlarda iyileĢme
ve prognozu düzeltme giriĢimleri takılan iki odacıklı pacemaker sistemlerinin
neden
olduğu
elektriksel
ve
mekanik
dissenkroni
nedeni
ile
baĢarıya
ulaĢamamıĢtır(15). Standart sağ ventrikül apikal pacing ile sol ventriküler
yada biventriküler pacingi karĢılaĢtıran çalıĢmalar mevcuttur.
Hamdan ve arkadaĢlarının yaptığı bir çalıĢmada sağ atriyum, sağ
ventrikül ve lateral kardiyak vene pacemaker leadleri yerleĢtirilmiĢ ve sağ
ventriküler(RV), sol ventriküler(LV) ve biventriküler(BV) pacing modaliteleri
ile hemodinamik parametreler( sistolik, ortalama, diastolik kan basıncı ve
santral ven basıncı) ve sağ peroneal sinir fasikülüne yerleĢtirilen bir steril
mikrokateterle
elde edilen sempatik
ÇalıĢma sonucunda
sol
ventrikülü
sinir
aktivitesi karĢılaĢtırılmıĢtır(32).
pace eden
sistemlerle( LV ve BV)
hemodinamik parametrelerin daha iyi olduğu ve sempatik sinir aktivitesinin
sağ ventrikül pacingine(RV)
kıyasla daha
ventrikül pacinginin faydalı etkileri
az olduğu
saptanmıĢtır.
Sol
çalıĢmalarda gösterilmiĢ ancak sol
ventrikül pace tekniği baĢlangıçta sorun teĢkil etmiĢtir.BaĢlangıçta cerrahi
yöntemle yada robotik torakoskopik yöntemle epikardiyal lead yerleĢtirilmiĢ,
fakat son zamanlarda koroner sinusun sol ventriküler dallarına
yöntemle
lead
yerleĢtirilmesine
baĢlanmıĢtır.
Transseptal
transvenöz
yaklaşımla
endokarddan sol ventrikül pacingi önerilmiĢ fakat teknik olarak zor ve kronik
antikoagulasyon
gerektiren
bir
yöntemdir(61).
Grosfeld
ve
arkadaĢları
yaptıkları bir hayvan deneyinde, transvenöz yaklaĢımla sağ ventriküler taraftan
20
aktif fiksasyon sistemli bir lead yardımı ile interventriküler septumun sol
ventrikül
tarafında
subendokardiyal
yüzeye
kadar
ilerlemiĢ
ve
buradan
pacemaker ölçümlerini almıĢlar(62). GeliĢtirdikleri bu tekniğin güvenli, stabil
bir yöntem ve pacemaker thresholdunun düĢük olduğunu ileri sürmüĢlerdir.
Ancak hemodinamik ölçüm yapmamıĢlardır. Yine amitani ve arkadaĢları his
demeti pacingi yöntemini test etmek amacıyla bir çalıĢma yapmıĢlar ve deney
hayvanlarının
his
yerleĢtirilmiĢ
ve
demeti
standart
bölgesine
pace
vidalı
ölçümleri
aktif
alınmıĢ,
fiksasyonlu
ayrıca
2
bir
ay
lead
sonra
histopatolojik değiĢimler bakılmıĢtır. Ġleti sisteminde histolojik olarak bir
değiĢim saptanmamıĢtır.
SAĞ VENTRĠKÜL ÇIKIMYOLU PACĠNGĠ
Alternatif sağ ventriküler pacing bölgeleri arayıĢlarında sağ ventrikül
çıkım yolu en fazla çalıĢılan bölgedir(43,45-48,50-53,55). Sağ ventrikül çıkım
yolu
pacinginin
çalıĢmanın
hemodinamik
sağ
analizinde
hemodinamik
fayda
etkilerinin
ventrikül
görülmüĢtür(47).
araĢtırıldığı
apikal
Çoğu
dokuz
kıyasla
anlamlı
hemodinamik
etkileri
pacingine
akut
prospektif
karĢılaĢtıran bu çalıĢmalarda , yalnızca 2 tanesi uzun dönem etkileri
karĢılaĢtırmıĢ ve birinde iki bölge arasında anlamlı fark saptanmazken(49) ,
diğerinde sağ ventrikül çıkım yolunun pacingi ile ikinci ayda sol ventrikül
fraksiyonel kısalmasında anlamlı artıĢ sağlanmıĢtır(51).
Guidici ve arkadaĢları 89 hastada kalıcı pacemaker yerleĢtirilmesinin
hemen ardından continuous-wave echo Doppler ile kardiyak output ve
kardiyak indeksi ölçmüĢler ve sağ ventrikül çıkım yolu pacingi ile sırasıyla
8.8% (p <0.0001) ve
21.0% (p <0.0001) artıĢ saptamıĢlardır(45). Bu
çalıĢmada özellikle baĢlangıç kardiyak indeksleri daha düĢük olan hastalarda
daha fazla artıĢ dikkati çekmiĢtir. Çok küçük bir hasta grubunda (n:5), 6 ay
sonraki değerlendirmede her iki grup arasında benzer iyileĢme görülmüĢtür.
13 kalp yetersizliği hastasının dahil edildiği ve ventriküler leadin
interventriküler septuma yerleĢtirildiği bir çalıĢmada, hastanın kendi ritminin
olduğu
bazal
dönem
ile
pacemaker
takıldıktan
15-20
dakika
sonra
hemodinamik parametreler karĢılaĢtırılmıĢ ve değiĢim izlenmemiĢ (54). Yine
21
kalp yetersizliği olmayan 20 hastada, sağ ventrikül apikal pacing ile sağ
ventriküler çıkımyolu pacingi değerlendirilmiĢ ve 23 hafta sonra sistolik sol
ventrikül
fonksiyonlarının
çıkımyolu
pacingi
yapılan
grupta
daha
iyi
korunduğu saptanmıĢ(55). 24 hastalık bir baĢka çalıĢmada, yine sağ venrikül
apikal pacing ile çıkımyolu pacingi karĢılaĢtırılmıĢ ve çıkımyolu pacingi
grubunda pacemaker sonrası QRS süresinin daha kısa olduğu saptanmıĢtır.
Ayrıca 6.ayda fark olmamasına rağmen, sağ ventrikül çıkım yolu pacingi
yapılan grupta 18.ayda talyum miyokard sintigrafisinde perfüzyon defekti
(%83 e karĢın %33), ve radyonüklid ventrikülografide bölgesel duvar hareket
bozukluğu (%75 e karĢın %33) daha düĢük, sol ventrikül ejeksiyon fraksiyonu
ise daha yüksek (%53 e karĢın %47) bulunmuĢtur.
Sağ ventrikül çıkım yolu pacingi ile apikal pacingi karĢılaĢtıran
ROVA çalıĢmasına kalp yetersizliği olan, kronik atriyal fibrilasyonlu ve
EF<%40 olan 103 hasta dahil edilmiĢ ve bahsedilen pacing modaliteleriyle
birlikte 3. ayda hayat kalitesi sorgulaması yapılmıĢtır. Çıkımyolu pacingi
yapılan grupta QRS süreleri daha kısa ancak hayat kalitesi açısından kısa
dönemde bir fark bulunmamıĢtır(63).
Sağ ventrikül çıkım yolu pacingi ile ilgili önemli soru hangi bölgenin
pace edileceği sorusudur. Sağ ventrikül çıkım yolunun septal kısmı ile serbest
duvarı ve ayrıca sağ ventrikül giriminin septal ve serbest duvarından
kaynaklanan uyarılar yüzeyel EKG
eĢliğinde
bu
bölgelere
fiksasyon
ile ayrıt edilebilirler. Kısaca EKG
leadleri
doğru
bir
biçimde
yerleĢtirilebilir(64,65).
Sağ ventrikül çıkım yolunun pace edilmesindeki ana sorunlardan bir
tanesi yerleĢtirilen leadin pace ve sense seviyelerinin stabilitesidir.Viktor ve
arkadalarının yaptığı bir çalıĢmaya sağ ventrikül çıkım yolu ve apeksin
birlikte pace edildiği 16 hasta dahil edilmiĢ ve 10 ay takip neticesinde
leadlerde yerinden oynama ve pace/sense seviyelerinde
bahsedilen bölgeler
arasında fark saptanmamıĢtır.(51)
22
BRIGHT çalıĢmasında da yine aynı Ģekilde sağ ventriküle bifokal
pacing yapılmıĢ( apeks ve çıkımyolu) lead de ve pace/sense seviyelerinde iki
bölge arasında fark saptanmamıĢtır(66).
Bir genelleme yapılacak olursa, aktif fiksasyon yöntemleri neticesinde
sağ ventrikül çıkım yoluna yerleĢtirilen pacemaker leadlerinin yer değiĢtirme
oranları %0 ile 5 arasında, ortalama olarak %1 dir.
Sağ ventrikül çıkımyolu, sağ ventrikül septal, biventriküler ve sol
ventriküler pacingin akut ve kronik hemodinamik ve klinik sonuçlarını sağ
ventrikül apikal pacing ile karĢılaĢtıran çalıĢmalar tablo 1 de gösterilmiĢtir.
23
24
HĠS DEMETĠ, SAĞ VENTRĠKÜLER SEPTAL PACĠNG
YADA
BĠFOKAL SAĞ VENTRĠKÜLER PACĠNG
Sağ ventrikül apikal pacinginin sol ventrikül fonksiyonu üzerindeki
olumsuz etkilerinin mekanizması olarak değiĢik hipotezler iler sürülmüĢ ancak
en kabul edilebilir olarak sağ ventrikül apikal pacinge bağlı değiĢmiĢ
ventriküler
depolarizasyon
değerlendirilmiĢtir.
ve
Bundan dolayı
netice
fizyolojik
olarak
oluĢan
depolarizasyonu
dissenkroni
elde
etme,
örneğin direk his demeti pacingi ile, ventriküler dissenkroniyi azaltabilir yada
oluĢturmayabilir. Fakat his demeti pacingi ile ilgili , lead yerleĢtirme, capture
ve stabilite sorunu nedeni ile yeteri kadar daha yoktur.(67-69) ayrıca his
pacingi için his demeti sonrasındaki iletim sistemi intakt olmalıdır.
Dar QRS‘li, kronik atriyal fibrilasyonlu ve ejeksiyon fraksyonu %40
‗ın altında olan 12 hastada his demeti pacingi yapılmıĢ ve sol ventrikül
performansında anlamlı iyileĢme sağlanmıĢtır(68).Aynı araĢtırıcılar baĢka bir
çalıĢmada 54 hastanın 39 ‗una bu tekniği uygulamada baĢarılı olmuĢ ve
ortalama 42 aylık takip sonunda 29 hastaları hayatta kalmıĢ ve semptom ve
EF de anlamlı iyileĢme saptanmıĢtır.( %23 den %33‘e). Fakat bu iyileĢmenin
hız kontrolu ve ritim düzenliliğine mi yoksa pace edilen bölgeyemi bağlı
olduğu belirtilmemiĢtir.
Sağ Ventrikül Septal Pacing:
Ġki odacıklı pacemaker takılacak 14 hastlık bir çalıĢmada en kısa
QRS‘i elde etmek için Ġnterventriküler septum haritalanmıĢ ve sağ ventrikül
septal pacing ile QRS süresinde azalma ve sol ventrikülde daha homojen bir
kontraksiyon, sistolik performansta iyileĢme görülmüĢtür(52)
Atrial fibrilasyonlu 12 hastaya his demeti ablasyonu yapılmıĢ ve RV
septal pacing ile apikal pacing çapraz dizayn ile karĢılaĢtırılmıĢ.RV septal
pacing daha dar QRS, daha iyi sistolik performans ve daha iyi sol ventrikül
EF ile iliĢkili bulunmuĢtur.(49)
25
Bifokal Sağ Ventriküler Pacing:
Herhangi bir nedenle ( koroner sinüsü kanule edememe, lead ilerletme
sorunu, leadi yerleĢtirecek uygun venöz dal bulamama, frenik sinir uyarılması
yada skar dokusu nedeni ile sense ve pace edememe) biventriküler pacing
yapılamayan
kalp
yetersizlikli
hatalara
uygulanmıĢ
ve
22
aylık
takip
neticesinde kabul edilebilir klinik iyileĢmeler meydana gelmiĢtir(70)(tablo 4).
Aynı bulgular New York Heart Association‘a göre
sınıf III, 39 AV tam
blok ve kalp yetersizliği hastasının dahil edildiği çalıĢmada da mevcuttur(71).
50
NYHA sınıf 2-3
hastanın
dahil edildiği ROVA çalıĢmasında
sağ
ventriküler bifokal pacing ile kısmi iyileĢme elde edilmiĢtir(63).
Kalp yetersizliği, sol dal bloğu ve mitral yetersizliği olan 25 hastaya
sağ ventrikül apeks ve interventriküler septum bazal bölgeden bifokal pacing
yapılmıĢ, 18 aylık takip sonucunda bifokal sağ ventriküler pacing QRS
süresini anlamlı olarak daraltmıĢ, mitral yetersizliğini azaltmıĢ, hemodinami
ve hayat kalitesini anlamlı olarak artırmıĢtır(72). Ġnter ve intraventriküler ileti
gecikmeleri azalmıĢtır.
Biventriküler yada Sol Ventriküler Pacing:
Sağ ventriküler pacing ile biventriküler yada sol ventriküler pacingi
karĢılaĢtıran çalıĢmalar mevcuttur(33,42,56,57). Ciddi kalp yetersizliği ile
beraber birinci derece AV blok ve/veya intraventriküler ileti gecikmesi
bulunan 27 hastada sol ventriküler yada biventriküler pacing ile bazal duruma
ve sağ ventriküler pacinge kıyasla akut hemodinamik parametrelerde iyileĢme
sağlanmıĢtır(42).
CRT yapılan 33 hastanın dahil edildiği bir baĢka çalıĢmada , implant
iĢleminden hemen sonra biventriküler , sağ ventrikül apeks pacingi ile ve
pace edilmeksizin TDĠ ile akut hemodinamik değiĢimler test edilmiĢ, yalnızca
biventriküler
yetersizlikte
pace
ve
sol
modunda
ventrikül
sistolik
fonksiyonlarda
boyutlarında
azalma,
iyileĢme,
sistolik
mitral
asenkronide
düzelme saptanmıĢtır(57).
Bir baĢka çalıĢmada 13 hastada hemodinamik parametreler ve sempatik
sinir aktivitesi ölçülmüĢ.sağ ventrkül, sol ventrikül ve biventriküler modlarda
3‘er dakikalık pacing sonrası bahsedilen parametreler değerlendirilmiĢ, sol
26
ventrikül ve biventriküler pacing grubunda QRS süresinden bağımsız olarak
sol ventrikül disfonksiyonu
olan
hastalarda
hemodinamik
parametrelerde
iyileĢme, sempatik sinir aktivitesinde azalma saptanmıĢtır.
Bir baĢka çalıĢmada koroner sinüs yoluyla sol ventrikül pacingi
sistolik fonksiyonları iyileĢtirmede biventriküler pacingden daha hafif ama sağ
ventriküler
apikal
yada
septal
pacingden
biçimde
belirgin
daha
iyi
bulunmuĢtur(56).
Kronik sağ ventrikül pacingi uygulanan 20 hasta en az 6 aylık süre
sonunda biventriküler moda upgrade edilmiĢ ve bundan sonraki 3 yada
6.ayda
yeniden
değerlendirilmiĢtir(59).
NYHA
fonksiyonel
sınıfda,
sol
ventrikül diastol ve sistol sonu çapta azalma, sol ventrikül ejeksiyon
fraksiyonunda artma saptanmıĢtır. Hastaneye yatıĢ %81 azalmıĢ, hayat kalitesi
artmıĢtır.
PAVE
çalışması:
Kronik
atriyal
fibrilasyon
nedeni ile AV
nod
ablasyonu yapılmıĢ hastalarda biventriküler pacing ile sağ ventrikül pacingi
karĢılaĢtırılmıĢ. 252 hasta dahil edilmiĢ ve 146 hasta ablasyon+biventriküler
pacing, 106 hasta ablasyon +sağ ventriküler pacing koluna alınmıĢ. Primer
sonlanım noktası 6 dakika yürüme testi ile değerlendirilen egzersiz kapasitesi,
sekonder sonlanım noktası peak O2 kullanımı ile değerlendirilen fonksiyonel
kapasite, egzersiz süresi ve hayat kalitesi skoru olarak belirlenmiĢtir. 3 .aya
kadar her iki grupta 6 dk yürüme testinde iyileĢme saptanırken, 3.aydan
sonra yalnızca biventriküer grupta fonksiyonel kapasitedeki iyileĢme devam
etmiĢtir. Sol ventrikül ejeksiyon fraksiyonu biventriküler pace grubunda stabil
seyrederken,
sağ
ventrikül
pacing
grubunda
6.aydan
sonra
azalmaya
sol
ventrikül
baĢlamıĢtır.( %45 den %41‘e)
PAVE
çalıĢmasının
subgrup
analizinde
özellikle
disfonksiyonu olan ( EF<%45 yada NYHA sınıf 2-3 ) grupta biventriküler
pacing daha faydalıdır(73). NYHA sınıf I yada normal sol ventrikül
ejeksiyon fraksiyonu olan hastalarda fayda daha azdır. Sol ventrikül sistolik
fonksiyonu normal dahi olsa uzun dönemde sağ ventrikül apikal pacinginin
neden olduğu mekanik asenkroni potansiyel olarak kötü sonuçlar doğurmaya
adaydır
ancak
bunun
ne
zaman
olacağı
yada
neden
sağ
ventrikül
fonksiyonlarında azalmaya neden olmadığı araĢtırılmalıdır.
27
Sol Ventrikül Pacing:
ġu ana kadar yapılan çalıĢmalar sol ventrikül pacingi ile biventriküler
pacing
arasında
anlamlı
fark
olmadığını göstermiĢtir.
Bu
anlamda sol
ventrikül pacing tek baĢına yeterli gibi gözükmektedir(17).
Köpeklerde yapılan bir çalıĢmada , sağ ventrikül ile sol ventrikülün
değiĢik bölgelerinden pacing yapılmıĢ ve sol ventrikül septum ve apeks
bölgesinden pacing ile sol ventrikül fonksiyonlarının daha iyi idame ettirildiği
saptanmıĢtır. Neden olarak da, uyarıların purkinje sisteminden çıktıkları yerler
olduğu için, bu bölgelerin pacingi ile daha fizyolojik bir iletim sağlandığı
düĢünülmüĢtür(74).
Bir baĢka çalıĢmada 11 sağlıklı köpek ile 8 çocuk karĢılaĢtırılmıĢ ve
sol ventrikül apikal pacinginin sağ ventrikül apikal pacingine kıyasla daha
üstün hemodinamik performansa neden olduğu saptanmıĢtır(75).
Sol ventriküler pacing ile biventriküler pacingin karĢılaĢtırıldığı bir
çalıĢmada
semptomlardaki
iyileĢmede
ve
sol
ventrikül
performansını
değerlendiren parametrelerde benzer bulgular saptanmıĢtır.
86
kalp
yetersizliği
hastasında
sol
ventrikül pacinginin
egzersiz
toleransı ve hayat kalitesinde anlamlı iyileĢme sağladığı ve bu etkinin
özellikle QRS süresi 150ms üzerinde olan hastalarda görüldüğü saptanmıĢtır.
Buna karĢın kronik atriyal fibrilasyon nedeni ile his demeti ablasyonu
yapılan, ciddi kalp yetersizliği bulunan 13 hastada biventriküler pacing sol
ventriküler pacinge kıyasla daha iyi hemodinamik sonuçlar sağlamıĢtır(76).
Otörler bunu sol ventrikül pacingi ile oluĢan interventriküler dissenkroniye
bağlamıĢlardır.
Triventriküler Pacing:
Biventriküler pacinge yanıt vermeyen kalp yetersizliği hastalarında yeni
bir yöntem olarak öne sürülmüĢtür. Sağ ventrikül apaks, çıkımyolu ve sol
ventrikül pace edilir.13 hastalık küçük bir çalıĢmada QRS süresinde anlamlı
28
olarak kısalmaya
neden olduğu, hemodinamik parametrelerde iyileĢmeye
neden olduğu saptanmıĢtır(77).
NORMAL MĠYOKARDĠYAL ELEKTRĠKSEL ĠLETĠM
Ventriküllerin normal aktivasyonu, elektriksel impulsun atriyaventriküler
noddan his demetine iletimi ile baĢlar. Daha sonra his demeti sağ ve sol ana dallara
ayrılır ve bu dallar birkaç major fasikül vererek, subendokardiyal bölgede lokalize
purkinje lifleri ağı halinde sonlanırlar. Sol ventrikülde bu purkinje lifleri ağı
papiller adaleleri de kapsar( 78,80).bu hızlı iletim ağının kalınlığı ve endokardepikard arasındaki yerleĢim düzeyi türler arasında farklılıklar gösterir.
Purkinje lifleri içerisindeki impuls iletimi bazalden apikale doğrudur veçok
hızlı gerçekleĢir (3-4 m/sn) (80-83)
Sağ ve sol dal ve bunlardan ayrılan ana dallar çevresindeki miyokard
dokusundan izoledirler. Ġmpulslar purkinje sistemini sağ ventrikülün alt ¼ ‗ünde ,
sol ventrikülü ise alt 1/3 ‗ ünde terkeder( 80). Bu çıkıĢ bölgesi miyokard dokusunda
aktivasyonun baĢladığı ik bölgeye tekabil eder. Ġnterventriküler septumda
aktivasyon apeksden bazale doğru meydana gelir(86-88). Sağ ve sol ventrikülde de
aktivasyon apeksden bazale ve endokarddan epikarda doğru olur( 86,89,90). Bu
impuls iletiminden dolayı posterobazal bölge en geç aktive olan ventrikül kısmıdır.
Elektriksel uyarı miyokard içerisinde, purkinje sistemine kıyasla yaklaĢık 4
kat daha yavaĢ iletilir.(83-85, 88,90). Ġnsanda total ventriküler aktivasyon 62-80
msn de sonlanır. Bu da QRS süresinde 70-80 msn‘ye denk gelir(86).
ANORMAL MĠYOKARDĠYAL ELEKTRĠKSEL ĠLETĠM
Ventriküllerin anormal aktivasyonu, sağ ve sol dal bloğu gibi iletim
sisteminin etkilendiği durumlar sonucu , aksesuar iletim yolları varlığında yada
ventriküler ektopi veya ventriküllerin pacemaker ile uyarımı sonucunda görülebilir.
Bu anormal iletimde miyokardın dört özelliği önemlidir.
Ektopik olarak oluĢan impuls, oluĢtuğu miyokard bölgesinden hızlı ileti sistemine
zayıf olarak girer.( normal miyokardda elektriksel iletim his purkinje sistemini
29
miyokardın apikal bölgesine yakın terkeder ve miyokardiyal ileti baĢlar.
Ventriküler pacingde yerden bağımsız olarak uyarı yavaĢ iletimli miyokard
dokusunda baĢlar)
Miyokarddaki iletim hızı purkinje sistemindekinden dört kat daha yavaĢtır ve
ventriküler pacing ile oluĢan aktivasyon sinüs ritmi ve atriyal pacine kıyasla daha
asenkrondur.
Kas liflerinde iletim iki yönlü ilerler. Lif boyunca iletim life dik yönlü iletimden 2
kat daha hızlıdır. Buda elips Ģeklinde bir iletim dalgasına neden olur ( figür 1, alt
panel)
Endokardiyal fiberler purkinje sisteminin parçası olmamalarına rağmen sol
ventrikülün diğer bölgelerinden daha hızlı iletime sahirtirler.( Ģekil 1, alt panel).
Bundan dolayı sol ventrikül endokardiyal pacing ile elektriksel aktivasyon için
geçen total süre epikardiyal pacingden daha kısadır.
Miyokardiyal iletim zaman aldığı için ventrikül pacingi QRS süresinde
sinus ritine göre iki kat artıĢ sağlıyor. Sağ ventrikül apeks pacinginde sol ventrikül
lateral duvar pacingine kıyasla QRS süresi daha kısadır. En uzun QRS süresi sol
ventrikül
posterobazal bölge pacinginde saptanmıĢtır. Bu anormal aktivasyon
paterninden kaçınmak için mümkün olduğunca hızlı iletim sistemine yakın pacing
yapılmalıdır.
Anormal kontraksiyon paternleri:
Ventriküler pacing ile bölgesel duvar kalınlaĢmasında(91-93) ve duvar
hareketlerinde(94-97) anormallikler saptanmıĢtır.
Sistolde segmenter kısalmanın pacing bölgesinden uzaktaki segmentlerde
daha büyük olduğu tespit edilmiĢtir.(94,98)
Badke ve arkadaĢlarının yaptığı çalıĢmada ventriküler pacing ile bölgesel
sol ventrikül fonksiyonlarındaki değiĢimler araĢtırılmıĢtır. Köpeklerde sol ventrikül
anterobazal bölge, anterior apeks ve posterior apeks bölgelerinin lokal
fonksiyonları, atriyal, sağ ventriküler, sol ventrikül apeks ve bazal bölge pacingleri
yapılarak karĢılaĢtırılmıĢ. Ventriküler pacing ile asenkron bir kontraksiyon,
miyokardiyal kısalmada bölgeler arası farklılıklar ve peak sistolik basınç ve peak
dp/dt de atriyal pacinge kıyasla azalma saptanmıĢ. Diğer grup köpekte lateral duvar
30
ve septum hareketi, atriyal ve sol ventrikül lateral duvar pacingi yapılarak
karĢılaĢtırılmıĢ, ventriküler pacing ile her iki duvar arasında resiprokal değiĢimler
saptanmıĢtır. Erken lateral kısalma septal bulgingi, geç septal kısalmada lateral
duvarda sistolik uzamayı tetiklemiĢtir. Bu karĢılıklı duvarlar arası resiprokal
değiĢiklikler, ventrikülde volüm hapsine ve basıncın yeterince yükselememesine,
miyokardiyal kontraksiyonun boĢa harcanmasına yol açarak global ventrikül
fonksiyonu üzerinde olumsuz etkilere neden olmuĢtur.
Şekil 1: Birinci panelde sağ
atriyal pacing ile oluşan
senkron miyokardiyal
aktivasyon izlenmeltedir.
İkinci panelde sağ
ventrikül apikal pacingi
neticesinde postreior
septumda elips şeklinde
erken kısalma( early
shortening) oluşuyor ve
septumun diğer
bölgelerine yayılıyor.
Alttaki panelde ise sol
ventrikül serbest
duvarının epikardiyal
uyarımı sonucu yine elips
şeklinde erken kısalma
oluşuyor( tek ok) ve iki
okla gösterildiği şekilde
endokardiyal yüzeyde
epikardiyal yüzeyden
daha hızlı yayılıyor.
31
MEKANĠK DĠSSENKRONĠN DEĞERLENDĠRĠLMESĠ
Atriyoventriküler Dissenkroni
Atriyal
doluĢun
kontraksiyon
ardından
sol
ideal
ventrikül
olarak
erken
diyastol
kontraksiyonunun
ile
ventriküler
hemen
öncesinde
gelir. Zamanında meydan gelmiĢ bir atriyal
kontraksiyon miyokardiyal
gerilme ve sol ventrikül önyükünde bir artmaya
neden olarak daha güçlü bir
ventriküler kontraksiyona neden olur(99). Atriyoventriküler dissenkroni AV
ileti geciktiği zaman( geç LV kontraksiyonu) yada
geciktiği zaman (geç sol atriyal kontraksiyon) meydana
atiyumlar
arası
ileti
gelir.
AV dissenkroni, mitral kapakta inkompetans, geç diyastolik mitral
yetersizliği , eĢ zamanlı aktif ve pasif ventrikül doluĢu (dopplerde E ve A dalgasının
f üzyonu), A dalgasının trunkasyonu yada diyastolik doluĢ zamanının kısalmasına
neden olabilir.
Ġnterventriküler Dissenkroni
Ġnterventriküler(ĠV) dissenkroni sağ ve sol ventrikül aktivasyonu arasında
40 ms den daha fazla gecikme olması olarak tanımlanır(100). ĠV dissenkroni
pulmoner ve aortik çıkıĢ yollarından elde edilen doppler akımları arasındaki zaman
farkından yararlanılarak hesaplanır. Alternatif olarak doku doppler inceleme ile
sample volum sol ventrikülün bazal septum, lateral duvarı ve sağ ventrikülün bazal
serbest duvarına yerleĢtirilerek alınan örnekler arasında, RV ve LV mekanik
aktivasyonunun zaman farklarından hesaplanabilir. Ġnterventriküler dissenkroni
birçok çalıĢmada CRT cevabının öngörücüsü olarak bulunmamıĢtır.
Ġntraventriküler Dissenkroni
Ġntraventriküler mekanik dissenkroni, sistol boyunca sol ventrikülün farklı
duvarlarının eĢ zamanlı olarak hareket etmemesidir. Bu CRT ile düzeltilen temel
anormallikdir. Ġntraventriküler dissenkroniyi değerlendirmek için, ekokardiografi
temelli bazı teknikler mevcuttur. Bunlar aĢağıda özetlenecektir.
32
M-Mode inceleme:
M-Mode, basit, spesifik ekipman gerektirmeyen ve datası kolaylıkla analiz
edilebilecek bir yöntemdir. M-Mode ekokardiyografi örneği parasternal aksdan
septum ve posterior duvardan geçecek Ģekilde alınır (ġekil 2).
Şekil 2: Sol ventrikül posterior
ve septal duvarının pik sistolik
içe hareketleri oklar ile
gösterilmiştir. Bu hareketler
arasındaki zaman farkı M-Mode
ile değerlendirilen
intraventriküler asenkroni
değeridir. 130 ms den uzun
olması asenkroni olarak
değerlendirilir(9). Bu vakada
140 msn dir.
Bu teknik sadece bazal iki duvarı karĢılaĢtırdığı için değeri düĢüktür. Diğer
segmentlerin dissenkronisi değerlendirilmez. Ayrıca görüntü kalitesine bağımlı ve
duvarlardaki pik içe hareketin ayırt edilmesi ( özellikle KMP li hastalarda septum
hareketi) değerlendirmeyi güçleĢtirebilir.
TVI( tissue velosity imaging- doku velosite görüntüleme):
33
TVI, intraventriküler asenkroniyi değerlendirmede en sık kullanılan
yöntemdir. TVI miyokardın velositesini(hızını) ölçer
ve bu genellikle kan
velositesinin %10 udur.
Şekil 3: apikal 2 boşluk
pencereden TVI ile
longitudinal miyokard
velositelerinin
değerlendirilmesi
Yukardaki Ģekilde TVI analizi için apikal iki boĢluk görüntüde iki bazal ve
iki mid bölge seçilmiĢtir. Sistolde (S) tüm segmentler transdusere doğru hareket
etmekte, diyastolde erken( E) ve geç diyastolik (A) miyokard relaksasyon
velositeleri oluĢmaktadır. Asenkroni değerlendirilmesi gösterilen pik miyokard
velositeleri arasındaki zaman farkının hesaplanması temeline dayanır. Genellikle
apikal 4 ve 2 boĢluk ile apikal uzun aks görüntüleri alınır, bazal ve mid segmentlere
örneklem yerleĢtirilerek 12 segmentin değerlendirilmesi yapılır. Sonuçlar değiĢik
yöntemlere göre yorumlanır. Yu ya göre bu 12 segmentin QRS baĢından pik
sistolik velositeye kadar geçen zamanlarının standart sapması alınır ve 32,6 ms
değerinden büyükse asenkroni olarak değerlendirilir.
BaĢka bir yaklaĢımda en
erken ve en geç pik velositeler arasındaki fark 65 ms‘den büyükse asenkroni olarak
değerlendirilir(10). Sadece bazal segmentlerin pik sistolik velositeleri arasındaki
fark > … ms ise asenkroni olarak değerlendirilir.
Genel olarak asenkroni değerlendirilmesinde TVI‘ı temel alan çalıĢmalarda
görüntüler sol ventrikülün apikal pencerelerinden alınsada( longitudinal sol
ventrikül hareketi), bazı son çalıĢmalarda kısa aks incelemeden radial sol ventrikül
velositeleri kullanılmıĢtır( 101).
Mekanik asenkroniyi değerlendirmek için gelecekte longitudinal, radiyal ve
sirkumferansiyel hareketler kombine olarak değerlendirilecektir.
34
TVI kullanılan cihazların büyük bir bölümünde mevcut olan bir opsiyondur.
Literatürdeki datanın büyük bir bölümü TVI kullanımından gelmiĢtir. Dezavantajı
ise, bazı hastalarda hangi velositenin pik sistolik velosite olduğu net olarak
değerlendirilemeyebilir
ve
zaman
alıcı
bir
yöntemdir.
Gözlemcilerarası
variyabilitesi %15 lere kadar çıkabilir.
Teknik özellikler ve sınırlılıklar: TVI klinik olarak kullanılabilir bir yöntem
olmasına rağmen, kaliteli görüntü elde etme ve değerlendirme açısından bazı
özellikler
arzetmektedir.
TVI
ile
amaç
―miyokardiyal
velositelerin
zamanlamasındaki küçük değiĢimlerden‖ bir sonuç elde etmek olduğu için,
variyabilite azaltmak çok önemlidir ve bunun içinde ―frame rate‖i
mümkün
olduğunca yüksek görüntü alınmalıdır.
Bu özellikle kalp yetersizliği hastalarında önemlidir çünkü nispeten daha
büyük ventrikülü inceleme sahasına sokmak için daha büyük sektör açısı
gerekecektir bu da frame rate‘i düĢürecektir. EKG ölçümlerin referans kaynağı
olacağı için net olarak elde edilmelidir. Özellikle AF li olgularda analiz daha güç ve
sonuçlar daha az güvenilirdir.
Tissue Tracking:
Tissue
tracking
(TT)
bir
miyokardiyal
segmentin
transduserden
uzaklaĢmasını ve yakınlaĢmasını değerlendirir. TT eğrileri TVI datasından elde
edilir. Bu modda miyokard segmentleri sistolde transdusre göre yaptığı hareketin
amplitüdüne göre belirlenmiĢ renklerle kodlanır. Normal bir kalpte bu renkli
bölümler kalbin uzun aksı boyunca bezer kalınlıkta ve simetrik olmalıdırlar.
Miyokarda kademeli bir hareket amplitüdü vardır. Yani bazal segmentlerde hareket
en fazla iken apikal segmentlerde an azdır.
35
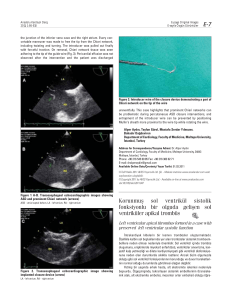
Şekil 3: sol ventrikül sistolik
disfonksiyonu olan bir
hastada tissue tracking ile
miyokardial asenkroniyi
gösteren bir resim. Oklar
apikal 4 boşluk incelemede
bazal septal ve bazal lateral
segmentlerin pik miyokardial
yerdeğişimlerii
göstermektedir.
ġekil 3 de bazal lateral segmentde aktivasyon septal segmentden daha geç
baĢlıyor. Lateral
duvar geç aktivasyon nedeni ile erken ve orta sistolde
kontraksiyona katkıda bulunmuyor. Apekse doğru pik duvar hareketi geç meydana
geliyor ve netice olarak sistolik fonksiyona katkı sağlamayan ve boĢa giden bir
kontraksiyon meydana geliyor.
TT‘nin avantajları:
Ölçümde minimal hata payı
Pik duvar hareketinin zamanlamasının ölçümü çabuk ve kolaydır
Bölgesel ve global longitudinal sistolik fonksiyon net olarak değerlendirilir.
Dissenkronide ve sistolik fonksiyondaki hafif değiĢimler tespit ediebilir ve bu
bilgiler CRT‘ye cevabı değerlendirmede ve pacemaker parametrelerini ayarlamada
kullanılabilir.
TT‘nin dezavantajları:
Yazılımı ekokardiyografi cihazlarında yaygın değil
CRT‘ye cevap verecek hastaları öngörmede TVI kadar yagın çalıĢılmamıĢtır.
TT miyokardiyal hareketi değerlendirdiği için, miyokardiyal velositeyi
değerlendiren TVI ile dissenkroni değerlendirmeinde farklı sonuçlar verebilir (Ģekil
4).
36
ġekil 4: Aynı hastadan, aynı
miyokardial segmentlerden
alınan tissue tracking( üstteki
pencere) ve TVI eğrileri
görülmektedir. Birinde
asenkroni izlenirken
diğerinde asenkroni
izlenmemektedir. Bu da
dissenkroni değerlendirirken
pik velositenin mi yoksa pik
hareketin (dispacement) mi
zamanlamasının daha önemli
olduğu sorusunu akla getirir.
Strain ve Strain Rate:
Strain ve strain rate(SRI)
görüntüleme renk kodlu-TVI türevi bir
incelemedir. TVI ile yalnızca miyokardiyal velositeler değerlendirilirken SRI
incelenen bölgedeki iki nokta arasındaki miyokardiyal deformasyonu değerlendirir.
Bundan dolayı SRI, TVI ve TT‘ e zıt olarak aktif ve pasif miyokardiyal hareketi
ayırt edebilir. SRI kullanılarak , QRS baĢından pik sistolik straine kadar geçen süre
ölçülerek
LV
dissenkroni
nicelik
olarak
belirtilebilir.
LV
dissenkroni
değerlendirmek için baĢlangıçta apikal görüntü pencereleri kullanılmıĢ ancak
yöntemin açı bağımlılığı nedeni ile etkinliği ve tekrarlanabilirliği düĢük
bulunmuĢtur (102). Daha sonraları kısa aks görüntü pencereleri kullanılmıĢ ve
buradan radial stran değerleri ölçülmüĢtür. Septal ve psoterior duvardaki pik
sistolik strainler arasındaki 130 ms zaman farkı CRT ile strok volümde artma
olasılığını %95 duyarlılık ve %85 özgüllük ile öngörebilir (103).
37
Speckle Tracking:
Konvansiyonel iki boyutlu ekokardiyografi görüntülerinden miyokardiyal
straini hesaplamak için geliĢtirilmiĢ bir tekniktir. TVI kaynaklı strain incelemesine
nazaran daha az açı bağımlıdır.
Tissue Synchronization Imaging ( doku senkronizasyon görüntüleme):
Doku senkronizasyon görüntüleme( TSI), TVI datasını temel alarak
oluĢturulmuĢ bir yöntemdir. Her bir miyokardiyal segment QRS baĢından pik
velositeye ulaĢma süresine göre önceden belirlenmiĢ renk kodları ile kodlanır. En
kısa sürede pik velositeye ulaĢan segment yeĢil, en geç ulaĢan segmentler ise
turuncu-kırmızı renk alırlar. ( Ģekil 5)
Ġnceleme yapılmadan önce aortik kapağın açılma ve kapanma zamanları sol
ventrikül çıkımından elde edilen doppler trasesinden yada m-mode yöntemi ile
iĢaretlenir. Bu iĢaretler EKG trasesinde istenirse sistolün sadece ejeksiyon
periyoduna denk gelecek Ģekilde manuel olarak ayarlanabilir. Bu Ģekilde varsa
yüksek velositeli postsistolik kısalma devre dıĢı bırakılmıĢ olur.
ġekil 5: apikal 4 boĢluk
incelemede miyokard
segmentleri pik velositelerine
ulaĢma sürelerine göre renk
alırlar. Bu resimde lateral
duvar pik velositeye daha geç
ulaĢmıĢ kırmızı renk koduyla
kodlanmıĢtır.
Avantajı:
Hangi miyokardiyal segmentin gecikmiĢ pik velosite gösterdiği kolayca
anlaĢılabilir.
Dezavantajı:
Bu yöntem TVI ve TT gibi daha detaylı ve nicel yöntemlerle kıyaslandığında
dissenkroniyi değerlendirmedeki duyarlılığı daha düĢüktür .
38
DeğiĢik ekokardiyografik yöntemlerle dissenkroninin değerlendirilmesi tablo da bir
bütün halinde özetlenmiĢtir(tablo 2)
Tablo 2 :Asenkroninin ekokardiografik değerlendirilmesinde özet bilgi
Değerlendirme yöntemi Kriter
EkG
M-mod
pw-TDI
pw-Doppler eko
kardiografi
2Boyutlu-TDI
segmentler
sınırlılıklar
I.Global ventriküler asenkroni
QRS süresi
Global
MI sonrası
>120 ms
değerlendirme LBBB
Septalskar dokusu,
posterior duvar
septal ve
sadece septal
hareket
posterior
yada
gecikmesi
posterior
>130 ms
LV içi (5
bazal segment)
Kümülatif
ve
DüĢük
asenkroni >102 interventriküle uzaysal
ms
r ( RV lateral
çözünürlük
segment‘e
karĢı)
II.Interventriküler asenkroni
Ġnterventriküle
r mekanik
Aortik ve
EĢ zamanlı
gecikme
pulmoner
değil
(IVMG) >40
çıkımyolu
ms
III. Intraventriküler asenkroni
Ts-SD:
intraventriküler
sistolik
12 segment
asenkroni
indeks: >33 ms
septal-lateral
time-to-peak
TDI farkı ,
12 segment
sınır değer >60
ms
Ortalama
bölgesel
12 segment
miyokardiyal 4 segment
performans
Analiz
zamanı
kısa
kısa
uzun
kısa
kompleks
(post-proces
gerektirir)
uzun
kompleks
uzun
kompleks
uzun,
offline
39
indeksi: Q
dalgasından
pik sistolik
yerdeğiĢime
kadar geçen
zamanın
bölgesel
farkları
Ts-SD: sınır
değer; 31,4 ms
12 segment
Strain ve strain
rate
Sistolde
Myokardiyal
deformasyon,
post-sistolik
kısalma varlığı
12 segment
Tissue Tracking
GecikmiĢ
longitüdinal
kontraksiyon
>2 basal
segment
Apikal 4
boĢluk
görüntüde 12
bazal segment.
TSI
QRS baĢından
pik sistolik
velositeye
geçen zaman
(apikal uzun
aksda
anteroseptumposterior arası
farkda
sınır değer >65
ms)
16 segment,
apeks hariç
3 boyutlu eko
Kuantitatif
kriter yok
kompleks
kompleks,
zaman alıcı,
dilate
ventrikülde
düĢük
rezolüsyon
LV ile iliĢkili
olaylarda
düzgün
zamanlama
gerektirir.
Tüm
segmentler
uzun
uzun
kısa
Sadece
velosite
datası
kısa
AzalmıĢ
uzaysal
çözünürlük
Zaman
alıcı ve
offline
analiz
gerektir
ir.
Kaynak: Knebel et al. Cardiovascular Ultrasound 2004 2:17
40
EGZERSĠZĠN DĠSSENKRONĠ ÜZERĠNE ETKĠSĠ
Egzersizin sol ventrikül disssenkronisi üzerine atkisini araĢtıran çeĢitli
çalıĢmalar mevcuttur. Ennezat ve arkadaĢlarının yaptığı çalıĢmada kronik kalp
yetersizliği olan bir hasta grubunda, dinamik egzersizle mitral yetersizliği
ciddiyetindeki değiĢimin potansiyel nedenleri araĢtırılmıĢtır. ÇalıĢmaya iskemik
yada noniskemik kardiyomiyopatili , sol ventrikül ejeksiyon fraksiyonu <%40 ve
fonksiyonel
mitral
yetersizliği olan 70
hasta dahil edilmiĢtir.
Ġskemik
kardiyomiyopatili hastalarda optimal revaskülarizasyon iĢlemi yapılmıĢtır. Atriyal
fibrilasyon, ortopedik kısıtlılıklar, uyarılabilir miyokardiyal iskemi ve kötü
ekokardiyografik görüntü kalitesi dıĢlama kriteri olarak seçilmiĢtir. Egzersiz,
bisiklet ergometrisi ile semptom sınırlı olarak yapılmıĢtır. Ekokardiyografik olarak
sol ventrikül volümleri , ejeksiyon fraksiyonu, mitral yetersizliği derecelendirilmesi
için PISA( proximal isovelosity surface area)
orifice)
ile ERO( effective
regurgitan
ölçümü, regurgitan volüm, sistolik mitral anuler çap ölçülmüĢtür.
Ġntraventriküler asenkroni TVI ile, interventriküler asenkroni dopplerde aortik ve
pulmoner ejeksiyon dalgalarından yararlanılarak ölçülmüĢtür(103).
ÇalıĢma sonucunda egzersiz ile kalp hızı ve kan basıncı artmıĢ, sol ventrikül
diyastol sonu volümü azalmıĢtır. Sol ventrikül ejeksiyon fraksiyonu değiĢmemiĢtir.
Mitral yetersizliğinde egzersiz ile birlikte çok değiĢken sonuçlar elde edilmiĢtir.
Hasta grubunun %59‘unda mitral yetersizliği kötüleĢmiĢtir. Bu hasta grubunda
değiĢiklikler egzersiz süresi ve peak vO2 ile iliĢkili değildir.
Mitral yetersizliği ERO ve RV deki değiĢiklik istirahat halindeki
intraventriküler ve interventriküler mekanik gecikme, diyastol sonu sol ventrikül
volümü, sistolik mitral anuler çap ve transmitral basınç gradiyenti ile
iliĢkili
bulunmuĢtur.
Bağımsız belirleyiciler ise sol ventrikül içindeki mekanik gecikme ve mitral
anuler sistolik çaptır.
Sonuç olarak sol ventrikül sistolik disfonksiyonu ve fonksiyonel mitral
yeersizliği olan hastalarda egzersizle mitral yetersizliği Ģiddeti artabilir veya
azalabilir. ÇalıĢmanın subgrup analizinde bazal sol ventrikül dissenkronisi olan
grupta
egzersiz ile birlikte mitral yetersizliği derecesinde %20 hastada artma
41
meydana gelmiĢ, hiçbir hastada azalma meydana gelmemiĢtir. Ancak bazal sol
ventrikül dissenkronisi olmayan hastalarda ise mitral yetersizliği derecesi ile sol
ventriül senkronisite arasında iliĢki saptanmamıĢtır. Bu hastaların 2/3 ‗ünde mitral
yetersizliği ERO azalmıĢ, 1/3‘ünde artmıĢtır.
Miyokardiyal asenkroninin sol ventrikülün ejeksiyon fazının etkinliğini
azalttığı ve mitral kapakların sistolde kapanması için uygulanan kuvvetin
zayıfladığı düĢünülmüĢtür. Bunun sonucunda fonksiyonel mitral yetersizliği
derecesi artmaktadır.
Bu fonksiyonel mitral yetersizliğindeki dinamik komponentin klinik bir
anlamı olabilir. Mitral yetersizliğinde egzersizin neden olduğu küçük değiĢimlerin
yada ERO daki düĢüĢlerin olduğu hastalarda daha iyi uzun dönem prognoz
beklenebilir. Bunun tersine egzersizle mitral yetersizliğinde anlamlı artıĢları olan
hastalarda
daha
sık
hastane
yatıĢı
beklenebilir.Bu
fonksiyonel
mitral
yetersizliğindeki tekrarlayan akut kötüleĢmeler sol atriyal ve sol ventriküler
yüklenmeye ve mortalitede artıĢa neden olabilir.
Ennezatın bahsedilen bu çalıĢmasında sadece istirahat halindeki asenkroni
değerlendirilmiĢtir. Halbuki kalp yetersizliği hastalarında egzersizle sol ventrikül
senkronisitesinin nasıl değiĢtiğini test eden çalıĢmalar mevcuttur(enneztat 9). Buna
göre bazı hastalarda egzersizle sol ventrikül senkronisitesi artarken bazı hastalarda
tam tersine asenkroni belirginleĢmektedir.
Bu nedenle bazal asenkronisi olmayan hastalarda, mitral yetersizliğindeki
azalma ve artmanın, baĢlangıçta olmayan ancak egzersizle geliĢen ―dinamik
asenkroniden” kaynaklanıp kaynaklanmadığı önemli bir soru iĢareti yaratmaktadır.
GEREÇ VE YÖNTEMLER
Hasta seçimi:
ÇalıĢmaya pacemaker implantasyonu yapılmıĢ 24 hasta dahil edildi( erkek:11
kadın:13). Hastaların %35 inde DDD, %56 sında VVI , %9 da VDD pacemaker
mevcut idi. Hastaların demografik verileri tablo 3 da gösterilmiĢtir. Pacemaker
takılma endikasyonları tam AV blok(%70), hasta sinus sendromu(%20) ve yavaĢ
ventrikül yanıtlı atriyal fibrilasyon (%10) idi. 3 hastanın NYHA ya göre
42
fonksiyonel kapasitesi 2 , geri kalanı 1 idi. 7 hasta angiotensin reseptör blokeri , 2
hasta ace inhibitörü, 3 hasta ise betabloker alıyordu.
ÇalıĢma protokolü:
Tüm hastalara bazal durumda ekokardiyografi uygulandı ( vivid 7, VingmedGeneral Electric, Horten, Norway) . 3V probe kullanılarak apikal 4 boĢluk, 2 boĢluk
ve apikal uzun aks görüntüleri eĢ zamanlı olarak alındı. En az 3 kardiyak siklus
uzunluğundaki görüntüler off-line analiz yapabilmek için kayıt edildi. Aortik ve
mitral kapakların açılma ve kapanma zamanlarının iĢaretlenebilmesi için mitral
inflow ve sol ventrikül çıkım yolundan pulse-wave doppler ile görüntüler alındı.
Pacemaker hızları bazalden baĢlayarak 20 vuru/dk intervallerle ve 5‘er dakika ara
ile artırıldı. Her hız artırımı sonunda ekokardiyografik kayıtlar tekrarlandı.
Ekokardiyografi:
Ekokardiyografik analiz için 3V probe ile eĢzamanlı apikal 4 boĢluk,2 boĢluk ve 3
boĢluk görüntüler alındı. Mümkün olan en yüksek frame oranını elde etmek için
sektör açısı ve derinlik ayarlandı. Ekokardiyografik ölçümlerde zamanlamanın net
olarak değerlendirilebilmesi için EKG traselerinin düzgün olması sağlandı.Off-line
analiz için en az 3 kardiyak siklus TVI modunda kaydedildi. Kaydedilen görüntüler
EchoPAC ile analiz edildi (EchoPAC PC-SWonly,version 6.0.0, Vingmed-General
Electric). Sol ventrikül volümleri, ejeksiyon fraksiyonu ve kardiyak output ölçümü
apikal 4 boĢluk ve 2 boĢluk görüntülerden biplane simpson yöntemi ile yapıldı.
Doku senkronizasyon görüntüleme(TSI) ve tissue tracking (TT) ölçümleri için
EchoPAC‘e kaydedilen TVI dataları kullanıldı. TSI için renk skalası en erken
aktive olan bölgede yeĢil en geç aktive olan bölgede kırmızı renk kodu ile
kodlanmıĢtı. Sol ventrikül çıkımyolundan alınan doppler trasesinden aortik kapak
açılma ve kapanma zamanları iĢaretlendi. TSI incelemesi için 3V prob ile alınan
görüntülerde off-line olarak 6 bazal ve 6 mid segment iĢaretlendi. Sonuçlar Septallateral gecikme, septal-posterior gecikme, bazal segmentler arası maksimum
gecikme, bazal segmentler arası standart sapma, tüm segmentler arası maksimum
gecikme ve tüm segmentler arası standart sapma değerleri olarak kaydedildi. TT ile
43
yapılan değerlendirme sonucunda 6 bazal ve 6 mid segmente örneklem
yerleĢtirilerek QRS baĢından miyokardiyal pik sistolik yer değiĢime(displacement)
kadar geçen zaman ölçüldü ve elde edilen değerlerin standart sapması alındı.
BULGULAR
ÇalıĢmaya kalıcı pacemaker implantasyonu uygulanmıĢ 24 hasta dahil edildi.
Hastaların demografik bilgileri tablo 3 de gösterilmiĢtir.
Tablo 3: Demografik bilgiler
HASTA( n:24)
YaĢ………………………………………………………60,95±20,94
Cinsiyet(E/K)…..………………………………………..10/14
Ritm( AF/ SR)…………………………………………...2/22
Pacemaker tipi
DDD……………………………………………………..6
VDD……………………………………………………..2
VVI……………………………………………...............16
Pacemaker endikasyonları
Tam AV blok………………………………….................17
Hasta sinus sendromu…………………………………....5
YavaĢ ventrikül yanıtlı AF……………………………....2
Ortalama ventriküler pacing yüzdesi…………………….72,8±37,7
NYHA sınıf………………………………………………1,13±0,34
44
DOKU SENKRONĠZASYON GÖRÜNTÜLEME(TSI) VE TĠSSUE
TRACKĠNG(TT) YÖNTEMLERĠ ĠLE DĠSSENKRONĠNĠN ARTAN
PACEMAKER HIZLARI ĠLE DEĞĠġĠMĠ
DeğiĢimler %20 lik değiĢim miktarına göre değerlendirildi. %20 eĢik değer
asenkroni değerlendirme yöntemlerinin kendi içerisindeki variabilite nedeni ile
sonuçların güvenli olması açısından alınmıĢtır. Asenkroni değerleri %20 nin
üzerinde artanlar artma, %20 lik değiĢim içerisindekiler değiĢmeme, %20 den fazla
azalanlar azalma olarak sınıflandırıldı. Buna göre tissue tracking ve TSI ile yapılan
ölçümler aĢağıda gösterilmiĢtir.
TT ile asenkroni değişimi
Tissue tracking ile yapılan değerlendirmede hastaların %48‘inde artan pacemaker
hızları ile asenkroni değerleri azalmıĢ,%8 hastada değiĢmemiĢ, %44 hastada ise
artıĢ göstermiĢtir.
12 hastada asenkroni
azalıyor
10 hastada asenkroni
artıyor
2 hastada asenkroni
değiĢmiyor
45
Tablo 4: TT ile 12 segment SD (time to peak displacement)
Dissenkroni değiĢimi
Azalma
Değişmeme
Artma
hasta sayısı
12(%48)
2 (%8)
11(%44)
TSI ile dissenkroni değişimi
Tablo 5: TSI ile değerlendirilen dissenkroni paremetreleri
Dissenkroni değiĢimi
s-l
s-p
BMD
BSD
ASMD ASSD
Azalma(n,%)
15(%65) 15(%65) 13(%56) 12(%52) 13(%56) 13(%56)
DeğiĢmeme(n,%)
2(%8)
0(%0)
3(%13) 4(%17) 8(%34) 7(%30)
Artma(n,%)
7(%27) 9(%35) 8(%31) 8(%31) 3(%10) 4(%14)
s-l: septolateral gecikme, s-p:septal-posterior gecikme, BMD: bazal segmentler
arası maksimum gecikme, BSD: bazal segmentler arası gecikmelerin standart
sapması, ASMD: 12 segment arası maksimum gecikme, ASSD: 12 segment time to
peak velositelerin standart sapması
TSI ile değerlendirildiğinde hastaların dissenkroni değerleri artan pacemaker hızları
ile her üç yönde değiĢim göstermekteydi. Ayrıca kiĢiler arasındaki bu büyük
farklılıkların yanı sıra, aynı kiĢinin değiĢik TSI paremetreleri kullanılarak
değerlendirilmesiyle de kiĢi içerisinde de farklı sonuçlar ortaya çıkmaktadır. 6
parametre birbiriyle karĢılaĢtırıldığında (septolateral gecikme, septal-posterior
gecikme, bazal segmentler arası maksimum gecikme, bazal segmentler arası
gecikmelerin standart sapması, 12 segment arası maksimum gecikme, 12 segment
time to peak velositelerin standart sapması) hastaların yalnızca %34 ünde tüm
paremetreler aynı yönde değiĢim göstermektedir. Hastaların büyük bir kısmında,
aynı olguda, bazı TSI parametrelerine göre dissenkronide artma, bazı parametrelere
göre değiĢmeme ve bazılarına görede azalma izlenebilmektedir(tablo 6).
46
TSI ile değerlendirilen parametrelere göre dissenkroni değiĢiminin eğilim eğrileri
gösterilmektedir.
47
Tablo 6: Farklı TSI parametreleri ve TT( sağ sütun) ile hastalardaki dissenkroni
değiĢimi
hasta
s-l
s-p
BazMD
Baz-SD
ASMD
AS-SD
TT-ASSD
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
19
20
21
22
23
24
Tablo 6: TSI
kökenli 6 değiĢik değerlendirme yöntemi ve TT ile
değerlendirildiğinde artan pacemaker hızları ile dissenkroni değiĢimi; kırmızı
renkler dissenkroninin azaldığını , sarılar değiĢmediğini, maviler ise arttığını
göstermektedir. (s-l: septolateral gecikme, s-p:septal-posterior gecikme, bazMD:
bazal segmentler arası maksimum gecikme, BazSD: bazal segmentler arası
gecikmelerin standart sapması, ASMD: 12 segment arası maksimum gecikme,
ASSD: 12 segment time to peak velositelerin(TT için displacement) standart
sapması)
48
SOL VENTRĠKÜL HEMODĠNAMĠK PARAMETRELERĠ
Tablo 7: Volümetrik ölçümlerin bazal ve peak kalp hızlarında karşılaştırması
Bazal
Peak
Test
Ort±SD
Ort±SD
p:
EF
52,28±17,49
52,70±12,12
t:-0,155; p:0,879
SVDSÇ
48,08±5,49
46,87±4,21
t:2,303; p:0,031*
SVSSÇ
34,00±5,17
33,41±5,38
t:0,634;p:0,533
SVDSV
75,82±28,85
63,30±30,07
t:3,841; p:0,001**
SVSSV
35,69±24,53
31,56±21,30
t:2,065; p:0,05*
CO
2,53±0,81
4,44±1,31
t:-10,243; p:0,001**
AOTVI
23,39±8,26
14,27±6,66
t:11,529; p:0,001**
t : Paired samples t test
*p<0.05 **p<0.01
EF: Ejeksiyon fraksiyonu, svdsç: sol ventrikül diyastol sonu çap, SVSSÇ: sol
ventrikül sistol sonu çap ,SVDSV: sol ventrikül diyastol sonu volüm, SVSSV:sol
ventrikül sistol sonu volüm,
CO:kardiyak output , AOTVI: aortik hız zaman
integrali
EF ölçümlerinin bazal ve peak arasındaki farklılığı istatistiksel olarak
anlamlı bulunmamıĢtır (p>0,05); olguların % 65,2‘sinde düĢüĢ görülmüĢ; % 30,4‘ü
yükselmiĢ ve % 4,3‘ü ise aynı kalmıĢtır.
49
LVEDD ölçümleri ise bazale göre peak dönemde istatistiksel olarak anlamlı
düzeyde düĢüĢ göstermiĢlerdir (p<0,05); olguların % 62,5‘inde düĢüĢ; % 16,7‘sinde
yükseliĢ görülmüĢ % 20,8‘i aynı kalmıĢtır.
LVESD ölçümleri arasında fark istatistiksel olarak anlamlı değildir
(p>0,05); olguların % 41,7‘sinde düĢüĢ; % 45,8‘sinde yükseliĢ görülmüĢ % 12,5‘i
aynı kalmıĢtır.
Bazal ile peak dönemde alınan LVEDV ölçümleri arasındaki fark
istatistiksel olarak ileri düzeyde anlamlı bulunmuĢtur (p<0,01); bazale göre peak
ölçümlerde anlamlı düĢüĢ görülmektedir; olguların % 73,9‘unda düĢüĢ; %
21,7‘sinde yükseliĢ görülmüĢ % 4,3‘ü aynı kalmıĢtır.
LVESV ölçümlerinin de bazale göre peak dönemde gösterdiği düĢme
istatistiksel olarak sınırda anlamlı farklılık göstermektedir (p<0,05); olguların %
65,2‘sinde düĢüĢ; %34,8‘inde yükseliĢ görülmüĢtür.
CO ölçümlerinde bazale göre peak dönemde görülen yükseliĢ istatistiksel
olarak ileri düzeyde anlamlı bulunmuĢtur (p<0,01); olguların % 100‘ünde yükseliĢ
görülmüĢtür.
AOTVI ölçümlerinde yine bazale göre peak dönemde görülen düĢüĢ
yönündeki değiĢim istatistiksel olarak ileri düzeyde anlamlıdır (p<0,01). olguların
% 96‘sında düĢüĢ; %4‘ünde yükseliĢ görülmüĢtür.
Tablo 8: EF sınıflamasına göre volümetrik ölçümlerin bazal ve peak
karşılaştırması
Bazal
Peak
Test
Ort±SD
Ort±SD
p:
EF
46,14±16,45
42,68±10,45
Z:-1,183; p:0,237
LVEDD
51,00±7,07
49,42±5,59
Z:-1,633; p:0,102
LVESD
36,42±4,79
38,71±4,49
Z:-1,524; p:0,128
LVEDV
93,28±41,91
82,85±41,93
Z:-2,197; p:0,028*
LVESV
51,85±37,94
48,14±30,22
Z:-0,762; p:0,446
EF DüĢük
(n=7)
50
CO
2,51±0,94
4,77±1,69
Z:-2,366; p:0,018*
AOTVI
20,01±3,01
10,80±2,36
Z:-2,366; p:0,018*
EF
54,97±17,75
57,09±10,21
t:-0,578; p:0,572
LVEDD
46,88±4,40
45,82±3,12
t:1,550; p:0,141
EF
LVESD
33,00±5,12
31,23±4,08
t:1,694; p:0,110
Normal
LVEDV
68,18±17,71
54,75±19,15
t:2,965; p:0,010*
(n=18)
LVESV
28,62±11,47
24,31±10,65
t:2,008; p:0,063
CO
2,54±0,78
4,29±1,14
t:-8,134; p:0,001**
AOTVI
24,70±9,31
15,62±7,34
t:8,364; p:0,001**
Z: Wilcoxon Signed rank test
t: Paired samples test
* p<0.05
** p<0.01
EF DÜŞÜK OLGULARDA;
EF ölçümlerinin bazal ve peak arasındaki farklılığı istatistiksel olarak
anlamlı bulunmamıĢtır (p>0,05). LVEDD ölçümleri ve LVESD ölçümleri de bazal
ile peak arasında anlamlı farklılık göstermemektedir (p>0,05).
Bazal ile peak dönemde alınan LVEDV ölçümleri arasındaki fark
istatistiksel olarak anlamlı bulunmuĢtur (p<0,05). LVESV ölçümleri de bazal ile
peak arasında anlamlı farklılık göstermemektedir (p>0,05).
CO ölçümlerinde bazale göre peak dönemde görülen yükseliĢ istatistiksel
olarak anlamlı bulunmuĢtur (p<0,05); AOTVI ölçümlerinde yine bazale göre peak
dönemde görülen düĢüĢ yönündeki değiĢim istatistiksel olarak anlamlıdır (p<0,05).
EF NORMAL OLGULARDA;
51
EF ölçümlerinin bazal ve peak arasındaki farklılığı istatistiksel olarak
anlamlı bulunmamıĢtır (p>0,05). LVEDD ölçümleri ve LVESD ölçümleri de bazal
ile peak arasında anlamlı farklılık göstermemektedir (p>0,05).
Bazal ile peak dönemde alınan LVEDV ölçümleri arasındaki fark
istatistiksel olarak anlamlı bulunmuĢtur (p<0,05). LVESV ölçümleri de bazal ile
peak arasında anlamlı farklılık göstermemektedir (p>0,05).
CO ölçümlerinde bazale göre peak dönemde görülen yükseliĢ istatistiksel
olarak ileri düzeyde anlamlı bulunmuĢtur (p<0,01); AOTVI ölçümlerinde yine
bazale göre peak dönemde görülen düĢüĢ yönündeki değiĢim istatistiksel olarak
ileri düzeyde anlamlıdır (p<0,01).
Tablo
9:
Asenkroniye
göre
hemodinamik
ölçümlerin
bazal
ve
peak
karşılaştırması
Bazal
Peak
Test
Ort±SD
Ort±SD
p:
EF
56,75±13,65
53,59±14,13
Z:-0,676; p:0,499
LVEDD
45,28±4,68
45,71±3,09
Z:-0,736; p:0,461
LVESD
31,71±4,71
32,71±5,64
Z:0,850; p:0,395
LVEDV
70,85±13,93
55,71±19,31
Z:-2,197; p:0,028*
LVESV
30,71±12,28
27,85±12,25
Z:-1,101; p:0,271
CO
2,55±0,90
4,23±1,19
Z:-2,366; p:0,018*
AOTVI
21,61±4,81
12,60±2,93
Z:-2,366; p:0,018*
EF
50,33±18,99
52,32±11,62
t:-0,557; p:0,586
LVEDD
49,23±5,50
47,35±4,59
t:3,108; p:0,007**
LVESD
34,94±5,18
33,70±5,41
t:1,015; p:0,325
LVEDV
78,00±33,57
66,62±33,74
t:3,110; p:0,007**
Asenkroni
Artan
olgular
Asenkroni
Azalan
olgular
52
37,87±28,38
33,18±24,41
CO
2,53±0,80
4,53±1,39
t:-8,652; p:0,001**
AOTVI
24,08±9,29
14,92±7,62
t:9,524; p:0,001**
LVESV
t:1,747; p:0,101
Z: Wilcoxon Signed rank test
t: Paired samples test
*
p<0.05
**
p<0.01
Asenkroni artan olgularda;
EF ölçümlerinin bazal ve peak arasındaki farklılığı istatistiksel olarak
anlamlı bulunmamıĢtır (p>0,05). LVEDD ölçümleri ve LVESD ölçümleri de bazal
ile peak arasında anlamlı farklılık göstermemektedir (p>0,05).
Bazal ile peak dönemde alınan LVEDV ölçümleri arasındaki düĢme
yönündeki fark istatistiksel olarak anlamlı bulunmuĢtur (p<0,05); LVESV
ölçümleri de bazal ile peak arasında anlamlı farklılık göstermemektedir (p>0,05).
CO ölçümlerinde bazale göre peak dönemde görülen yükseliĢ istatistiksel
olarak anlamlı bulunmuĢtur (p<0,05); AOTVI ölçümlerinde yine bazale göre peak
dönemde görülen düĢüĢ yönündeki değiĢim istatistiksel olarak anlamlıdır (p<0,05).
Asenkroni azalan olgularda;
EF ölçümlerinin bazal ve peak arasındaki farklılığı istatistiksel olarak
anlamlı bulunmamıĢtır (p>0,05). LVEDD ölçümlerinde bazale göre peak
ölçümlerde görülen düĢüĢ istatistiksel olarak ileri düzeyde anlamlı bulunmuĢtur
(p>0,05).
LVESD
ölçümleri
bazal
ile
peak
arasında
anlamlı
farklılık
göstermemektedir (p>0,05).
Bazal ile peak dönemde alınan LVEDV ölçümleri arasındaki düĢme
yönündeki fark istatistiksel olarak ileri düzeyde anlamlı bulunmuĢtur (p<0,01).
LVESV ölçümleri de bazal ile peak arasında anlamlı farklılık göstermemektedir
(p>0,05).
53
CO ölçümlerinde bazale göre peak dönemde görülen yükseliĢ istatistiksel
olarak ileri düzeyde anlamlı bulunmuĢtur (p<0,01); AOTVI ölçümlerinde yine
bazale göre peak dönemde görülen düĢüĢ yönündeki değiĢim istatistiksel olarak
ileri düzeyde anlamlıdır (p<0,01).
Ġstatistiksel Ġncelemeler
Ġstatistiksel analizler için SPSS (Statistical Package for Social Sciences) for
Windows 10.0 programı kullanıldı. ÇalıĢma verileri değerlendirilirken tanımlayıcı
istatistiksel metodların (Ortalama, Standart sapma) yanısıra normal dağılım
gösteren parametrelerin grup içi karĢılaĢtırmalarında paired sample t testi, normal
dağılım göstermeyen parametrelerin grup içi karĢılaĢtırmalarında ise Wilcoxon
Signed Rank testi kullanıldı. Sonuçlar % 95‘lik güven aralığında, anlamlılık p<0.05
düzeyinde değerlendirildi.
TARTIġMA
Kalıcı pacemaker implantasyonu yapılmıĢ hastalarda artan kalp hızları sol ventrikül
dissenkronisinde önemli değiĢiklikler meydana getirebilir. Bazı hastalarda
dissenkronide artma meydana gelirken ,bazı hastalarda anlamlı değiĢiklik
izlenmiyor, bazı hastalarda ise sol ventrikül dissenkronisi önemli bir biçimde
azalıyor. Sol ventrikül ejeksiyon fraksiyonu düĢük olan veya normal olan gruplar
arasında da artan pacemaker hızlarında dissenkroni değiĢimi arasında önemli bir
fark izenmedi. Her iki hasta grubunda da bazı olgularda asenkroni artarken,
bazılarında azalıyor veya değiĢmiyordu. Hastalar arası yanıtta izlenen bu önemli
fark yanında, aynı hastanın aynı inceleme yönteminden köken alan farklı
metodlarla( TSI kaynaklı, septolateral gecikme, septal posterior gecikme, bazal
maksimal gecikme, bazal gecikmelerin standart sapması, 12 segment maksimal
gecikme ve 12 segment gecikmelerin standart sapması) farklı değiĢimlerinin
izlenmesi
kullanılacak
yöntemin
yöntemin
güvenilirliği
veya
dissenkroni
değerlendirilmesinde
hangisi olduğu konusunda önemli soru
iĢaretleri
54
oluĢturmaktadır. Yapılan bu çalıĢmada TSI ile hastaların ancak %34 lük bir
kısımında tüm TSI parametreleri ile aynı yönde bir değiĢim izleniyor. Önemli bir
hasta grubunda bir metodla asenkroni azalıyor gibi görünürken, bir baĢka metodla
asenkronide belirgin artma izlenebiliyor
Sorunlar
Farklı ekokardiografik değerlendirme yöntemleri arasında dissenkroni
değiĢimi açısından farklı sonuç(bizim çalıĢmamızda TT-TSI arası fark)
Aynı ekokardiografik teknikden köken alan farklı değerlendirme metodları
arasında farklı sonuç (bizim çalıĢmamızda TSI ile septolateral gecikme,
septal posterior gecikme, bazal maksimal gecikme, bazal gecikmelerin
standart sapması, 12 segment maksimal gecikme ve 12 segment
gecikmelerin standart sapması)
Lafitte ve arkadaĢlarını yaptığı çalıĢmada sol ventrikül sistolik fonksiyonarı normal
yada azalmıĢ olan olgularda egzersiz ile dissenkroni değiĢimi araĢtırılmıĢtır. Bu
araĢtırmada doku doppler inceleme ve strain görüntüleme ile asenkroni
değerlendirilmiĢtir. Özellikle kalp yetersizliği olan hasta grubunda egzersizle
hastaların %34 ünde asenkronide %20 ve üzerinde artıĢ, %37 sinde değiĢmeme,
%29 unda ise %20 nin üzerinde azalma izlenmiĢtir. Sol ventrikül sistolik
fonksiyonları normal olan hasta grubunda egzersizle asenkronide önemli bir
değiĢim izlenmemiĢtir. Aynı çalıĢmada, değerlendirme parametrelerine göre (
septal ve lateral segmentlerin maksimal velositeye ulaĢmaları arasındaki fark, 12
segmentin maksimal velositeye ulaĢma sürelerinin standart sapması, 6 bazal
segmentin maksimal velositeye ulaĢma süreleri arası maksimal fark, 6 bazal
segmentde segmental kontaksiyona kadar geçen süreler arası maksimal fark, strain
ile gecikmiĢ longitüdinal kontraksiyon gösteren segment yüzdesi) farklı sonuçlar
elde edilmiĢtir. Hastaların yalnızca %37 sinde tüm parametreler ile dissenkroni
gösterilirken,%14 ünde hiçbir parametre ile dissenkroni gösterilmemiĢ, %49
hastada bazı parametrelerle dissenkroni mevcut gibi görünürken bazılarıyla ise yok
gibi değerlendirilmiştir.
Özellikle kardiyak resenkronizasyon tedavisi(KRT) yapılan hastalarda bazal
dissenkroni ne kadar belirgin ise KRT sonrası remodeling o kadar belirgin
55
olmaktadır. Murphy ve arkadaĢlarının yaptığı bir çalıĢmada en fazla klinik ve
hemodinamik fayda “en geç aktive olan miyokard segmenti” pace edilirse
sağlanıyor. Maksimal geciken segmentden 1 segment uzak bir bölge pace edilirse
orta derecede bir fayda, birden fazla segment uzaklıktaki bir alan pace edilirse
anlamlı bir fayda izlenmiyor.
vardığını
düĢünecek
olursak,
KRT‘ye cevapsızlığın bazı serilerde %40 lara
teorik
olarak,
dissenkroniyi
değerlendirme
yöntemlerinin birbirinden farklı sonuçlar vermesi, KRT ye aday hastanın seçiminde
sorunlara neden olarak cevapsızlığın bir nedenini oluĢturabilir.
Ayrıca teorik olarak, artan pacemaker hızları ile bazı hastalarda asenkroninin
artıyor olması uzun dönemde bu hasta grubunda olumsuz kardiyak sonuçlara neden
olabilir.
ÇalıĢmamızda artan pacemaker hızları ile birlikte sol ventrikül hemodinamik
parametreleri değerlendirildiğinde, artan hızlarla birlikte sol ventrikül ejeksiyon
fraksiyonunun değiĢmediği, sol ventrikül diyastol sonu çap, diyastol ve sistol sonu
volüm ile aortik hız zaman integralinin anlamlı ölçüde azaldığı, kardiyak outputun
ise anlamlı ölçüde arttığı saptanmıĢtır. Ancak sol ventrikül ejeksiyon fraksiyonu
normal yada azalmıĢ olan gruplar arasında, yada sol ventrikül dissenkronisi artan
yada azalan gruplar arasında bu bahsedilen parametreler açısından anlamlı bir fark
izlenmemiĢtir.
56
KAYNAKLAR
1.
Theodore C. Chan, MD*, Taylor Y. Cardall, MD; Electronic Pacemakers,
Emerg Med Clin N Am 24 (2006) 179–194
2.
Baldasseroni S, Opasich C, Gorini M, et al. Left bundle-branch block is
associated with increased 1-year sudden and total mortality rate in 5517
outpatients with congestive heart failure: A report from the Italian Network on
Congestive Heart Failure. Am Heart J 2002; 143:398–405.
3.
Shamim W, Francis DP, Yousufuddin M, et al. Intraventricular conduction
delay: A prognostic marker in chronic heart failure. Int J Cardiol 1999; 70:171–178.
4.
Grines CL, Bashore TM, Boudoulas H, et al. Functional abnormalities in
isolated left bundle-branch block. The effect of interven- tricular asynchrony.
Circulation 1989; 79:845–853.
5.
Xiao HB, Lee CH, Gibson DG. Effect of left bundle-branch block on
diastolic function in dilated cardiomyopathy. Br Heart J 1991; 66:443–447.
6.
Xiao HB, Roy C, Fujimoto S, et al. Natural history of abnormal conduction
and its relation to prognosis in patients with dilated cardiomyopathy. Int J Cardiol
1996; 53:163–170.
7.
Ozdemir K, Altunkeser BB, Danis G, et al. Effect of the isolated left
bundle branch block on systolic and diastolic functions of left ventricle. J
Am Soc Echocardiogr 2001; 14:1075–1079
8.
Lee SJ, McCulloch C, Mangat I, Foster E, De Marco T, Saxon LA. Isolated
bundle branch block and left ventricular dysfunction. J Card Fail 2003; 9:87–92
9.
Littman L, Symanski JD. Hemodynamic implications of left bundle bransh
block. J Electrocardiol 2000; 33(suppl.): 115-121
10.
Shenkman HJ, Pampati V, Khandelwal AK, et al. Congestive heart failure
and QRS duration: Establishing prognosis study. Chest 2002; 122:528–534.
11.
Hesse B, Diaz LA, Snader CE, et al. Complete bundle branch block as an
independent predictor of all-cause mortality: Report of 7,073 patients referred for
nuclear exercise testing. Am J Med 2001;
12.
Daubert JC, Ritter P, Le Breton H, et al. Permanent left ventricular pacing
with transvenous leads inserted into the coronary veins. Pacing Clin Electrophysiol
1998; 21:239–245.
57
13.
Cazeau S, Leclercq C, Lavergne T, et al. for the MUSTIC Study
Investigators. Effects of multisite biventricular pacing in patients with heart failure
and intraventricular conduction delay. N Engl J Med 2001; 344:873–880.
14.
Abraham WT, Fisher WG, Smith AL, et al. for the MIRACLE study group
Cardiac resynchronization in chronic heart failure. N Engl J Med 2002; 346:1845–
1853.
15.
Gerber TC, Nishimura RA, Holmes DR, et al. Left ventricular and
biventricular pacing in congestive heart failure. Mayo Clin Proc 2001; 76:803–812
16.
Young JB, Abraham WT, Smith AL, et al. for the MIRACLE ICD
Trial Investigators. Combined cardiac resynchronization and implantable
cardioversion defibrillation in advanced chronic heart failure. The MIRACLE
ICD Trial. JAMA 2003; 289:2685– 2694.
17.
Leclercq C, Kass DA. Retiming the failing heart: Principles and current
clinical status of cardiac resynchronization. J Am Coll Cardiol 2002; 39:194–
201.
18.
Linde C, Leclerq C, Rex S, et al. (MUSTIC Study Group). Long- term
benefits of biventricular pacing in congestive heart failure: Results from the
Multisite Stimulation In Cardiomyopathy (MUS- TIC) Study. J Am Coll Cardiol
2002; 40:111–118.
19.
Linde C, Braunschweig F, Gadler F, Bailleul C, Daubert J-C. Long- term
improvement in quality of life by biventricular pacing in patients with chronic heart
failure: Results from the MUSTIC study. Am J Cardiol 2003; 91:1090–1095
20.
Puererfellner H, Nesser HJ, Winter S, et al. for the EASYTRAK Clinical
Investigation Study Group and the European EASYTRAK Registry. Transvenous
left ventricular lead implantation with the EASYTRAK lead system: The European
experience. Am J Cardiol 2000; 86:157K–164K.
21.
Alonso C, Leclercq C, Revault d‘Allonnes F, et al. Six year experience of
transvenous left ventricular lead implantation for permanent biventricular pacing in
patients with advanced heart failure: Technical aspects. Heart 2001; 86:405–410.
22.
Manolis AS. Cardiac resynchronization therapy in congestive heart
failure: Ready for prime time? Heart Rhythm 2004; 1:355– 363.
58
23.
Bradley DJ, Bradley EA, Baughman KL, et al. Cardiac resynchronization and death from progressive heart failure. A meta-analysis of
randomized controlled studies. JAMA 2003; 289:730-740.
24.
Bristow MR, Saxon LA, Boehmer J, et al., for the COMPANION
Investigators. Cardiac resynchronization therapy with or without
implantable defibrillator in advanced chronic heart failure. N Engl J Med
2004; 350:2140-2150.
25.
McAllister FA, Ezekowitz JA, Wiebe N, et al. Systematic review:
Cardiac resynchronization in patients with symptomatic heart failure.
Ann Intern Med 2004; 141:381-390.
26.
Cleland JGF, Daubert J-C, Erdmann E, et al., for the CARE-HF
Study Investigators. The effect of cardiac resynchronization or morbidity
and mortality in heart failure. N Engl J Med 2005; 352:1539-1549.
27.
Tanabe A, Mohri T, Ohga M, et al. The effects of pacing-induced left
bundle branch block on left ventricular systolic and diastolic performances.
Jpn Heart J 1990; 31:309-317.
28.
Modena MG, Mattioli AV, Mattioli G. Right ventricular pacing and
left ventricular filling pattern: An echo-Doppler study. Chest 1991;
100:744-747.
29.
Tantengco MVT, Thomas RL, Karpawich PP. Left ventricular
dysfunction after long-term right ventricular apical pacing in the
young. J Am Coll Cardiol 2001; 37:2093.
30.
Karpawich PP, Rabah R, Haas JE. Altered cardiac histology
following apical right ventricular pacing in patients with congenital
atrioventricular block. Pacing Clin Electrophysiol 1999; 22:1372-1377.
31.
Thambo J-B, Bordachar P, Garrigue S, et al. Detrimental ventricular
remodeling in patients with congenital complete heart block and chronic
right ventricular apical pacing. Circulation 2004; 110:3766-3772.
32.
Tse H-F,Yu C, Wong K-K, et al. Functional abnormalities with
permanent right ventricular pacing. J Am Coll Cardiol 2002; 40:1451-1458
59
33.
Hamdan MH, Zagrodzky JD, Joglar JA, et al. Biventricular pacing
decreases sympathetic activity compared with right ventricular pacing in
patients with depressed ejection fraction. Circulation 2000; 102:10271032
34.
Erol-Yilmaz A, Tukkie R, Schrama TAM, Romkes HJ, Wilde AAM.
Reversed remodeling of dilated left sided cardiomyopathy after upgrading
from VVIR to VVIR biventricular pacing. Europace 2002; 4:445-449.
35.
The DAVID Trial Investigators. Dual-chamber pacing or ventricular
backup pacing in patients with an implantable defibrillator: The dual
chamber and VVI implantable defibrillator (DAVID) trial. JAMA 2002;
285:3115-3123.
36.
Steinberg JS, Fischer A, Wang P, et al., for the MADIT II Investigators. The clinical implications of cumulative right ventricular pacing in
the
multicenter
automatic
defibrillator
trial
II.
J
Cardiovasc Electrophysiol 2005; 16:359-365
37.
PAVE Trial. American College of Cardiology Annual Scientifi
Session, March 2004.
38.
Daoud E, Doshi R, Fellows C, et al. Ablate and pace with cardiac
resynchronization therapy for patients with reduced ejection fraction: Subanalysis of PAVE study (Abstract 181). Heart Rhyth 2004; 1(suppl.):S59.
39.
Thackray SDR, Witte KKA, Nikitin NP, Clark AL, Kaye GC,
Cleland JGF. The prevalence of heart failure and asymptomatic left
ventricular dysfunction in a typical regional pacemaker population. Eur
Heart J 2003; 24:1143-1152.
40.
O‘Keefe JH, Abuissa H, Jones PG, et al. Effect of chronic right ventricular apical pacing on left ventricular function. Am J Cardiol 2005;
95:771-773.
41.
Ueng K-C, Tsai T-P, Tsai C-F, et al. Acute and long-term effects of
atrioventricular junction ablation and VVIR pacemaker in symp-tomatic
patients with chronic lone atrial fibrillation and normal ventricular
response. J Cardiovasc Electrophysiol 2001; 12:303-309.
60
42.
Blanc J-J, Etienne Y, Gilard M, et al. Evaluation of different ventricular pacing sites in patients with severe heart failure: Results of an
acute hemodynamic study. Circulation 1997; 96:3273-3277.
43.
De Cock CC, Giudici MC, Twisk JW. Comparison of the haemodynamic effects of right ventricular outflow-tract pacing with right
ventricular apex pacing: A quantitative review. Europace 2003; 5:275278.
44.
Cowell R, Morris-Thurgood J, Ilsley C. Septal short atrioventric-ular
delay pacing: Additional hemodynamic improvements in heart failure.
Pacing Clin Electrophysiol 1994; 17(Pt II):1980-1983.
45.
Giudici MC, Thornburg GA, Buck DL, et al. Comparison of right
ventricular outflow tract and apical lead permanent pacing on cardiac
output. Am J Cardiol 1997; 79:209-212.
46.
Buckingham TA, Candinas R, Schlaepfer J, et al. Acute
hemodynamic effects of atrioventricular pacing at different sites in the
right ventricle individually and simultaneously. Pacing Clin Elec-trophysiol
1997; 20(Pt I):909-915.
47.
Karpawich PP, Mital S. Comparative left ventricular function
following atrial, septal, and apical single chamber heart pacing in the young.
Pacing Clin Electrophysiol 1997; 20(Pt I):1983-1988.
48.
De Cock CC, Meyer A, Kamp O, Visser CA. Hemodynamic benefits of
right ventricular outflow tract pacing: Comparison with rightventricular
apex pacing. Pacing Clin Electrophysiol 1998; 21:536-541.
49.
Mera F, DeLurgio DB, Patterson RE, Merlino JD, Wade ME, Leon
AR. A comparison of ventricular function during high right ventricular
septal and apical pacing after His-bundle ablation for refractory atrial
fibrillation. Pacing Clin Electrophysiol 1999;22:1234-1239.
50.
Buckingham TA, Candinas R, Attenhofer C, et al. Systolic and
diastolic function with alternate and combined site pacing in the right
ventricle. Pacing Clin Electrophysiol 1998; 21:1077-1084.
51.
Victor F, Leclercq C, Mabo P, et al. Optimal right ventricular pacing
site in chronically implanted patients: A prospective random-ized
61
crossover comparison of apical and outflow tract pacing. J Am Coll
Cardiol 1999; 33:311-316.
52.
Schwaab B, Froehlig G, Alexander C, et al. Influence of right
ventricular stimulation site on left ventricular function in atrial
synchronous ventricular pacing. J Am Coll Cardiol 1999; 33:317-323.
53.
Kolettis TM, Kyriakides ZS, Tsiapras D, Popov T, Paraskevaides IA,
Kremastinos DT. Improved left ventricular relaxation during short-term
right ventricular outflow tract compared to apical pacing. Chest 2000;
117:60-64.
54.
Gold MK, Shorofsky SR, Metcalf MD, Feliciano Z, Fisher
ML,Gottlieb SS. The acute hemodynamic effects of right ventricular septal
pacing in patients with congestive heart failure secondary to ischemic or
idiopathic dilated cardiomyopathy. Am J Cardiol 1997; 79:179-681.
55.
Bourke JP, Hawkins T, Keavey P, et al. Evolution of ventricular
function during permanent pacing from either right ventricular apex or
outflow tract following AV-junctional ablation for atrialfibrillation.
Europace 2002; 4:219-228.
56.
Kass DA, Chen CH, Curry C, et al. Improved left ventricular
mechanics from acute VDD pacing in patients with dilated cardiomyopathy and ventricular conduction delay. Circulation 1999;99:15671573.
57.
Yu C-M, Lin H, Fung W-H, Zhang Q, Kong S-L, Sanderson JE.
Comparison of acute changes in left ventricular volume, systolicand
diastolic functions, and intraventricular synchronicity after biventricular
and right ventricular pacing for heart failure. Am Heart J 2003; 145:e23
(G1-G7)
58.
Leclercq C, Walker S, Linde C, et al. on behalf of the MUSTIC
study group. Comparative effects of permanent biventricular and rightuniventricular pacing in heart failure patients with chronicatrial
fibrillation. Eur Heart J 2002; 23:1780-1787.
59.
Leon AR, Greenberg JM, Kanuru N, et al. Cardiac
resynchronization in patients with congestive heart failure and chronic
atrial fibrillation: Effect of upgrading to biventricular pacing after chronic
right ventricular pacing. J Am Coll Cardiol 2002; 39:1258-1263.
62
60.
Leclercq C, Cazeau S, Lellouche D, et al. Upgrading from right
ventricular pacing to biventricular pacing in previously paced patients
with advanced heart failure: A randomized controlled study. Presented at
the European Society of Cardiology Congress 2003; August 30-September
3, 2003; Vienna, Austria. Abstract 1965.
61.
Jais P, Takahashi A, Garrigue S, et al. Mid-term follow-up of
endocardial biventricular pacing. Pacing Clin Electrophysiol 2000; 23 (Pt
II):1744-1747
62.
Grosfeld MJW, Res JCJ, Vos DHS, de Boer TJM, Bos HJ. Testing a
new mechanism for left interventricular septal pacing: The transseptal
route: A feasibility and safety study. Europace 2002; 4:439-444.
63.
Stambler BS, Ellenbogen KA, Zhang X, et al. Right ventricular outflow
versus apical pacing in pacemaker patients with congestive heart failure
and atrial fibrillation. J Cardiovasc Electrophysiol 2003; 14:1180-1186
64.
Dixit S, Gerstenfeld EP, Callans DJ, Marchlinski FE.
Electrocardiographic patterns of superior right ventricular outflow tract
tachycardias: Distinguishing septal and free-wall sites of origin. J
Cardiovasc Electrophysiol 2003; 14:1-7.
65.
Josephson
ME,
Callans
DJ.
Using
the
twelve-lead
electrocardiogram to localize the site of origin of ventricular tachycardia.
Heart Rhythm 2005; 2:443-446.
66.
Res JCJ, Bokern MJJA, Vos DHS. Characteristics of bifocal pacing:
Right ventricular apex versus outflow tract: An interim analysis. PACE
2005; 28:S36-S38.
67.
Amitani S, Miyahara K, Sohara H, et al.Experimental His-bundle
pacing: Histopathological and electrophysiological examination.Pacing
Clin Electrophysiol 1999; 22 (Pt I):562-566.
68.
Deshmukh P, Casavant DA, Romanyshyn M, Anderson K. Permanent, direct His bundle pacing: A novel approach to cardiac pacing in
patients with normal His-Purkinje activation. Circulation 2000; 101:869877.
63
69.
Deshmukh PM, Romanyshyn M. Direct His-bundle pacing:
Present and future. Pacing Clin Electrophysiol 2004; 27 (Pt.II):862870.
70.
Vlay SC. Alternate site biventricular pacing: Bi-v in the RV-is there a
role?Pacing Clin Electrophysiol 2004; 27:567-569.
71.
Pachon JC, Pachon EI, Albornoz RN, et al. Ventricular endocardial
right bifocal stimulation in the treatment of severe dilated
cardiomyopathy heart failure with wide QRS. Pacing Clin Electrophysiol
2001; 24:1349-1376.
72.
Zamparelli L, Martiniello AR. Right ventricular bifocal DDD pacing
as primary choice for cardiac resynchronization in heart failure
patients with severe mitral regurgitation (Abstr). Heart Rhythm 2005;
2(Suppl.):S250.
73.
Daoud E, Doshi R, Fellows C, et al. Ablate and pace with cardiac
resynchronization therapy for patients with reduced ejection fraction: Subanalysis of PAVE study (Abstract 181). Heart Rhythm 2004; 1(suppl.):S59.
74.
Peschar M, de Swart H, Michels KJ, Reneman RS, Prinzen FW. Left
ventricular septal and apex pacing for optimal pump function in canine
hearts. J Am Coll Cardiol 2003; 41:1218-1226.
75.
Vanagt WY, Verbeek XA, Delhaas T, Mertens L, Daenen WJ,
Prinzen FW. The left ventricular apex is the optimal site for pediatric
pacing: Correlation with animal experience. Pacing Clin Electrophysiol
2004; 27:837-843.
76.
Garrigue S, Bordachar P, Reuter S, et al. Comparison of permanent
left ventricular and biventricular pacing in patients with heart failure
and chronic atrial fibrillation: Prospective haemodynamic study. Heart
2002; 87:529-534.
77.
Aonuma K, Yokoyama Y, Seo Y, et al. Tri-ventricular pacing: A
novel concept of resynchronization therapy for better left ventricular
performance in end-stage heart failure (Abstr). Heart Rhythm 2005;
2(Suppl.):S131.
78.
Uhley HN, Rivkin L. Peripheral distribution
Vconduction system. Am J Cardiol 1960; 5:688-691.
of the canine A-
64
79.
Esmond WG, Moulton GA, Cowley RA, et al. Peripheral ramification of
the cardiac conduction system. Circulation 1963;27:732-738.
80.
Myerburg RJ, Nilsson K, Gelband H. Physiology of canine
intraventricular conduction and endocardial excitation. Circ Res1972;
30:217-243.
81.
Abramson DI, Margolin S. A Purkinje conduction network in the
myocardium of the mammalian ventricles. J Anat 1936;70:251-259.
82.
Truex RC, Copenhaver WM. Histology of the moderator band in man and
other mammals with special reference to the conduction system. Am J Ana 1947;
80:173-200.
83.
Hoffman BF, Cranefield PF, Stuckley JH, et al. Direct measurement of
conduction velocity in in situ specialized conduction system of mammalian
heart. Proc Soc Exp Biol Med 1959;102:55-57.
84.
Scher AM, Young AC, Malmgreen AL, et al. Spread of electrical activity
through the wall of the ventricle. Circ Res 1953;1:539-547
85.
Scher AM, Young AC, Malmgren AL, et al. Activation of the
interventricular septum. Circ Res 1955; 3:56-64.
86.
Durrer D, van Dam RT, Freud GE, et al. Total excitation of the isolated
human heart. Circulation 1970; 41:899-912.
87.
Burchell HB, Essex HE, Pruitt RD. Studies on the spread of excitation
through the ventricular myocardium. Circulation 1952;6:161-171.
88.
Sodi-Pallares D, Rodriguez MI, Chait LO, et al. The activation of the
interventricular septum. Am Heart J 1951; 41:569-608.
89.
Sodi-Pallares D, Bisteni A, Medrano GA, et al. The activation of the free
left ventricular wall in the dog‘s heart. Am Heart J 1955;49:587-602.
90.
Spach MS, Barr RC. Ventricular intramular and epicardial potential
distributions during ventricular activation and repolarizationin the intact dog.
Circ Res 1975; 37:243-257.
65
91.
Torres MAR, Corday E, Meerbaum S, et al. Characterization of left
ventricular mechanical function during arrhythmias by two-dimensional
echocardiography. II Location of the site of onset of premature ventricular
systoles. J Am Coll Cardiol 1983;1:819-829.
92.
Wilson JR, Douglas P, Hickey WF, et al. Experimental congestive heart
failure produced by rapid ventricular pacing in the dog: Cardiac effects.
Circulation 1987; 75:857-867.
93.
Maurer G, Torres MA, Corday E, et al. Two-dimensional
echocardiographic contrast assessment of pacing-induced mitral regurgitation:
Relation to altered regional left ventricular function. J Am Coll Cardiol 1984;
3:986-991.
94.
Badke FR, Boinay P, Covell JW. Effect of ventricular pacing on regional
left ventricular performance in the dog. Am J Physiol 1980;238:H858-H867.
95.
Little WC, Reeves RC, Arciniegas J, et al. Mechanism of abnormal
interventricular septal motion during delayed left ventricular activation. Circ
Res 1982; 65:1486-1490.
96.
Gomes JAC, Damato AN, Akhtar M, et al. Ventricular septal motion and
left ventricular dimensions during abnormal ventricular activation. Am J Cardiol
1977; 39:641-650.
97.
Miyazawa K, Honna T, Haneda T, et al. Dynamic geometry of the left
ventricle during ventricular pacing: Correlation with cardiac pumping action.
Tohoku J Exp Med 1978; 124:261-266.
98.
Augustijn CH, Arts T, Prinzen FW, et al. Mapping the sequence of
contraction of the canine left ventricle. Eur J Physiol 1991;419:529-533.
99.
Nishimura RA, Hayes DL, Holmes DR, Tajik AJ. Mechanism of
hemodynamic improvement by dual-chamber pacing for severe left ventricular
dysfunction:
an
acute
Doppler
and
catheterization
hemodynamic study. J Am Coll Cardiol 1995;25:281-8
100. Cleland JGF, Daubert JC, Erdmann E, Freemantle N, Gras D,
Kappenberger L, et al. The effect of cardiac resynchronization on morbidity and
mortality in heart failure. N Engl J Med 2005;352:1539-49
66
101. Sade LE, Kanzaki H, Severyn D, Dohi K, Gorcsan J III. Quantification of
radial mechanical dyssynchrony in patients with left bundle branch block and
idiopathic dilated cardiomyopathy without conduction delay by tissue displacement
imaging. Am J Cardiol 2004;94:514-8.
102. Sandhu R, Bahler RC. Prevalence of QRS prolongation in a community
hospital cohort of patients with heart failure and its relation to left ventricular
systolic dysfunction. Am J Cardiol 2004;93:244-6.
103. Bader H, Garrigue S, Lafitte S, Reuter S, Jais P, Haissaguerre M, et al. Intraleft ventricular electromechanical asynchrony; a new independent predictor of
severe cardiac events in heart failure patients. J Am Coll Cardiol 2004;43:24856.
104. Ennezat VP, Maréchaux S, Tourneau T et all; Myocardial asynchronism is a
determinant of changes in functional mitral regurgitation severity during dynamic
exercise in patients with chronic heart failure due to severe left ventricular systolic
dysfunction,European Heart Journal 2006 27(6):679-683
67
68