A. ATOMUN YAPISI VE ELEKTRİK YÜKLERİ
advertisement

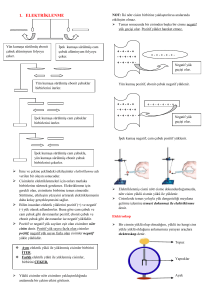
A. ATOMUN YAPISI VE ELEKTRİK YÜKLERİ Maddenin tüm fiziksel ve kimyasal özellikleri, en küçük yapı taşı olan atomun elektronik yapısı ile ilgilidir. • Maddenin elektrik yüklü olduğu çok eskiden beri bilinmektedir. • Süs eşyası yapımında kullanılan kehribar taşı ,( ağaç reçinesinin fosilleşmesiyle oluşmuştur) ipek yada yünlü kumaşa sürtüldüğünde çok küçük cisimleri çekmesi ile elektriklenme çok eskiden gözlemlenmişti. • Plastik tarak saça sürtüldüğünde elektriklenir.Saça ve suya yaklaştırıldığında çeker. • Yün kazağımızı çıkarırken oluşan kıvılcım elektrik yükünün bir yerden bir yere hareket ettiğini gösterir. • Maddenin elektrikle yüklü hale gelmesi , maddede elektrik yüklerinin olduğunun ve bunların hareket ettiğinin bir kanıtıdır. • Bu hareket eden yükün türü nedir? ATOM VE ELEKTRİK • Atomlarda hareketli olan parçacıklar sadece negatif elektrik yükleridir. • ELEKTRİKLENME ÇEŞİTLERİ 1. SÜRTÜNME İLE ELEKTRİKLENME • Ebonit çubuk yün kumaşa sürtüldüğünde ebonitin (-) , yün kumaşın (+) yüklendiği görülür. Cam çubuk ipek kumaşa sürtüldüğünde camın (+), ipek kumaşın ise (-) yüklendiği görülür. Sürtünme ile elektriklenme yalnızca bazı yalıtkan maddeler arasında gözlenebilir. 2. ETKİ İLE ELEKTRİKLENME Yüklü bir cisme bir başka iletken cisim yaklaştırıldığında aynı tür yükler birbirini itip, zıt yükler birbirini çekeceği için cisimlerin üzerinde bir yük hareketi oluşacaktır.. 3. DOKUNMA İLE ELEKTRİKLENME Yüklü bir cisim nötr veya yüklü bir başka iletken cisme dokundurulduğunda aralarında yük alışverişi olur • Bir süre sonra yükler dengelenerek yük alışverişi durur. • Cisimlerdeki yük varlığını ve türünü anlamamıza yarayan alete elektroskop denir. Elektroskop yüklendiğinde yaprakları açılır ve yüksüz olduğunda yaprakları kapalı durumda olur. Metaller gibi elektriği ileten maddelere iletken madde denir, iletkenlerde elektronlar serbestçe hareket edebilir. • Periyodik cetvelde 1A grubu ( H hariç), 2A grubu, 3A grubu ve tüm B grubu elementleri metaldir. • Elektriği ileten sulu çözeltilere de elektrolit denir. • Asitlerin, bazların, tuzların sulu çözeltileri elektrik akımını iletir. • Sulu çözeltilerde elektrik akımını ileten iyonlardır. ŞİMŞEK, YILDIRIM ve GÖK GÜRÜLTÜSÜ Bulutlar hareket ederken birbirlerine ve hava moleküllerine sürtünürler. Sürtünme sonucu üzerlerinde elektriklenme oluşur. Yer yüzünün buluta yakın olan kısımları da zıt cinste elektriklenebilir. Bu sebeple bulut ile yeryüzü arasında zaman zaman elektriksel boşalma olur.Bu olaya yıldırım denir. • Yüksek binaları, kuleleri yıldırımdan korumak için yıldırımlık yapılır. Yıldırımlık (paratoner), toprağa bağlı sivri uçlu bir metal çubuktur. Bu uca düşen yıldırımdaki elektrik, iletken bir kablo yardımıyla toprağa aktarılır. Böylece paratoner yardımıyla yıldırımın tehlikelerinden korunuruz. Bulutlarda biriken elektrik yalnız yer yüzüne değil, bulutun bir noktasından diğer bir noktasına da boşalabilir. Bu olaya şimşek denir. Gerek şimşek, gerekse yıldırım, ışık ile birlikte şiddetli bir ses meydana getirir. Bu sese gök gürültüsü denir. Işık, sesten çok daha hızlı yayılır. Şimşeklerin çaktığı bir havada ilk önce parlak ışığı görür sonrada gök gürültüsünü duyarız. Örneğin; gök gürültüsünün şimşekten bir saniye sonra duyulması yıldırımın 350 metre uzakta oluştuğunu bize gösterir. Elektrikte yük hareketi negatif elektrik yüklerinin hareketiyle gerçekleşir. Pozitif yükler hareketsizdir. Bir atomda pozitif yükler ile negatif yükler birbirine eşit ise buna nötr (yüksüz) atom denir. • Eğer nötr bir atom elektron kaybetmiş ise pozitif yükler çoğunlukta olacağı için bu atoma pozitif yüklü atom (iyon) denir. Eğer nötr atom elektron kazanmış ise bu atoma negatif yüklü atom (iyon) denir. Yükler arasındaki bu kuvvete . Coulomb kuvveti denir. Aynı tür yükler birbirini iter, zıt yükler birbirini çeker UYARI I . Aynı cins elektrik yükleri ile yüklü cisimler birbirlerini İTERLER. + + - - UYARI II. Zıt yükler birbirlerini ÇEKER. + • Elektriklenme atom alışverişi ile olmaz.Olsaydı iki maddenin de yapısının değişmesi gerekirdi. • Cam çubuk, ebonit çubuk, plastik çubuk, tarak sürtülürken herhangi bir değişikliğe uğramamıştır. ETKİNLİK 1: Plastik çubuk ve cam çubuktaki elektriklenme • ETKİNLİK 1 : Sürtme ile elektriklenme ve atomik yapı • AMAÇ: Atomun elektrikli bir yapıya sahip olduğunu belirlemek. • ARAÇ VE GEREÇLER: • plastik cetvel (plastik çubuk, tarak) 2 adet • cam çubuk (cam deney tüpü) 2 adet • döküm ayak 1 adet • ikili bağlama parçası 1 adet • demir çubuk (50 cm) 1 adet • yalıtılmış çubuk 1 adet • yünlü kumaş parçası 1 adet • ipekli kumaş parçası 1 adet • iplik • ETKİNLİĞİN YAPILIŞI • A) Etkinlik düzeneğini kurunuz. • B) İple astığınız plastik cetvele kumaş parçasını sürtün. • C) Diğer plastik cetvele de yün kumaş parçasını sürtünüz. • Şimdi bu cetveli iple asılı cetvele yaklaştırınız. • D) İpteki plastik cetveli çıkarınız. • Yerine cam çubuğu bağlayınız. • E) Cam çubukları ipek kumaşa sürterek elektriklenmelerini sağlayınız. • F) Cam çubuğu asılı cam çubuğa yaklaştırınız. • İki Cam çubuk birbirini itiyor mu? • SONUÇ: • 1. Sürtme ile elektriklenmiş iki cetvel birbirini itmektedir. • 2. Elektriklenmiş iki cam çubuk birbirini itmektedir. • 3. Cam çubuk ve plastik cetvel birbirini çekmektedir. • Buradan şöyle bir sonuca varılabilir. • Benzer deneyler yapıldığında elektriklenmeler farklıdır. • Cam çubuk ve plastik cetvelde olduğu gibi. • Cam çubuğun yükü artı (+), plastik çubuğun yükü eksi (-) kabul edilir. • Bu, tabiatta iki farklı tür yükün olduğunu gösterir. • Atomun çekirdeğinde bulunan protonlar, elektriklenme sırasında yer değiştirmez. • Elektriklenmede, elektronlar yer değiştirir. • Mesela: plastik çubuğun elektriklenmesini atom modeline göre açıklayabiliriz. • Başlangıçta plastik çubuk yüksüz idi. • Proton sayısı elektron sayısına eşit durumdaydı • Böylece; plastik çubukta elektron fazlalığı, yün kumaşta ise elektron eksikliği vardır. • Plastik çubuk(-), yün kumaşta(+) yüklü olur • Yani bir maddedeki elektronlar başka bir maddeye geçebilmektedir. • Elektron veren atom (+) yüklü, elektron alan atom (-) yüklü hale gelmektedir. • Bu olay atomun elektrikli yapıda olduğunu gösterir. • Sürtme ile elektriklenme sırasında protonlar yer değiştirmez. • Protonlar sabit kalarak sadece elektronlar yer değiştirir. • Eğer elimizdeki kazağı sönük bir floresan lambaya yaklaştırırsak lambanın hafifçe parladığını da görürüz. Yünlü bir eşyaya sürülmüş ebonit çubuk kağıt parçacıklarını çeker. Bunun nedeninin ebonit çubuk üzerindeki elektrik yükleridir ETKİNLİK 2: YÜKLÜCİSİMLERİN ELEKTROSKOBA ETKİSİNİN İNCELENMESİ • ETKİNLİK AMACI: Yüklü cisimlerin elektroskop üzerindeki etkisini incelemek. • KULLANILAN ARAÇ VE GEREÇLER: • 1-elektrostatik takım • 2-elektroskop • HAZIRLIK SORUSU: • 1-Bir cismin yüklü olup olmadığını nasıl anlarsınız? Araştırınız. • 2-Yüklü bir elektroskopun yükünü nasıl boşaltabiliriz?Tartışınız. • El TEORİK BİLGİ : Bir cismin yüklü olup olmadığını yüklü ise yükünün, cinsini bulmak için kullanılmaya yarayan araca “Elektroskop” denir. elektroskop yüksüzken metal yapraklar kapalıdır. ( - ) yükle yüklenmiş bir elektroskopun topuzuna parmağımızla dokunursak, negatif yükler vücudumuz üzerinden toprağa akar, elektroskop nötr hale gelir ve yaprakları tamamen kapanır. (+) yüklü elektroskopta; negatif yükler topraktan elektroskopa geçer ve yapraklar yine kapanır. Bu olaya “elektroskobun boşalması” denir. • ETKİNLİĞİN YAPILIŞI: • 1. Yüklü bir cismi nötr bir elektroskoba yaklaştırırsak, topuz yaklaştırılan cismin yükünün zıttı ile, yapraklar ise aynı yükle yüklenirler. • Yapraklar açılır. • 2. Yüklü bir cismi nötr bir elektroskopa dokundurursak topuz ve yaprak aynı yükle yüklenir. • Yapraklar açılır. • 3. Yüklü bir cismi zıt yüklü bir elektroskoba yaklaştırırsak, elektroskobun ve yüklü cismin yük miktarına bağlı olmak şartıyla; • a)Yapraklar biraz kapanabilir.(Elektroskop yükü çoksa) • b)Yapraklar tamamen kapanabilir.(Yükler eşitse) • c)Yapraklar önce kapanıp sonra açılabilir.(Cismin yükü çoksa) • 4. Yüklü bir cismi aynı yüklü bir elektroskoba yaklaştırırsak yapraklar biraz daha açılır. • Eğer dokundurulursa ; • a)Yapraklar biraz açılır. (cismin yükü fazla ise) • b)Yaprakta değişme olmaz. (yükler eşit ise) • c)Yapraklar biraz kapanır.(Elektroskobun yük fazla) • 5. Yüklü bir cismi zıt yüklü bir elektroskopa dokundurursak, yük miktarlarına bağlı olmak şartıyla üç durum gözlenir: • a)Yapraklar biraz kapanabilir.(Elektroskopun Yükü fazla ise) • b)Yapraklar tamamen kapanabilir. (Yükler eşitse) • c)Yapraklar önce kapanıp sonra zıt yüklenerek açılabilir.(Cismin yükü fazla ise) ETKİNLKİ 3:YÜKLÜ BİR EBONİT ÇUBUĞUN SUYU ÇEKTİĞİNİN GÖZLENMESİ • ETKİNLİĞİN AMACI: Elektrikle yüklenmiş yalıtkan maddelerde bulunan elektronların, uygun ortamda bir başka maddeye aktığını görmek. • HAZIRLIK SORUSU: • Yüklü bir ebonit çubuk çeşmeden akan suya yaklaştırılırsa suyun akışını etkiler mi? Tartışınız. • KULLANILAN ARAÇ VE GEREÇLER: • Döküm ayak, statif çubuk, bağlama parçası, şişe tutturucu, kısa cam boru, tek delikli tıpa, geniş beherglas, tabanı kesik şişe, ebonit çubuk, yün parçası, su • TEORİK BİLGİ: • Yünlü kumaş parçasına sürtülerek negatif ( - ) yükle yüklenen ebonit çubuk, çeşmeden ip şeklinde çok ince akan suya yaklaştırılırsa suyu kendine doğru çeker. Çünkü bir iletkene (metal, su .. ) yaklaştırılan yüklü bir cismin etkisiyle, yüklerin ayrılmasına “etkiyle elektriklenme” denir. • Yaklaştırılan cisimdeki yüklerin etkisiyle iletkendeki aynı cins yüklerin itildiği, zıt yüklerin birbirini çektiği görülür. • • Etki ile elektriklenmede yüklü cisimle nötr cisim birbirlerine dokunmadığından aralarında elektron alış verişi olmaz. Yalnız nötr cismin elektronları yer değişir. Yüklü cisim uzaklaştırılırsa elektronlar tekrar eski yerlerine dönerler. Bu şekilde cisim tekrar nötr hale gelir. • ETKİNLİĞİN YAPILIŞI: • 1-Statif çubuğa bağlama parçası takıp, bu parçaya şişe tutturucusunu takınız. • 2-Cam boruyu lastik tıpaya geçiriniz ve şişenin ağzına sıkıca kapayarak şekildeki düzeneği hazırlayınız. • 3-Beherglasa su koyunuz. Cam borunun ağzını kapatarak şişeye su doldurunuz. • 4-Ebonit çubuğu yüne sürterek elektrikle yükleyiniz. • 5-Parmağınızı cam borudan çekiniz ve akan suya yüklediğiniz ebonit çubuğu yaklaştırınız. Çubuğun suyu çektiğini gözleyiniz. Çubuğu ters tarafta tutarak deneyi tekrarlayınız. • ETKİNLİĞİN SONUCU: • Yüklü bir cisim bir iletkene yaklaştırıldığında yüklerin ayrılmasına neden olur. Bu olaya “elektrostatik indüksiyon” (etkiyle elektriklenme ) denir. FARADAYIN ELEKTROLİZ DENEYLERİ • Aslında maddenin elektriksel yapısına ilişkin ilk kanıtlar 1834 yılında M. Faraday tarafından ortaya konmuştur. • Faraday, elektriğin maddeler üzerindeki etkisini inceleyerek elektroliz deneylerini gerçekleştirmiştir. • Elektroliz deneylerinde bir elementin çeşitli bileşiklerinin sulu çözeltilerine elektrik akımı uygulamış ve ve elektrotlarda elementler elde etmiştir. • Faraday kimyasal bileşiklerin sulu çözeltilerinden elektrik akımı geçirerek kimyasal yapıda değişiklik sağlandığını göstermiş ve maddenin elektriksel yapısı hakkında ip uçları elde etmiştir. • Faraday katotta elementi saf olrak elede etmiş ,ve katotta belirli bir miktar madde elde etmek için bir elektrik yükü yada bu yükün basit katları kadar elektrik yükü taşıyabileceğini farketmiştir. • Faraday elektrik yüklerinin parçacıklar halinde taşındığını , elektriğin tanecikli yapıda olduğunu göstermiştir.Faraday , atomların elektrik yüklerini taşıdığını ve bu taneciklerin atomda olduğunu belirtmiştir. • Elektrikle kimyasal değişme ilişkisi , İngiliz fizikçisi ve kimyacısı Michael Faraday (1830) tarafından bulunmuştur. Bugün hala kullanılan elektroliz, elektrolit, elektrot, anot ve katot, Faraday'ın ortaya attığı terimlerdir. ELEKTROLİZDE KULLANILAN TERİMLER • Elektroliz: Bir bileşiği kendisini oluşturan elementlere ayırmak için elektrik enerjisinden yararlanarak yapılan kimyasal bir ayrıştırma işlemidir. • Elektrolit : Elektrik akımını ileten, elektrolize uğrayan sıvıdır. İyonlardan oluşur. (İyonik bağlı bileşiklerin katıları halde elektrik akımını iletmediği, sıvı halde veya sulu çözeltilerinin ilettiği unutulmamalıdır.) • Elektrot : Elektrik akımını ileten çubuk. Elektrolit ile tepkime vermesi gerekir. Genellikle soy metaller ( Cu, Ag, Pt, Au ) kullanılır. • Katot : • Katyonların ((+) yüklü iyonların) gittiği ver. • İndirgenmenin ( elektron almanın ) olduğu yer. • (-) yüklü çubuk. • Anot : • Anyonların (-) yüklü iyonların gittiği yer. • Yükseltgenmenin ( elektron vermenin ) olduğu yer. • (+) yüklü çubuk. FARADAY’IN 1.KANUNU • Elektrolizde biriken madde miktarı elektrik yükü miktarı ile doğru orantılıdır. • Devreden geçen elektrik yükü doğrudan bilinemeyeceği için ampermetre ile ölçülür. • Akım Şiddeti ( I) : Bir elektrik devresinden birim zamanda ( 1 saniyede ) geçen elektrik yükü miktarına akım şiddeti denir. Akım şiddeti birimi Amper dir. Amper = Coulomb / Saniye dir. • Devreden geçen , • elektrik yükü Q (Coulomb) akım şiddeti I (amper) • Zaman t ( saniye) • Elektrik yükü miktarı Q= I. t • Örnek : Bir elektrik devresinde 50 saniye süre ile 150C yük geçerse akım şiddeti kaç amper olur? • Çözüm : t = 50 s q=150C I= q /t = 150 / 50 = 3 Amper olur. I =? • Devereden 1 Amperlik elektrik akımı 1 saniye süre ile geçerse 1 kulonluk ( C) elektrik yükü elde edilir. • 96500kulonluk elektrik yüküne 1 Faraday denir.Bu sırada devrede 1 mol elektron kullanılır. • Elektrik yük birimi olan coulomb (C) , • • Gümüş nitrat çözeltisinin elektrolizinde , katotta 1,118 mg metalik gümüş birikmesine neden olan elektrik yükü miktarına denir. 96500 coulomb= 1 Faraday = 1 mol elektron FARADAY’IN 2. KANUNU • Devreden 1 Faraday’lık akım geçtiğinde elektrotlarda 1 eşdeğer gram madde toplanır. • Elektrotlarda biriken madde miktarı • • m= Q.MA 96500. Td. • MA : Mol kütlesi • Td: Atomun aldığı yada verdiği elektron sayısı • Q:Elektrik yükü • m:Elektrotlarda açığa çıkan madde miktarı • Elektroliz deneylerinden yararlanan İngiliz kimyacı Humphry Davy , bileşikleri ayrıştırmak için elektrik akımı kullanarak potasyum, sodyum, kalsiyum, stronsiyum ve baryum elementlerini saf olarak bileşiklerinden ayırarak elde etmiştir. ELEKTROLİZLE KAPLAMACILIK • Bir metalin üzeri başka bir metalle kaplanır. • Kaplanacak metal katottur. • Elektrolit olarak , kaplamada kullanılacak metalin tuzu kullanılır. • Anot ise kaplamada kullanılan metaldir Bakır bileziği altınla kaplama • Anot : Altın plaka • Katot : Bakır bilezik • Elektrolit : Altının suda çözünen bir tuzu • Anotta çözünen altın plaka , katotta bakır bileziğin üstünde toplanarak, bileziği kaplar. SUYUN ELEKTRİK AKIMININ ETKİSİYLE ELEMENTLERİNE AYRILMASININ GÖZLENMESİ • ETKİNLİK AMACI: Bileşikleri (su) elektrik enerjisi ile ayrıştırarak başka saf maddeler elde etmek. • HAZIRLIK SORULARI: • 1-Farklı yükler birbirini çekerler yargısı elektrotta gerçekleşen olaylar için söylenebilir mi? Araştırınız. • 2-Suyu oluşturan gazlardan oksijen gazı hangi elektrotta toplanmasını beklersiniz? • 3-Suyun elektrolizinde oluşan hidrojen ve oksijen gazları arasındaki yaklaşık oran nedir? Araştırınız. • 4-Saf su ile elektroliz olayını gerçekleştirmek mümkün müdür? TEORİK BİLGİ • • Bir bileşiğin elektrik yardımıyla bileşenlerine ayrılma olayına “elektroliz” denir. Herhangi bir bileşiğin elektrolizinde bileşiğin anyonu anottan, katyonu ise katottan açığa çıkar. • Elektroliz düzeneğinde pozitif ve negatif kutupların her ikisine birden “elektrot” denir. Güç kaynağının pozitif kutbuna bağlanan elektrot “anot” , negatif kutbuna bağlanan ise” “katottur”. İki kutup arasında elektrik taşınmasını sağlayan iletken çözeltiye “elektrolit” denir. • Suyun elektrolizinde katotta ( - ) “hidrojen, anotta( + ) ise oksijen gazı toplanır. Deney sırasında bir süre sonra tüplerde toplanan hidrojen gazı hacim olarak oksijen gazının iki katı olur. • Yapılan deneyde yaklaşık olarak 1 coulomb’luk yükün devreden geçmesi halinde yaklaşık olarak 0,12 cm3 hidrojen, 0,06 cm3 oksijen gazının açığa çıktığı görülmüştür. ETKİNLİK DÜZENEĞİ ETKİNLİĞİN YAPILIŞI • 1-Bir beherglas içerisine 500 ml su koyunuz. İçine az miktar sülfirik asit veya 30 gr kadar çamaşır sodası (Na2CO3) koyarak çözeltinizi hazırlayınız. • 2-İki deney tüpünü de hazırladığınız çözeltiyle ağzına kadar doldurunuz. Sonra hava almayacak şekilde parmağınızla kapatarak ters çeviriniz ve beherglas içerisindeki çözeltiye daldırınız. Tüpleri Bunzen kıskacıyla sabitleyiniz. • 3-Elektrotların uçlarını şekilde görüldüğü gibi tüplerin içlerine yerleştiriniz. Krokodilleri elektrotlara bağlayarak, diğer uçlarını güç kaynağının doğru akım çıkışına bağlayınız. • 4-Tüplerdeki gaz birikmesi sona erdikten sonra yine hava almayacak şekilde sudan çıkarınız. Tüplere kibrit alevi yaklaştırdığınızda patlayarak yanan gaz hidrojen (yanıcı gaz), alevi daha parlak yakan gaz ise oksijen (yakıcı gaz) gazıdır. ETKİNLİĞİN SONUCU • Suyun elektrolizinde; ( - ) kutba bağlı olan tüpte iki hacim hidrojen , ( + ) kutba bağlı olan tüpte bir hacim oksijen gazı toplanır. ELEKTRONUN KEŞFİ CROOKS TÜPÜ • 1870 ‘de İngiliz Fizikçi Williams Crooks , Vakumlu tüp geliştirmiştir.Bu vakumlu tüp içerisinde gazların elektrikle etkileşimi sonucu ortaya çıkan davranışlarını incelemiştir. • Crooks tüpleri olarak bilinen bu tüpler televizyon tüplerinin yapılmasında öncü olmuştur. • Crooks tüpünde elektrotlar arasına yüksek gerilim uygulandığında tüpün cam çeperinde sarı- yeşil floresan ışık yansıması meydana gelir.Tüpün ortasına bir nesne yerleştirildiğinde ise tüpün sonunda bir gölge oluşmaktaydı. • Crooks gölgenin oluşmasında bazı ışınların etkili olabileceğini belirtmiştir.Bu ışınlara daha sonraları katot ışını adı verilmiştir. • Katot Işını:Katottan anota hareket eden ışınlara katot ışınları denir.Katot ışınları doğrusal yol boyunca hareket eden negatif taneciklerdir.katot ışınları hızla hareket eden (-) yüklü taneciklerdir. • Crooks , buradan katot ışınlarının doğrusal hareket ettiği sonucuna varmıştır. ELEKTRONUN KEŞFİ STONEY • 1891 yılında ise J. J. Stoney elektriğin taneciklerden ibaret olduğunu ve bu taneciklerin atomun yapısında da bulunduğunu önermiş ve 1891 yılında bunları elektronlar olarak isimlendirmiştir. • John Stoney’e göre bu negatif elektrik yükleri ( elektronlar) her maddede farklı miktarda bulunmaktadır. • Maddenin nötr olması için bu negatif yüklere eş sayıda pozitif yük bulunması gerekir. • 1897 yılında Joseph John Thomson havası alınmış tüplerde katot ışınlarına manyetik alan ve elektriksel alan uygulayarak davranışlarını incelemiştir. • Thomson elektriksel alan uygulanan katot ışınlarının negatif kutup tarafından itildiğini ve pozitif kutba doğru çekildiğini belirlemiştir. • Aynı cins elektrik yükleri birbirini itmesi ve zıt yüklü elektrikli yüklerinin birbirini çekmesinden dolayı katot ışınlarının negatif elektrik yükleri olduğunu belirlemiştir. • Thomson deneyini farklı metal ve gazlarla tekrarladığında , katot ışınlarının davranışlarında bir değişiklik olmadığını belirleyerek, • Katot ışınlarının maddenin cinsine bağlı olmadığının sonucuna varmıştır. ELEKTRONUN KÜTLESİ VE YÜKÜNÜN BULUNMASI • Thomsan atom modelinde (-) ve (+) yüklerden bahsetmiştir. • Elektriksel ve manyetik alanların şiddetinden yararlanarak , elektron için 1897 yılında • Yük , e_ oranını bulmuştur. • Kütle m • Yük Kütle e_ oranını m -11 1,7588.10 -1 C.kg olarak buldu. • İngiliz fizikçi Thomson ,Gazların elektrik iletkenliği üzerine yaptığı çalışmalardan dolayı Nobel Fizik ödülü almıştır. MİLLİKAN’IN YAĞ DAMLASI DENEYİ • Elektronun yükü ilk defa 1908 yılında Robert Andrews Millikan tarafından ölçülmüştür. • Elektrik yükünü Millikan yağ damlası deneyi ile ölçmüştür. • Millikan yağ damlası düzeneğinde ,yüklü levhalar arasına yağ damlacıklarını küçük bir delikten göndermiş ve yağ damlaları ,aşağıya doğru inerken X ışınları göndermiştir. • Yağ damlacıkları bu X ışınları tutarak negatif yüklenmiştir. • Üst plaka ( + ) • Alt plaka ( - ) • Negatif yüklü yağ damlacıklarının aşağıya doğru düşmemesini sağlayarak , üst plaka tarafından çekilmesini sağlayarak , yukarı hareketi ile damlacığın davranışlarını, düşme hızını , mikroskopta gözlemleyerek bulmuştur. • Millikan yağ damlacığının yükünü , elektronun yükünü, -19 • -1,6.10 Coulomb olarak bulmuştur • Millikan elektronun yükünü bulduktan sonra , Thomson’un e/m değerinden faydalanarak elektronun kütlesini de hesaplamıştır. Elektronun Kütlesi -31 Yük__= yük kütle -28 9,21096.10 kg =9,21096.10 Olarak hesaplamıştır. gr • Millikan’dan önce bilim adamları su damlacıklarını kullanmışlardı. • Kullanılan yağ damlacığının düşük buhar basıncına sahip olanını tercih eden Millikan yağ damlacığının , ışık kaynağının etkisiyle buharlaşmasını önleyerek , deney boyunca yağ damlacığının kütlesinin sabit kalmasını sağlamıştır. ATOMDA ELEKTRONUN YÜKÜ İLE POZİTİF YÜKLER ARASINDAKİ İLİŞKİ • Nötr bir atomdan bir veya daha çok elektron koparıldığında geriye kalan tanecik , koparılan elektronların toplamına eşit miktarda pozitif yük kazanır. • Elektron kaybeden atom (+) yük kazanır. • Crooks tüpünde , katot ışınları tüpün içindeki gaz atomlarından elektronların ayrılmasına neden olduğundan pozitif yüklü iyonlar oluşmuştu. • Bu iyonları ilk araştıran Alman bilim adamı Goldştayn ‘dır. Bu iyonlara pozitif iyonlar yada kanal ışınları adı verilmiştir. • Thomson elektronun kütlesini , • Pozitif iyonların kütlesinin 1/ 1836 ‘sı olarak hesaplamıştır. • Elektrik yükü • Pozitif elektrik yükü • Negatif elektrik yükü kütlesi 1 1/1836 • Rutherford 1918 yılında pozitif yüklü alfa taneciklerini azot, flor, sodyum, alüminyum, fosfor ve bor elementlerine gönderdiğinde hepsinin H+ iyonuna eşit pozitif tanecikler saçtığını gözlemiştir. • Rutherford , bütün elementlerin atomlarında elektronun yüküne eşit fakat zıt yüklü taneciklerin , protonların bulunduğunu belirlemiştir. • Aşağıda verilen özelliklerden hangisi katot ve kanal ışınları için yanlıştır? • • • • A) Yüklü taneciklerden oluşma B) Doğrusal hareket etme C) Elektrik alanda saparlar D) Kullanılan gaz değiştiğinde içerdiği taneciğin değişmesi • E) Ekranda iz , gölge oluşturma • Çözüm: Katot ışınları negatif yüklü elektronlardır.Kullanılan maddenin cinsine bağlı değildir.Doğrusal hareket ederler.Ekran üzerinde iz bırakırlar. • Kanal ışınları ise pozitif iyonlardır.Doğrusal hareket ederler.Kullanılan gazın iyonu içerirler.Katot ışınları maddenin cinsine bağlı değilken kanal ışınları bağlıdır. D şıkkı yanlıştır. ATOM NUMARASI VE ÇEKİRDEK YÜKÜ • Nötr bir atomda pozitif yük sayısı , negatif yük sayısına eşittir.Yani elektron ve proton sayıları aynıdır. • Atomdaki proton sayısı o elementin çekirdek yükü ve proton sayısı olarak adlandırılır. • Atom numarası Z ile gösterilir. ATOMUN PROTON SAYILARININ BELİRLENMESİ • İngiliz kimyacı Henry Moseley , 1912 yılında X ışınlarını kullanarak, değişik elementlerin farklı X ışınları spektrumunu elde etmiştir. • Spektrumları incelediğinde her elementin sadece birkaç karekteristik spektral çizgi içeren X ışınları spektrumu olduğunu görmüştür. • Moseley, elementlerin atom numaralarını doğru bir şekilde belirlemiştir. • Moseley, elementlerin özelliklerinin atom kütlelerinden değil, atom numaralarına bağlı olduğunu deneysel olarak belirlemiştir. • Bu sonuç, atom kütlelerine göre sıralanarak oluşturulan Mendeleyev’in elementler tablosunu değiştirerek günümüzde kullanılan elementlerin atom numaralarına göre sıralandığı Periyodik tablo oluşturulmuştur. • HENRY MOSELEY • Moseley atom numaraları 13 ile 79 arasında olan 38 elementin X-ışınları spektrumunu inceledi.Her elemen için o elemente karşılık gelen karakteristik spektrum çizgisini kullanan Moseley , elementin atom numarası ile çizgi frekansının kare kökü arasında doğrusal bir ilişki olduğunu • buldu.Başka bir değişle elementler atom numarası artışına göre dizildiğinde spektrum çizgisi frekansının karekökü bir elementten diğerine gittikçe sabit bir miktarda artar. • Henri Moseley elementlerin spektrumlarını incelediğinde Ca ve Ti elementleri arasında bir uyumsuzluk olduğunu gördü.Bu iki element arasında başka bir element bulunması gerektiğini belirterek Sc elementinin keşfedilmesini sağlamıştır. • Bundan dolayı Moseley X-ışınları spektrumuna dayanarak elementlerin doğru atom numaralarını tahmin edebildi.Böylece atom ağırlıkları komşu atomlarınkine uygun düşmeyen K,Ni ve I un sınıflandırılması problemi de çözümlenmiş oldu. • Diğer taraftan Moseley Ce den Lu e kadar olan seride 14 element bulunması ve bu elementlerin ve bu elementlerin periyodik çizelgede Lantan’dan sonra gelmeleri gerektiğini bildirdi.Moseley’in diagramları ayrıca 79 numaralı elementten önce henüz o zamana kadar bulunmamış 4 elementin var olması gerektiğini de gösterdi. • Nihayet Moseley’in çalışmalarına dayanarak periyodik yasa • “Elementlerin fiziksel ve kimyasal özellikleri atom numarasının periyodik fonksiyonudur” şeklinde tekrar tanımlandı. • Moseley ayrıca, atomda bir elementten diğerine gidildikçe artan temel bir nicelik bulunduğunu ifade ederek bu niceliğin ancak merkezdeki artı yüklü çekirdeğin yüklü olabileceğini belirtti. • Moseley,Atom numarası ile proton sayısının aynı olduğunu belirterek bu yükün çekirdek yükü olduğunu belirtmiştir. • Henry Moseley: • Periyodik Sistemin, elementlerin fiziksel ve kimyasal özelliklerinin atom numarasının periyodik bir sonucu olduğunu belirtmiştir. • Periyodik cetvelde aynı gruptaki elementlerin fiziksel ve kimyasal özellikleri birbirine benze özellikler göstermektedirler. Periodik Tablo 1911 Kütle numarası K.N. X Atom numarası Z Moseley’in Ölümü: 10 Aug 1915 Moseley’s death:10 Aug 1915 1915 (8 Ağustos, 05:00) Baldwin kuvvetleri Conk Bayrı’nın kuzey bölümüne hücum edecektir. Bir süre sonra Birlikler Çiftlik (Farm) denilen bölgede sıkışırlar. Ne ileri ne geri gidilebilmektedir. Baldwin Q tepesine ulaşma amacı için açık olan sol taraftan hücuma karar verir. Ancak hücum başarısızdır. Çiftlik alanını tutmaya çalışırlar. (9 Ağustos) Baldwin’in birliği hala Çiftlik’tedir.(Baldwin’s unit is in the Farm) (10 Ağustos) Türkler karşı atağa geçerler. Conk Bayırı’ndan Çiftlik (Ağıl Dere)’ye akarlar. Gögüs göğüse bir savaş olur. İngiliz Kuv. Kom. Sir Hamilton’un daha sonraki tasvirine göre ‘bu kadar umutsuz bir savaş tanımlanamaz. Muhteşem döğüşen Türkler, Allah’ın adını tekrarlayarak dalga dalga geliyorlardı. Adamlarımız bu akışa kahramanca tüm gücleri ile karşı koydular. Hiçbir fedakarlıktan kaçınmadılar. Dayandıkları yerlerde öldüler.’ Baldwin ve tüm adamları ve bu arada haberleşme subayı HM, yaşayan İngiliz bilimci gençlerinin en gelecek vaat edeni, de bu savaşta yaşamını yitirdi. (Moseley’s death) Aynı gün, bir başka mermi de, Türk Birlikleri Komutanı Alb. Mustafa Kemal’in cep saatine çarparak onun yaşamını kurtaracak, bu tesadüf ise Türk ulusunun tüm kaderini değiştirecektir. • İngiliz fizikçi ve kimyacı Moseley 1915’te Çanakkale Savaşında ölmüştü ve orda yatıyordu!... • Atatürk’ün dediği gibi, artık düşmanımız değil, dostumuz, hatta bizim de fizikçimiz sayılırdı.. TÜBİTAK BİLİM TEKNİK, Haziran 2002 (my article on H.M. TBT, June 2002 Doğadaki en küçük elektrik yükü elektronun ve protonun yüküdür. Bunlar birbirine değer olarak eşit fakat işaret olarak zıttır. Elektron ve protonun yükü çok küçük olduğu için yük birim olarak coulomb (C) kullanılır. Atom,maddenin en küçük yapı taşıdır. Elektron ( e - ) Yörünge Proton ( p +) +p 0n Çekirdek Nötron (n 0 ) Atomun Yapısı • Kütle numarası 27 3+ iyon yükü X Atom numarası 13 10 elektron sayısı NÖTRONUN KEŞFİ • Atomun kütlesi , protonların kütlelerinin toplamından büyüktür.Bu büyüklük ya iki katı kadar yada daha fazla büyüktür. • Protonların kütlesinin yarısı kadar yada daha fazla olan tanecik nedir? • 1920 yılında Rutherford çekirdekte yüksüz taneciklerin olabileceği fikrini ileri sürmüştür. • 1932 yılında İngiliz fizikçi James Chadvich , çekirdek reaksiyonları üzerinde yaptığı çalışmalar sonrasında ,atomun çekirdeğinde protonlardan başka , kütlesi protonun kütlesine eşit olan yüksüz tanecikleri bularak bu taneciklere yüksüz anlamındaki nötron adını verdi. • Atomun çekirdeğinde pozitif yükleri bir arada tutan nötronu keşfeden James Chadvch ,1935 yılında bu çalışmasıyla Nobel Fizik ödülünü almıştır. • Kütle numarası= Proton sayısı+ nötron sayısı • K.N. = p + n