MADDE VE ISI
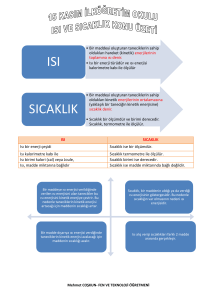
Sıcaklık, Enerji değil sadece enerjinin varlığını gösteren bir
Öz ısısı küçük olan maddelerin sıcaklığı daha hızlı ve
değerdir. Termometre ile ölçülür. Birimi 0C(santigrat derece),
çok artar, büyük olan maddelerin ise sıcaklığı yavaş
Madde miktarına bağlı değildir.
ve az artar. Yani hızlı artan hızlı azalır.
Isı, Madde taneciklerinin sahip olduğu toplam enerjiye ısı denir.
Isı, bir enerjidir. birimi ise joule veya kalori (cal)’dir Madde
miktarına bağlıdır. Bir maddenin ısısı artarsa sıcaklığı da
artar Yani doğru orantılıdır. Isı aktarımı sıcaklığın fazla
Öz ısı ile sıcaklık artışı ters orantılıdır.
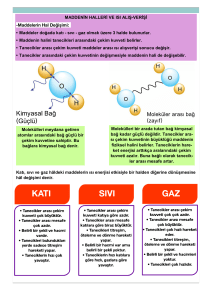
MADDENİN HALLERİ VE ISI ALIŞ--VERİŞİ
olduğu yerden sıcaklığın az olduğu yere doğru olur.
1-Aynı süre ısıtıldığında
şekilde miktarı fazla
olan sıvının sıcaklık
artışı diğerine göre
daha yavaş olur.
2-Kaplardaki sıvıları
aynı sıcaklığa ğetirmek için miktarı fazla olan sıvıyı daha
fazla süre ısıtmak gerekir veya ısıtıcının gücünü
arttrımalıyız.
TEMOMETRELER: içindeki maddenin ısı almasıyla
genleşme veya büzüşmesiyle ölçüm yapar. termometre
içinde kullanılan Sıvının donma ve kaynama
sıcaklıkları arasındaki değerleri ölçebilir.
Metal, sıvılı(civa, alkol) ve gazlı termometreler vardır.
KÜTLE VE ISI İLİŞKİSİ
Maddelerin sahip oldukları ısı enerjisi kütleleriyle doğru
orantılıdır. Yani sıcaklıkları aynı olan aynı tür iki maddeden
kütlesi büyük olanın ısısı daha fazladır. Bunun nedeni kütlesi
büyük olan maddede tanecik sayısının daha fazla olmasıdır.
Enerji Dönüşümü
Doğada Isı, ışık, mekanik, kimyasal, nükleer enerji gibi
farklı enerji türleri vardır. Toplam enerji miktarı hiçbir
zaman değişmez fakat cismin sahip olduğu enerji türleri
birbirine dönüşebilir. Örneğin Tost makinesi, fırın, su
ısıtıcısı ve elektrik sobasında elektrik enerjisi ısı enerjisine
dönüşür. Ampulün yanması sırasında elektrik enerjisi ısı
ve ışık enerjisine dönüşür. Fren yapan aracın lastiklerinde
mekanik enerji, ısı enerjisine dönüşür. Ellerin birbirine
sürtülmesi sırasında mekanik enerji ısı enerjisine
dönüşür. Besinlerin kimyasal bağlarında depolanan
enerji, besinlerin solunum olayında parçalanması sonucu
ısı ve kimyasal enerjiye dönüşür.
Erime
Katı haldeki maddenin ısı alarak sıvı hale geçmesine erime denir.
Katı haldeki madde ısıtılırsa;
• Madde ısı enerjisi alır.
• Tanecikler enerji kazanır ve kinetik enerjisi artar.
• Maddenin sıcaklığı artar.
• Taneciklerin hızı artar.
• Taneciklerin arasındaki çekim kuvveti azalır.
• Tanecikler arasındaki boşluk artar.
• Tanecikler birbirinden uzaklaşır.
• Hızlanan tanecikler yer değiştirerek başka taneciklerle yeni
bağlar oluşturur.
• Madde sıvı hale geçer.
Donma
Sıvı haldeki maddenin ısı vererek katı hale geçmesine donma
denir.
Sıvı haldeki madde soğutulursa;
• Madde dışarıya ısı enerjisi verir.
• Tanecikler enerji kaybeder ve kinetik enerjisi azalır.
• Maddenin sıcaklığı azalır.
• Taneciklerin hızı azalır.
• Taneciklerin arasındaki çekim kuvveti artar.
• Tanecikler arasındaki boşluk azalır.
• Tanecikler birbirine yaklaşır.
• Madde katı hale geçer.
Buharlaşma
Sıvı haldeki maddenin ısı alarak gaz hale geçmesine
buharlaşma denir. Sıvı haldeki madde ısıtılırsa;
ÖZ ISI
• Madde ısı enerjisi alır.
• Tanecikler enerji kazanır ve kinetik enerjisi artar.
Bir maddenin 1 gramının sıcaklığını 10C değiştirmek için
• Maddenin sıcaklığı artar.
gerekli olan ısı miktarına öz ısı denir. Öz ısı c ile
• Taneciklerin hızı artar.
• Taneciklerin arasındaki çekim kuvveti azalır ve yok denecek
gösterilir ve her madde için farklıdır. Bu nedenle
kadar azdır.
maddeler için ayırt edici özelliktir. Öz ısının birimi öz ısı
• Tanecikler arasındaki boşluk artar.
cal/g 0C veya j/g 0C birimiyle ifade edilir.
• Tanecikler birbirinden çok fazla uzaklaşır ve bağımsız
Aynı kütleye sahip iki ayrı maddeye, aynı ısıyı verdiğimizde
sıcaklık artışları aynı olmaz. Isıtılan bir maddenin sıcaklık
artışı maddenin türüne göre değişir.
hareket eder.
• Madde gaz hale geçer.
ERİME ve DONMA ISISI
2 ve 4. Bölgelerde madde hal değiştiriyor demektir. Madde ısı
almaya devam ettiği halde sıcaklık artışı olmaz. Madde iki
halde bulunur. Katı +sıvı veya sıvı +gaz şeklinde
Erime ve Donma ısısı arttıkça gerekli olan ısısı da artar.
Erime ısısı ile erime sıcaklığı birbirine karıştırılmamalıdır.
Erime sıcaklığı = Erime noktası (su için bu 0 0C dir.)
Donma sıcaklığı = Donma noktası (su için bu 0 0C dir.)
Erime sıcaklığı = Donma sıcaklığı
Erime ısısı = Donma ısısı
Buharlaşma ısısı = Yoğuşma ısısı
SOĞUMA EĞRİSİ
Erime - Donma - Buharlaşma – Yoğuşma Isıları yukarıdaki
formüle göre hesaplanır veya yorumlanır.
Bu ısılar her madde için farklıdır yani ayırt edici özelliktir.
Donma ve Kaynamayı Geciktirme
Saf bir maddeye eklenen farklı cins madde, saf maddenin
kaynama noktasını yükseltir donma noktasını düşürür.
Örneğin suyun içine tuz atılırsa suyun kaynama sıcaklığı
tuzun miktarına göre 100 0C den yukarı çıkar veya donma
sıcaklığı 0 0C den aşağı iner.
Soğuma eğrisi ısınma eğrisinin tam tersidir.
Zamanla sıcaklık artışı görülüyorsa ısınma eğrisi, zamanla
sıcaklıkta düşüş oluyorsa soğuma eğrisi demektir.
ISINMA EĞRİSİ
Bu tür sorularda sizden
istenen sıcaklık değeri E.N
den küçük ise katı E.N---K.N
arasında ise sıvı K.N den
büyük ise gaz halde bulunur.
Termometreler içinde kullanılan sıvıların E.N ve K.N arasında ki
değerleri ölçebilir.
Eşit kütleli cisimlerde buharlaşma veya erime ısısı fazla olan
daha çok ısı alır ya da daha uzun sürer. Doğru orantılı
Kaynama tek sıcaklıkta olur.
Kabın tabanında başlar
1
2
3
4
5
1, 3 ve 5. Bölgelerde madde ısı alıyor ve sıcaklık artışı
gerçekleşiyordur. Bu bölgelerde sıcaklık artışı olduğundan
tanecikler hızlanır, enerjiler artar. Madde tek halde bulunur.
Q=m.c. t formülüne göre yorumlar yapılır.
Q : alınan ısı
m : kütle
t : sıcaklık
Buharlaşma her sıcaklıkta olur.
Kabın üstünde gerçekleşir
Yükseklere çıkıldıkça açık hava basıncı azalacağından bir
maddenin kaynama noktası da düşer.
Araştırılan özelliklerde veya kıyaslama sorularında her zaman
ne isteniyorsa o değişir diğer bütün özellikler aynı olmalıdır.
Formülde eşitliğin sağı ve solundaki ifadeler doğru orantılı.
Eşitliğin aynı tarafında olanlar ters orantılıdır.