Kimyasal Tepkimeler
advertisement

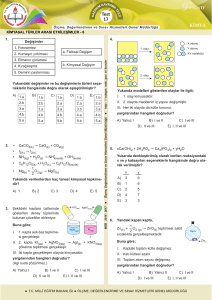
KİMYASAL TEPKİMELER KİMYASAL TEPKİMELER Kimyasal olayların sembol ve formüllerle gösterilmesine kimyasal tepkime denir. H2 gazı, O2 gazı ile tepkimeye girerse H2O oluşur. Bu olay, H2 + O2 H2O şeklinde yazılır. Okun solundaki maddelere reaksiyona giren, okun sağındaki maddelere ürün denir. Kimyasal reaksiyonları aşağıdaki şekillerde sınıflandırabiliriz. 1. Organik Maddelerin Yanma Reaksiyonları O2 ile reaksiyona girmeye yanma tepkimesi denir. Genellikle yanma olaylarında ısı açığa çıkar. CH4 + 2O2 CO2 + 2H2O + ısı C2H6 + 7/2 O2 2CO2 + 3H2O+ ısı C2H5OH + 3O2 2CO2 + 3H2O+ ısı Yanmanın Şartları 1. Yanıcı madde 2. Oksijen 3. Tutuşma sıcaklığı Yanma olayları için gerekli şartlardır. Yanma olayları yavaş ve hızlı yanma olarak ikiye ayrılır. Doğalgazın yanması hızlı gerçekleşirken, demirin paslanması yavaş gerçekleşir. Oksijen : Havada % 21 (yaklaşık 1/5) oranında bulunur. Renksiz, kokusuz, havadan ağır yakıcı bir gazdır. 2. Ayrışma (Analiz) Reaksiyonları Bir bileşiğin kendisinden daha basit maddelere ayrıştırılmasına analiz denir. 3. Birleşme (Sentez) Reaksiyonları İki farklı maddenin birleşerek kendi özelliklerini kaybedip yeni özellikte bir madde meydana getirmesi olayına sentez denir. H2 + 1/2 O2 H2O C + O2 CO2 CO2 + H2O H2CO3 4. Endotermik Reaksiyonlar Dışarıdan ısı alarak gerçekleşen kimyasal reaksiyonlardır. Kireç taşının ısıtılması ile CaO ve CO2 ye ayrışması gibi. CaCO3 + ısı CaO + CO2 KClO3 + ısı KCl + O2 5. Ekzotermik Reaksiyonlar Dışarıya ısı veren kimyasal reaksiyonlardır. Kömürün yanması gibi. C + O2 CO2 + ısı CH4 + 2O2 CO2 + 2H2O + ısı 6. Nükleer Reaksiyonlar a. Bölünme (Nükleer fisyon) reaksiyonları : Büyük çekirdeklerin küçük çekirdeklere parçalanması olayıdır. Reaksiyon sırasında çok fazla enerji açığa çıkar. Örnek: Atom bombası gibi. b. Birleşme (Nükleer füzyon) reaksiyonları : Küçük kütleli atom çekirdeklerinin birleşerek büyük kütleli atom çekirdekleri oluşturması olayıdır. Hidrojen bombası gibi. Hidrojen bombasından açığa çıkan enerji, atom bombasından yaklaşık 1000 kat daha fazladır. Güneşte hidrojen atomlarının birleşip helyuma dönüşmesi (füzyon reaksiyonu) sırasında çok büyük enerji açığa çıkar. Oksijenin elde edilmesi a. Oksijen, sıvı havanın damıtılmasıyla elde edilir. Endüstride kullanılır. b. Potasyum klorat (KClO3) ın ısıtılmasıyla c. Laboratuarda cıva oksit (HgO) in ısıtılması ya da suyun elektroliziyle elde edilir. Elektroliz : İletken bir sıvının elektrik akımı ile kendini oluşturan elementlere ayrılmasına elektroliz denir. Elektriği ileten eriyiklere de elektrolit denir. Elektroliz sırasında oluşan yüklü atom veya atom gruplarına da iyon denir. Şekildeki elektroliz düzeneğinde anot ve katot iletken metallerden yapılır. Elektrolit olarak asit, baz veya tuzun sulu çözeltisi kullanılırsa devreden akım geçtiği gözlenir. Sıvı (elektrolit) içindeki (–) yüklü iyonlar anota (+) yüklü iyonlar katoda gider ve böylece sıvı elementlerine ayrılmış olur. Elektroliz olayında anyonlar anottan, katyonlarda katottan elementel olarak açığa çıkarlar. Örnek olarak; asitli ortamda H2O nun elektrolizinden anotta oksijen gazı, katotta H2 gazı toplanır. KİMYASAL REAKSİYONLARDA DENKLEM DENKLEŞTİRME Denklem Denkleştirirken: 1. En kalabalık atom grubu bulunan bileşiğin kat sayısı 1 olarak alınır. 2. Hidrojen ve oksijenin eşitlenmesi en sona bırakılmalıdır. 3. Atom eşitliğini sağlamak için kullanılan katsayılar bileşiğin baş tarafına yazılır ve bu katsayılar bileşikteki herbir atomla çarpım durumundadır. H2O 2H, 1 O H3PO4 3H, 1P, 4O Ca(OH)2 1Ca, 2O, 2H CH3COOH 2C, 4H, 2O 2CaCl2 2Ca, 4Cl şeklinde atom sayıları hesaplanır. Denklem Katsayılarının Anlamı Bir denklem eşitlendiğinde maddenin katsayısı o maddenin mol sayısı demektir. Örnek 1 Al + S Al2S3 denklemini denkleştiriniz? Çözüm Bu denklemde Al2S3 ün katsayısı 1 olarak alınır. Al nin katsayısı 2, S nin katsayısı 3 olmalıdır. Denklemin denkleşmiş hali; 2Al + 3S Al2S3 olur. Örnek 2 CaO + H3PO4 Ca3(PO4)2 + H2O denklemini denkleştiriniz? Çözüm Ca3(PO4)2 nin katsayısını 1 alalım. Denklemin sağ tarafında 3 tane Ca atomu vardır. Sol tarafta da 3 tane Ca atomu olması için CaO nun katsayısı 3 olmalıdır. Sağ tarafta 2 tane P atomu vardır. Sol tarafta da 2 tane P olması için H3PO4 ün katsayısı 2 olmalıdır. Hidrojen ve oksijenin eşitlenebilmesi için H2O nun katsayısı 3 olmalıdır. Denklemin denkleşmiş hali : 3CaO + 2H3PO4 Ca3(PO4)2 + 3H2O Örnek 3 K2Cr2O7 + 2X 2K2CrO4 + H2O denkleminde X bileşiğinin formülü ne olmalıdır? Çözüm K2Cr2O7 + 2X 2K2CrO4 + H2O Denklemin sol tarafında Denklemin sağ tarafında 2K, 2Cr, 7O 4K, 2Cr, 9O, 2H X in katsayısı 2 olduğundan X bileşiğinin formülü KOH olmalıdır.