PowerPoint Sunusu - files.eba.gov.tr
advertisement
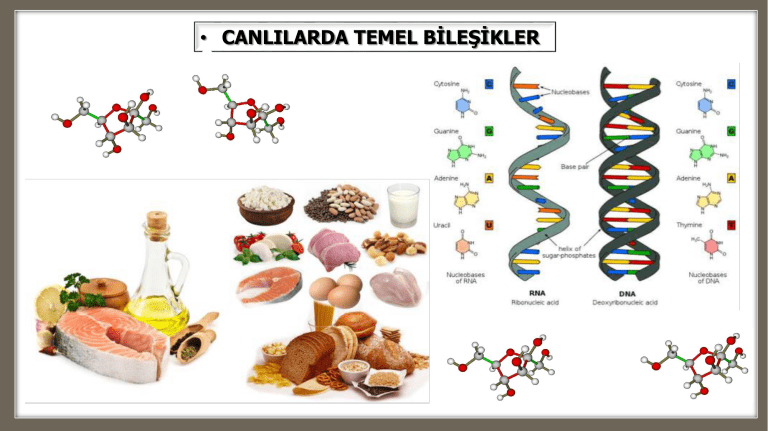
• CANLILARDA TEMEL BİLEŞİKLER • Hidroliz Polimer (Büyük Molekül) Monomer (Küçük Molekül) Hidroliz Yıkım H2 O H2 O Monomer (Yapıtaşı) H2O H2 O H2 O • Dehidrasyon Polimer Dehidrasyon Yapım H 2O H2 O H2 O H2 O H2 O • Hidroliz • Yıkım olayıdır. Büyük moleküllerin (polimer) yapısındaki kimyasal bağlara su vererek parçalanması ve küçük moleküllerin (yapıtaşı – monomer) açığa çıkmasıdır. • Dehidrasyon • Yapım olayıdır. Küçük moleküllerin (yapıtaşı – monomer) birleşirken aralarında oluşan kimyasal bağlardan suyun çıkmasıyla büyük molekül (polimer) yapılmasıdır. • ATP’ nin Yapısı (5C) Organik baz (N) Adenin Riboz Yüksek Enerjili Bağlar Pİ Pİ Adenozin Adenozin monofosfat ( AMP ) Adenozin difosfat ( ADP ) Adenozin trifosfat ( ATP ) Pİ • ATP ve ATP’ nin Yapısı • Bir organik baz (N) olan adenin, riboz şekeri (5C) ve üç tane organik fosfattan oluşur. • Önce adenin ile riboz birleşerek adenozini meydana getirir. • Adenozinde sırasıyla üç inorganik fosfatla birleşerek sonuçta ATP oluşur. • Defosforilasyon • Fosforilasyon • ADP‘ den ATP oluşumu ATP nin yapımını yani enerji üretimini ifade eder. Fosforilasyonda inorganik fosfat organik fosfata dönüşür. ADP + Pİ ATP • ATP ‘den ADP oluşumu ATP nin yıkımını yani enerji tüketimini ifade eder. Defosforilasyonda organik fosfat inorganik fosfata dönüşür. ATP ADP + Pİ • Metabolizma • Metabolizma canlılığı ifade eden bir terimdir. • Genel anlamda bir canlının hücresinde geçen enerji üretim ve tüketim sürecidir. • Metabolik süreç dış ortamdan bağımsız değildir. • Bu süreç dış ortamdan bazı maddelerin hücreye girmesine ve çıkmasına bağlıdır. • Örneğin ATP üretmek için hücreye enerji hammaddesi ve O2 gelmeli hücreden de dış ortama CO2 verilmelidir. • Metabolizmada enerji üreten süreç Katabolizma enerji tüketen süreç Anabolizma olarak adlandırılır. • Katabolizmada önce hücre solunumu (hidroliz) ile glukoz parçalanır. • Glukozun yapısındaki kimyasal bağlarda saklı olan enerji açığa çıkar. • Açığa çıkan bu enerjiyle ADP + Pİ ATP yapılır (dehidrasyon). • Bir başka değişle enerji bağdan çıkar bağa girer. • Anabolizma ise katabolizmada ATP şeklinde üretilen enerjinin madde yapımı ve birçok yaşamsal faaliyetlerde tüketilmesidir. • O halde madde yapmak (dehidrasyon) için ATP (hidroliz). ADP + Pİ yıkılır Metabolizma Anabolizma (Madde yapımı) Katabolizma (Madde yıkımı) Glukoz Hücre solunumu Monomer + ( n ) Enerji H2 O (Dehidrasyon) (Hidroliz) H2 O ATP ADP + Pİ Fosforilasyon H 2O (Dehidrasyon) Polimer ATP H2 O (Hidroliz) ADP + Pİ Defosforilasyon • Anabolizma Polimer Monomer + ( n ) H2 O ATP H2 O (Hidroliz) H 2O H2 O (Dehidrasyon) ADP + Pİ Defosforilasyon • Katabolizma H2 O H2 O H2 O Glukoz H2 O Kimyasal bağ Hücre Solunumu H2 O H2 O Hidroliz (Yıkım) Bağdan çıkan enerji Bağa girer. ADP + Pİ H2 O Dehidrasyon (Yapım) ATP • ATP’ in Yapımı Ve Yıkımı ATP Pİ Aktifleşme enerjisi Madde yapımı Oksijenli solunum Isı Sinirsel iletim Hareket ve kasılma Oksijensiz solunum Pİ FOSFORİLASYON ADP + Pİ ATP ADP DEFOSFORİLASYON ATP ADP + Pİ • Fosforilasyon Çeşitleri • Fotofosforilasyon: Işık enerjisi kullanarak ATP üretimi (fotosentez) • Oksidatif fosforilasyon: Oksijen varlığında (oksijenli solunum) ATP üretimi. • Substrat seviyesinde fosforilasyon: Enzimler yardımı ile ATP sentezi. (glikoliz ve krebs döngüsü) • Kemosentetik fosforilasyon: İnorganik maddelerin ( NH3 - NO2 ) yükseltgenmesi (oksitlenmesi) ile açığa çıkan kimyasal enerji ile ATP sentezi. • Canlılarda Temel Bileşikler • Organik • İnorganik • Karbonhidratlar • Su • Yağlar • Asitler • Proteinler • Bazlar • Enzimler • ATP • Nükleik asitler • Vitaminler • Hormonlar • Karbonhidratlar • Yapılarında C – H – O içeren bileşiklerdir. Genel formülleri (CH2O) n dir. • Unlu ve şekerli tüm besinler karbonhidratlara girer. • Hücrelerde ilk olarak tercih edilen enerji hammaddesidirler. Çünkü yıkımları kısa sürer yani kısa sürede enerjiye dönüşürler. • Karbonhidratlar azda olsa hücrede yapı maddesi olarak kullanılırlar. • Örneğin bitki hücrelerinde bulunan hücre çeperi bir karbonhidrat olan selülozdan yapılmıştır. Yine hücre zarlarının yapısında da az miktarda bulunurlar. Karbonhidratlar üç grupta incelenir. Monosakkaritler Disakkaritler Polisakkaritler • Monosakkaritler (tek şekerler) • Karbonhidratların hidrolizi sonucunda oluşan monomerleridir. • Suda çözünürler. • Monosakkaritler Karbon sayılarına göre; Heksoz (6C) Glukoz Fruktoz Galaktoz süt şekeri Bitkisel Hayvansal Pentoz (5C) Riboz - RNA - ATP Deoksiriboz - DNA Trioz (3C) PGA PGAL - Fotosentez - Hücre solunumu • Heksozlar (6C) (Glukoz – Fruktoz – Galaktoz) • Üçünün de kimyasal formülü C6H12O6 dır. Ancak molekül dizilişleri farklı olduğundan (izomer) değişik adlar alırlar. • Glukoz Başlıca kan şekeridir. Fazlalığı ve eksikliği hastalıklara yol açar. Kandaki düşük glukoz düzeyinden özellikle beyin etkilenir. Çünkü beyin hücreleri enerji kaynağı olarak sadece glukozu kullanır. • Glukozun fazlası hayvanlarda glikojen şeklinde depo edilir. Glikojen karaciğer ve kaslarda depo edilir. Kan şekerinin düzenlenmesinde karaciğer glikojeni rol oynar. Kas glikojeni kasın kendi faaliyetleri için kullanılır. • Bitki hücrelerinde ise glukozun fazlası nişasta şeklinde depo edilir. • Açlıkta kandaki glukoz azalır. • Bu durumda karaciğerde glikojen yıkıma (hidroliz) uğrar ve oluşan glukozlar kana geçer. • Karaciğer hücresinde su azalır. • Toklukta ise kanda glukoz artar. • Bu durumda glukozlar karaciğerde glikojene dönüşür. (dehidrasyon). • Karaciğer hücresinde su artar. • Bitki hücrelerinde ise glukozun fazlası nişasta şeklinde depo edilir. • Disakkaritler (ikili şekerler) • İki mol monosakkaritin dehidrasyonu ile oluşur. H2 O Monosakkarit + Monosakkarit Dehidrasyon Disakkarit Hidroliz • Üç çeşit disakkarit bulunur. Glukoz + Glukoz Dehidrasyon Maltoz Glukoz + Fruktoz Sukroz Glukoz + Galaktoz Laktoz Bitkisel Hayvansal • Polisakkaritler (çoklu şekerler) • (n) sayıda glukoz molekülünün dehidrasyonu ile oluşur. Üç çeşittir. • Nişasta – Sellüloz – Glikojen • Üçünün de monomeri glukozdur. Glukozların dizilişlerindeki fark moleküllerin farklı olmasına yol açar. Glukoz + (n) Dehidrasyon Nişasta Bitkisel Glukoz + (n) Sellüloz Glukoz + (n) Glikojen Hayvansal • Nişasta suda erimez. • Nişastanın ayracı İyottur. Nişasta + I Mavi – mor renk verir. • Karbonhidratların arasındaki bağlar glikozid bağ adını alır. • Yağlar (Lipid) • Yapısında C – H – O içeren bileşiklerdir. Ayrıca N – P’ da içerebilirler. Ancak oksijen oranı karbonhidratlara göre daha düşük karbon oranı ise daha yüksektir. Bu nedenle bir mol yağ bir mol karbonhidrata göre iki kat enerji verir. • Yağlar karbonhidratlardan sonra tercih edilen enerji hammaddesidir. Çünkü yağların yıkımı uzun sürer. • Yağlar suda erimez ancak organik eriticilerde (alkol – eter – kloroform) erirler. • Yağlar vücutta yapı maddesi olarak da görev yaparlar. Hücre zarlarının yapısında, iç organların etrafında (koruma), derinin altında (ısı kaybını engeller) bulunur. • Göçmen kuşlarda ve kış uykusuna yatanlarda enerji ile su ihtiyacını karşılar. • Yağlar biyolojik önemlerine göre dört grupta incelenir. • Nötral yağlar (trigliseridler) • Vücutta depo edilen yağlardır. Enerji ve yapı maddesi olarak kullanılırlar. 3 ester bağı 3 H2 O Gliserol + 3 Yağ asidi Dehidrasyon Hidroliz Trigliserid (Nötr yağ) • Yağ asitleri Doymuş yağ asitleri CH2 CH2 CH2 CH2 CH2 CH2 CH2 • Karbon atomları arasında tek bağ bulunur. Katı hayvansal yağlar bu gruba girer. Tereyağı ve kuyruk yağı .. Doymamış yağ asitleri CH2 CH2 CH2 CH2 CH2 CH2 CH2 • Karbon atomları arasında çift bağ bulunur. Sıvı bitkisel yağlar bu gruba girer. ayçiçek ve zeytinyağı .. • Fosfolipidler • Hücre zarlarının yapısına katılırlar. • Steroid yağlar • Organik eriticilerde çözünmelerinden dolayı yağ olarak kabul edilirler. Bazı hormonların (eşeysel) ve bazı vitaminlerin (D vitamini) yapısına katılırlar. • Hayvan hücrelerinde hücre zarının yapısına katılan kollesterolde bu gruba girer. • Yağlar karbonhidrat ve proteinlerle bileşik oluştururlar. • Glikolipid ve lipoprotein gibi.. • Yağların ayıracı Sudan III ‘dür. • Yağ + Sudan III Kırmızı – kahverengi renk verir. • Proteinler • • • • • Et, tavuk, yumurta, balık, süt ve süt ürünleri başlıca protein kaynaklarıdır. Yapılarında C – H – O ve N içeren bileşiklerdir. N proteinleri diğer organik bileşiklerden ayıran karakteristik elemandır. Proteinlerin hidrolizi ile oluşan monomeri amino asit adını alır. Amino asitlerin dehidrasyonu ile protein sentezlenir. Peptid bağı aa aa H2 O aa + (n) aa aa H2 O H2 O Dehidrasyon Protein (polipeptid) Hidroliz Radikaller (değişken gruplar) R1 NH2 Amino grubu C COOH Karboksil grubu R2 • Amino Asitlerin Genel Formülü R1 NH2 C Peptid bağı 1. Amino asit H N COOH R2 R1 C H R2 H2 O Dehidrasyon 2. Amino asit • İki Amino Asitin Birleşmesi COOH • Canlılarda bulunan 20 çeşit aa’ den bazıları (12) vücut tarafından sentezlenir. Bunlara temel olmayan aa’ ler denir. • Geri kalanı ise vücut tarafından sentezlenmez ve temel aa’ ler adını alır. Besinler yolu ile alınır. • Canlılarda 20 çeşit aa olduğu halde protein çeşidi sonsuzdur. • Protein Çeşitliliğinin Sebepleri • • • • Bir protein molekülünde yer alan aa sırası Bir protein molekülünde yer alan aa çeşidi Bir protein molekülünde yer alan aa sayısı Değişirse sentezlenen proteinde farklı olur. aa1 + aa2 + aa3 + aa4 + aa5 A Proteini aa1 + aa3 + aa2 + aa4 + aa5 B Proteini (Sırası) aa1 + aa2 + aa3 + aa3 + aa5 C Proteini (Çeşidi) aa1 + aa2 + aa3 + aa4 D Proteini (Sayısı) aa1 + aa2 + aa3 + aa4 + aa5 + aa6 E Proteini (Sayısı) • Proteinler vücutta yapısal ve işlevsel olarak görev yapar. • Yapısal olarak; • Hücre zarlarının bileşiminde, DNA’ ın etrafında, birçok organelin yapısında, kanın bileşiminde, kasların yapısında, derinin etrafında, saç tırnak gibi birçok yapıda ayrıca tüm antikorlar ve bazı hormonlarda proteindir. O halde proteinler canlıda en fazla bulunan organik bileşiklerdir. • İşlevsel olarak ise metabolizmada rol oynayan işlevsel proteinler yani enzimlerdir. • Enerji hammaddesi olarak proteinler en son tercih edilir. Çünkü vücutta hem yapısal hem de işlevsel olarak görev yaparlar. Proteinler enerji hammaddesi olarak ya vücuda fazla alındıklarında ya da uzun süren açlık hallerinde kullanılırlar. • Protein ayraçları • Protein + Millon • Protein + Fehling Kırmızı renk verir. Menekşe rengi oluşur. Amino grubu NH2 NH3 R1 Karboksil grubu C R2 COOH Enerji üre ürik asit İdrar • Amino asitlerden azotlu bileşikler ve enerji üretimi Bir amino asidin hücrede izlediği yol; • Protein sentezine girer. • Farklı bir amino aside dönüşür. • Enerji hammaddesi olarak ve protein olmayan azotlu bileşiklerin yapımında kullanılır. (özellikle fazla olan amino asitler için) • Amino asitlerin amino (N) grupları karaciğerde amonyak üre ve ürik aside çevrilerek idrarla dışarı atılır. Geri kalan C-H-O bölümü ise karbonhidratlara dönüşerek enerji hammaddesi olarak kullanılır. • Enzimler • Metabolizmada gerçekleşen tüm reaksiyonlar kimyasaldır. Metabolizma canlı hücrede geçtiğine göre bu reaksiyonlar Biyokimyasal Reaksiyon adını alır. • Anabolizmada gerçekleşen biyokimyasal reaksiyonlara Anabolik reaksiyon denir. • Katabolizmada gerçekleşen biyokimyasal reaksiyonlara ise Katabolik reaksiyon denir. • Vücudun dışında kimyasal reaksiyonlar yüksek sıcaklıkta, kuvvetli asit veya bazik ortamlarda gerçekleşebilir. • Ancak bu özelliklere sahip ortamlardan hücre zarar görür. • O halde ister katabolik ister anabolik olsun tüm biyokimyasal reaksiyonlar canlı hücreye zarar vermeden gerçekleşmelidir. • Bu da enzimler sayesinde olur. • Enzimler reaksiyonların gerçekleşmesi için gerekli olan aktifleşme enerji sini azaltarak hücrenin zarar görmesini engellerler . • Aktifleşme enerjisi bir molekülün diğer bir molekülle reaksiyona girmesi veya bir molekülün parçalanması için gerekli olan minumum enerji miktarıdır. • Enzimlerin Aktifleşme Enerjisini Azaltması • Örneğin ; H2O2 (hidrojen peroksit) hücrede metabolizma sonucu oluşan zehirli bir maddedir ve hemen parçalanması gerekir. Bu maddeyi cansız ortamda hücre dışında da parçalamak mümkündür. • Hücre Dışında: H2O2 MnO2 18000 cal • Hücre İçinde: H2O2 Katalaz 5500 cal MnO2 (katalizör) H 2 O + ½ O2 Katalaz (enzim) H2O + ½ O2 • İki reaksiyon arasındaki farka bakıldığında aktifleşme enerjisinin enzim varlığında azalmasıdır. • O halde enzimler aktifleşme enerjisini azaltarak biyokimyasal tepkimelerin hücreye zarar vermeden gerçekleşmesini sağlarlar. 18000 Aktifleşme enerjisi Enzim yok 5500 Enzim var H2O + ½ O2 Enerji cal. Tepkimenin ilerlemesi • Enzimlerin Aktifleşme Enerjisini Azaltması • Bu reaksiyonlarda görülen diğer bir farkta, aktifleşme enerjisinin hücre dışında katalizörle hücre içinde ise enzimle sağlanmasıdır. • Katalizör nedir? X maddesi herhangi bir katalizör olsun. A + B C X X C + X A + B + X veya • Katalizörler; • Aktifleşme enerjisini azaltırlar. • Tepkimeleri başlatmaz ancak tepkimelerin süresini kısaltarak tepkime hızını artırırlar. • Genellikle tepkimeleri çift yönlü katalizler. • Tepkime esnasında yapılarında değişme olmaz. Bu nedenle tekrar tekrar kullanılırlar. • Enzimlerde katalizörlerle aynı özellikleri taşır. O halde enzimler canlı hücrelerde sentezlenen doğal katalizörlerdir. • Enzimlerin Yapısı • Enzimler Basit ve Bileşik Enzim olarak ikiye ayrılır. • Basit enzimler sadece proteinden oluşur ve Apoenzim adını alır. • Apoenzimler genellikle tek başlarına çalışmazlar. Yapılarına yardımcı bir molekül ekleyerek aktif enzim (Holoenzim) yani bileşik enzim haline gelirler. • Bileşik enzimlerde, yardımcı molekül iki türlü olur. • Koenzim (organik) • Kofaktör (inorganik) • Koenzimler protein olmayan bir organik maddedir. Genellikle vitaminlerdir. • Kofaktörler ise Fe, Mn, Mg, Zn, Na, K gibi inorganik maddelerdir. • Bir apoenzim ya koenzimle ya da kofaktörle çalışır. Apoenzim (protein) + Koenzim Bileşik enzim (Holoenzim) Kofaktör (tam – aktif enzim) • Bir yardımcı molekül farklı apoenzimlerle çalışır. • Bir apoenzim aynı yardımcı molekülle çalışır. • Bu nedenle yardımcı molekül çeşidi apoenzim çeşidinden daha azdır. + Apoenzim Ko enzim (veya) Ko + faktör Holoenzim (Bileşik enzim) (tam – aktif enzim) • Enzimlerin Çalışması • Enzimin etki ettiği maddeye substrat denir. Enzimin substratı tanımladığı yer aktif bölge adını alır. Aktif bölge ile substrat arasında anahtar – kilit uyumu vardır. Substrat aktif bölgeye geçici olarak bağlanır. Enzim – substrat kompleksi oluşur. Tepkime gerçekleşir. Tepkime sonunda yeni ürün meydana gelir. Enzim serbest hale geçer. Enzim + Substrat Enzim – Substrat Kompleksi Enzim + Yeni Ürün Substrat Aktif bölge + Enzim Enzim – Substrat Kompleksi Enzim Yeni Ürün • Enzim Özgüllüğü • Hücrede bir çeşit enzim bulunmaz ve her enzim DNA’ da bulunan farklı genler tarafından üretilir. Bu durumda her enzimin etki ettiği substrat diğerinden farklıdır. Buna göre her enzim ayrı bir biyokimyasal tepkimeyi katalizler buna Enzim Özgüllüğü denir. • Enzim özgüllüğü sayesinde biyokimyasal tepkimeler birbirine karışmadan düzenli bir şekilde gerçekleşir. • 1 Gen = 1 Enzim • Metabolik reaksiyonlar DNA ‘da yer alan genler tarafından üretilen enzimlerle (protein) kontrol edilir. • O halde 1 gen = 1 enzimdir. • 1 Gen = 1 Enzim G1 E1 A G2 G3 DNA E2 E3 E1 G1 B E2 G2 C E3 G3 D E4 G4 E • Enzimler genellikle takım halinde çalışırlar. • Bir tepkime sonucunda oluşan ürün diğer tepkimede etkili olan enzimin substratıdır. • Bir enzimin yapısının bozulması tepkimenin durmasına yol açar. • Örneğin E3 bozulursa tepkime C’ de durur. Yani ortamda C maddesi birikir, D maddesi oluşmaz. Enzimler farklı çünkü enzimi üreten genler farklıdır. • Enzimatik Reaksiyonların Hızını Etkileyen Faktörler 1. Enzim yoğunluğu 2. Substrat yoğunluğu 3. Sıcaklık 4. Substrat yüzeyi 5. pH 6. Su 7. Kimyasal maddeler (Aktivatör – İnhibitör ) • Enzim Yoğunluğu • Substrat miktarının sabit olduğu bir ortama enzim ilavesi yapılırsa tepkime hızı artarak devam eder. • Substrat sabit Tepkime hızı • Çünkü substrat molekülleri boş kalmaz. • Ortamda substrat bitince reaksiyon sonlanır. Enzim yoğunluğu • Enzim sabit • Substrat Yoğunluğu Tepkime hızı • Enzim miktarının sabit olduğu bir ortama substrat ilavesi yapılırsa tepkime hızı bir süre artar sonra sabit bir hızla devam eder. • Çünkü her substrat molekülü için enzim bulunmaz. Substrat yoğunluğu • Sıcaklık Tepkime hızı • Sıcaklık artışı bir dereceye kadar tepkime hızını artırır. o Optimum sıcaklık 37 C • Ancak yüksek sıcaklık enzimin protein yapısını bozar ve enzim çalışmaz. Buna Denaturasyon denir. • Eğer enzimin yapısı bozulmadan sıcaklık normale getirilirse enzim çalışmaya devam eder. Buna da Sıcaklık 0 10 20 30 o 40 50 Renaturasyon denir. C • Düşük sıcaklıkta enzimler • Enzim çalışmaz. • Enzim çalışmaz. çalışmaz ancak yapıları (yapısı bozulmaz) (yapısı bozulur) bozulmaz. • Substrat Yüzeyi • Enzimler etkilerini substrat yüzeyinden başlatırlar. O halde; • Substrat yüzeyi arttıkça enzimin etki yüzeyi artar. Tepkime hızı artar. • Enzim sabit Tepkime hızı Enzim s s s s Substrat I II Substrat yüzeyi • pH • Genellikle enzimler nötr ortamda etkili olurlar. Bazı enzimler asidik bazıları da bazik ortamda çalışırlar. Tepkime hızı Pepsin Amilaz Tripsin pH 1 7 14 • Su • Enzimlerin çalışması için mutlaka ortamda su bulunmalıdır. Ortamdaki su miktarı % 15 olursa enzim çalışmaz. • Tohumlarda bu miktar % 5’ e kadar iner. Enzimler çalışmadığından tohumda uzun süre dayanır. • Kimyasal Maddeler • Kimyasal maddelerin bir kısmı reaksiyonları hızlandırır. Bunlara Aktivatör madde denir. (Ca, K, KCl) • Bazıları ise durdurur ve İnhibitör madde adını alır. (Kurşun, civa, siyanür, bakır, alüminyum gibi..) • Örneğin siyanür solunum enzimlerine bağlanır. Enzim çalışmaz. • Enzimler hücre içinde ,hücre dışında ve uygun koşullar sağlandığında cansız ortamlarda da çalışabilir. • Karaciğerde bulunan Katalaz enzimi karaciğerde oluşan H2O2‘ i (hidrojen peroksit) etkisiz hale getirir. Bütün karaciğer su o 35 C A Kıyılmış karaciğer su su o 60 C B Doğranmış karaciğer o 0 C C • Eşit miktarlarda karaciğerin bulunduğu bu üç sistemden hangisinde enzimatik reaksiyon meydana gelir? Neden. • Hangi sistemde sıcaklık normale getirilirse tepkime devam eder? • Nükleik Asitler • Yapısı • Nükleik asitlerin yapısal birimleri Nükleotid adını alır. • Bir nükleotid üç farklı maddeden oluşur. (5C) (N) Organik Baz + Şeker + Fosfat = Nükleotid +++++ (n) = Nükleik asit (polinükleotid) Dehidrasyon Nükleozit P B PURİN (ÇİFT HALKA) ADENİN (DNA-RNA) PURİN GUANİN (DNA-RNA) BAZLAR (N) PİRİMİDİN (TEK HALKA) CİTOZİN (DNA-RNA) TİMİN (DNA) URASİL (RNA) • Bir nükleotidin değişken grubu bazlardır. • Bu nedenle nükleotidler içerdikleri baz çeşidine göre adlandırılır. PİRİMİDİN O O P H O H DEOKSİRİBOZ (DNA) ŞEKER ( 5C ) RİBOZ (RNA) O H FOSFAT (DNA – RNA) H3PO4 (Fosforik Asit) Nükleik Asitler DNA (Deoksiribonükleik asit) Kalıtım maddesi Üç çeşit RNA bulunur. • mRNA (elçi - haberci) : DNA dan aldığı bir proteine ait bilgiyi ribozoma götürür. • tRNA (taşıyıcı): Sitoplazmadan aldığı aminoasitleri protein sentezinde kullanılmak üzere ribozoma taşır. • rRNA (ribozomal): Ribozomun yapısına katılır. RNA (Ribonükleik asit) Protein sentezi 1 GEN = 1 ENZİM GEN GEN a.a tRNA mRNA mRNA Ribozom DNA Protein İşlevsel Yapısal (enzim) Metabolizma DNA Ve RNA Arasındaki Farklar DNA RNA ADENİN VAR VAR GUANİN VAR VAR CİTOZİN VAR VAR TİMİN VAR YOK URASİL YOK VAR VAR YOK RİBOZ YOK VAR FOSFAT (FOSFORİK ASİT) VAR VAR İPLİK SAYISI (POLİNÜKLEOTİD) İKİ BİR REPLİKASYON VAR YOK GÖREVİ KALITIM MADDESİ PROTEİN SENTEZİ ÇEKİRDEK KLOROPLAST MİTOKONDRİ ÇEKİRDEK KLOROPLAST MİTOKONDRİ RİBOZOM BAZLAR (N) PURİN ÇİFT HALKA PRİMİDİN TEK HALKA ŞEKER (5C) DEOKSİRİBOZ HÜCREDE BULUNDUĞU YER • DNA Molekülünün Özellikleri I • • • • • DNA iki polinükleotid zincirinden oluşur. İki zincir saat yönünde dönümler yaparak sarmal yapıyı oluşturur. (Paketleme ) Her bir zincirin omurgasını Fosfat ve Şeker oluşturur. P ve şeker arasında fosfodiester bağları bulunur. Bir P iki ayrı nükleotidin şekeri ile bağ yapar. Baz ile şeker arasındaki bağlarda glikozid bağ adını alır. Bu şekilde nükleotidler alt alta bağlanarak zincir yapısı oluşur. • • • • • • İki zincir birbirine bazlar arasındaki Hidrojen bağlarıyla bağlanır. Bir DNA molekülünde purin bazı pirimidin bazı ile A bazı T bazı ile G bazı C bazı ile birleşir. Sonuç olarak bir DNA molekülünde; Purin = Pirimidin A=T G=C olur. • • • DNA Molekülünün Özellikleri II • • A – T arasında 2H bağı G – C arasında 3H bağı bulunur. • DNA molekülünün çapı tüm zincir boyunca sabittir. • (Çünkü iki halka tek halkayla bağ kurar.) • • • DNA doğada kendini eşleme yeteneğine sahip tek moleküldür. Bu sayede kalıtsal bilginin, dölden döle ve bir bireyde bir hücreden diğer hücreye sabit bir şekilde geçmesi sağlanmış olur. DNA’ nın iki zinciri birbirinin tamamlayıcısıdır. Fosfodiester bağı Glikozid bağ • Hidrojen bağı DNA • DNA Replikasyonu • Replikasyon esnasında DNA nın iki ipliği birbirinden ayrılır. • Her bir iplik kendini eşler. • Bölünme sonucu oluşan hücrelerde bir yeni bir eski iplikten oluşan DNA yer alır. • Bu nedenle DNA eşlenmesi Yarı Korunumlu Eşleme şeklinde gerçekleşir. Yeni iplik Eski iplik T C G T C G T T C G T C G T — — — — — — — A G C A G C A A G C A G C A — — — — — — — T C G T C G T A G C A G C A • DNA Replikasyonu (Yarı korunumlu eşleme) T C G T C G T — — — — — — — A G C A G C A • Vitaminler • Vücutta düzenleyici olarak görev yaparlar. Genellikle enerji metaboliz masında rol oynayan koenzimlerin yapısına girerler. İkiye ayrılırlar. • Yağda Eriyen Vitaminler : ( A – D – E – K ) vitaminleri. Vücutta depo edilirler. • Suda Eriyen Vitaminler: ( B grubu – C ) vitaminleri . Fazlası idrarla dışarıya atıldığı için günlük alınması gerekir. Depo edilmezler. • A Vitamini • Büyüme ve gelişmeyi sağlar. Görme pigmentlerinin yapısına katılırlar. • Eksikliğinde: Gece körlüğü ve enfeksiyonlarda vücut direncinde azalma görülür. • Kaynakları: Balık yağı - tereyağı – havuç -yumurta sarısı ve karaciğerdir. • D Vitamini • Kalsiyum ve fosforun emilimi ve kemiklerde depo edilmesini sağlar. • Eksikliğinde: Çocuklarda raşitizm büyüklerde osteomalazi oluşur. • Kaynakları: Balık yağı – özellikle güneş ışığıdır. • E Vitamini • • • Üreme ve hücrelerin yenilenmesi için gereklidir. Eksikliğinde; Kısırlık meydana gelir. Kaynakları: Tahıllar - bitkisel yağlar ve yeşil bitkilerdir. • K Vitamini • • • • Kanın pıhtılaşmasında etkilidir. Kalın bağırsaktaki bakteriler tarafındanda üretilir. Eksikliğinde; Kan pıhtılaşmaz. Fazla antibiyotik kullanıldığında bakteriler ölür ve K vitamini eksikliği meydana gelir. Kaynakları: Balık - et - süt ve yeşil yapraklı sebzelerde bulunur. • Suda Eriyen Vitaminler • • • Genel olarak vücudun karbonhidrat, protein ve yağ metabolizmasında görev alırlar. Bu vitaminler (B1 - B2 -B3 -B5 - B6 - B9 -B12) Isıya karşı duyarlıdırlar. • B1 (Tiamin) • • Kaynakları: Tahılların kepek kısmında ve bira mayasında bulunur. Eksikliğinde: Beriberi hastalığı oluşur. (Karbonhidrat metabolizması yavaşlar sinirsel faaliyetlerde bozulmalar.) • B2 (Riboflavin) • • Besinlerden enerji elde edilmesinde görevlidir. Görme olayında etkilidir. Demirin emilmesini kolaylaştırır. Eksikliğinde; Kansızlık - ciltte beyazlıklar - yaralar ve sinirsel bozukluklar görülür. • B3 (Niasin) Besinlerden enerji elde edilmesinden görevlidir. Eksikliğinde; Pellegra hastalığı görülür. Pellegra Hastalığı: Sinir sisteminde bozukluklar, davranış anormallikleri, sindirim sistemi bozuklukları ve deride yaralar görülmesi durumudur. • • • • B5 (Pantotenik asit) • • Besinlerden enerji elde edilmesinden görevlidir. Eksikliğinde; deride yaralar, saç renginin değişmesi, saç dökülmesi ve sinirsel bozukluklar görülür. • B6 (Piridoksin) • • • Besinlerin enerji elde edilmesinden görevlidir. Hemoglobin sentezi için gereklidir. Eksikliğinde; Anemi - merkezi sinir sistemindeki düzensizlikler sonucu havaleler ve ciltte yaralar görülür. • B9 (Folik Asit) • • • Kemik iliğinde kan hücrelerinin üretiminde görevlidir. Aminoasit ve protein metabolizması için gereklidir. Eksikliğinde; Kansızlık – yorgunluk ve baş ağrısı görülür. Kaynakları: Özellikle koyu yeşil yapraklı sebzeler. • B12 (Siyanokobalamin) • Kan yapımı için gereklidir. • Eksikliğinde; Kansızlık – yorgunluk ve çarpıntı görülür. • Kaynakları: Karaciğer – et – süt – balık ve yumurta. • B grubu vitaminleri genel olarak; • Tahılların kabuklarında et – süt – karaciğer – yumurta – fındık – dalak ve ıspanakta bol miktarda bulunur. • C Vitamini • • • • Bağ dokunun kollogen liflerinde bulunan proteinlerin üretimi için gereklidir. Aminoasit metabolizması ve folik asidin etkin hale geçmesinde görevlidir. Eksikliğinde; iskorpit (diş eti kanaması) görülür. Kaynakları: Kırmızı biber – yeşil biber – portakal – limon ve domates gibi besinlerde C vitamini bol miktarda bulunur. Vitamin Eksikliğinde Oluşan Hastalıklar A Gece körlüğü B Beriberi, pellegra C İskorpit, yaraların geç iyileşmesi D Çocuklarda raşitizm, erginlerde osteomalazi E Kısırlık K Kanın pıhtılaşmaması • İnorganik Bileşikler • Su • Mineraller • Asitler • Bazlar • Tuzlar • Eritici özelliğe sahiptir. • Hidrolizde rol oynar. • Enzimlerin çalışması için gereklidir. • Madde taşınmasında ve vücutta oluşan zehirli maddelerin • Suyun Özellikleri seyreltilmesinde rol oynar. • Buharlaşma özelliği ile suyun gaz haline gelmesini yani terleme ile vücut ısısının dengelenmesini sağlar. • Su zor şekil değiştirir (geç soğur, geç ısınır) Bu şekilde ısının dengelenmesinde rol oynar. • Suyu oluşturan bağlar kovalent bağlardır. • Su iki kutupludur. H (+) O (-) H2O • Mineraller ( Ca – I – Fe – Na – K – S – F – P – Cl) • • • • • • • Hidrolize uğramazlar. Enerji vermezler. Yapıcı ve onarıcıdırlar. Enzimlerin yapısına kofaktör olarak katılırlar. (Düzenleyici) Kas kasılmasında ve sinirsel iletimde rol oynarlar. Kanın ozmotik basıncının ve pH’ın dengelenmesinde etkili olurlar. Vücuttan çeşitli yollarla (idrar – ter – dışkı) atıldıklarından devamlı olarak besinlerle alınmaları gerekir. • Asitler - Bazlar -Tuzlar • • • Suyun iyonlarına ayrılması ile H (+) ve OH (-) oluşur. Çözeltilerde hangisi fazla olursa ortam asit veya bazik özellik kazanır. H fazla ise asidik. OH fazla ise bazik olur. Eşitse ortam nötr olur. • Önemleri • • Canlılar belli pH değerinde yaşarlar. Çünkü enzimler belirli pH değerlerinde etkili olurlar. İnsanda pH 7.4 tür. 7 veya 7. 8 olması ölümle sonuçlanır. • Tuzlar • Tuzlar asitle bazın tepkimeye girmesi ile oluşur. • Hücrede iyon şeklinde bulunur. • Örneğin NaCl hücrede su ve pH’ın dengelemesini sağlar.