GENİŞLEMİŞ
SPEKTRUMLU
BETA-LAKTAMAZ
OLUŞTURAN
ESCHERİCHİA
COLİ
SUŞLARINDA
İKİ
FARKLI
YÖNTEMLE
BİYOFİLM ARAŞTIRILMASI
Brian Roy Ives, Elmas Tohumoğlu, Atike Gül, Nuh Can Koçak, Özen Taş,
Damlasu S. Bağcaz
Danışman: Doç. Dr. Müge Demirbilek
ÖZET
Bu çalışmada GSBL pozitif Escherichia coli suşlarında biyofilm oluşum
oranlarının görülmesi ve iki farklı yöntemin kıyaslanması amaçlanmıştır.
GSBL pozitif suşlardan biyofilm oluşumunu araştırmak için modifiye
Christiensen mikroplak yöntemi ve BioTimer yöntemi kullanılmıştır.
Mikroplak yönteminde triptik soy buyyonda üreyen bakterilerin 96
kuyucuklu U tabanlı plaklarda biyofilm oluşturması sağlanmıştır. Sonuçlar
24 saat sonra spektrofotometrik olarak değerlendirilmiş, optik
yoğunluklarına (OD) göre kantitasyonu yapılmıştır.
BioTimer yönteminde triptik soy buyyonda bakteri süspansiyonu
hazırlanmış cam boncuklar üzerinde biyofilm oluşturulmuştur. Daha sonra
bu boncuklar BioTimer-Fenol kırmızısı(BT-PR) besiyerine aktarılmıştır. Bu
besiyerinde 24 saat inkübasyondan sonra biyofilm oluşumu; renk
değişikliğine göre değerlendirilmiştir.
Tüm deneyler 3 kere tekrarlanmış ve biyofilm oluşumu bilinen standart
Enterococcus faecalis suşu çalışmaya dahil edilmiş ayrıca her plakta en az
3 negatif kontrol denenmiştir.
Mikroplak yönteminde negatif cutoff esaslı değerlendirme yapıldığında
suşların %68’nin BioTimer yöntemi ile %74’nün biyofilm oluşturduğu
görülmüştür. BioTimer yönteminin Duyarlılığı %100, Özgüllüğü %81.2,
Pozitif prediktif değeri %91.8, Negatif prediktif değeri %100 bulunmuştur.
Çalışmamıza göre GSBL pozitiflik oranları oldukça yüksektir. Bu suşlar ile
oluşan enfeksiyonların tedavisinin daha zor olduğu unutulmamalı ve birinci
tercih ilaç olan karbapenemlerin biyofilmler üzerine etkisine bakılmalıdır.
Cam boncuklarda biyofilm oluşturma temeline dayalı BioTimer yönteminin
E.coli suşları için uygun olduğu görülmüş ve ileri biyofilm duyarlılık
araştırmalarında büyük kolaylık sağlayacağı düşünülmüştür.
Anahtar Kelimeler: Escherichia coli, biyofilm, biotimer yöntemi, GSBL
GİRİŞ
Bakterilerde antibiyotiklere direnç gelişmesi ile antibiyotik kullanımı
arasında doğrudan bir ilişki vardır. Antibiyotik kullanımının çok fazla olması
nedeniyle hastaneler, bakterilerde antibiyotik direncinin ortaya çıkması ve
yayılması için en uygun ortamlardır. Hastane enfeksiyonlarında da
saptanan etkenlerdeki antibiyotiklere direnç oranı, hastane dışında
saptanan etkenlere göre daha yüksektir. Bakterilerde antibiyotik direncinin
başta gelen nedenlerinden biri olan beta-laktamaz üretimi, endişe verici
bir hızla yayılmakta ve çeşitlenmektedir. Öte yandan nozokomiyal
1
etkenlerde başta olmak üzere, plazmidler yoluyla bakteriden bakteriye
direnç aktarımı beta-laktamazların yaygınlığına katkıda bulunmaktadır.
Beta-laktamazlar arasında TEM ve SHV grubu enzimler, klinik mikrobiyoloji
laboratuvarlarında sık soyutlanan türlerde yaygın olmaları ve plazmidlerce
taşınmaları nedeniyle klinik önem açısından ön plandadır. TEM-1 TEM-2 ve
SHV-1 beta-laktamazları, penisilinler ve 1.kuşak sefalosporinleri etkin bir
biçimde parçaladıkları halde; sefalotaksim, seftazidim ve aztreonam gibi
geniş spektrumlu beta laktamlara kısıtlı etki gösterirler. Ana enzimleri
kodlayan genlerdeki nokta mutasyonlara bağlı olarak yeni enzimler
gelişmiştir. Geniş spektrumlu beta laktam ajanları inaktive edebildikleri
için genişlemiş spektrumlu beta-laktamaz(GSBL) olarak adlandırılmıştır.
GSBL, en sık Klebsiella pneumoniae Escherichia Coli suşlarında
bulunmakta ve bu türler ile oluşan enfeksiyonların tedavisinde sorun
yaratmaktadır(3).
GSBL’ler sefotaksim, seftazidim, seftriakson gibi oksiimino betalaktamlara ve aztreonama direnç kazandıran ve genetik şifresi plazmid
üzerinden taşınan enzimlerdir. İlk olarak 1983 yılında Avrupa’da Klebsiella
pneumoniae
türlerine
karşı,
geniş
spektrumlu
beta-laktamların
kullanılmaya başlanmasından hemen sonra, tanımlanan bu enzimler, daha
sonra Enterobacteriaceae familyasının diğer üyelerinde de gösterilmiştir
(2,4).
Biyofilm, canlı veya cansız bir yüzeye yapışarak kendi ürettikleri
polisakkarid bir matriks içine gömülü halde yaşayan mikroorganizmaların
oluşturduğu topluluktur. Değişik mikrobial türlerin, kendilerini çevresel
etkenlerden korumak ve besin kaynağını daha verimli kullanmak için
oluşturdukları mikro-ekosistem olarak da tanımlanabilir. Biyofilmler;
kateterler, eklem ve kalp protezleri gibi kalıcı ya da kalıcı olmayan tıbbi
araçları veya kistik fibrozis gibi bazı hastalıklarda solunum yollarını
kolonize eden bakterilerin oluşturduğu bir mikroorganizma topluluğudur.
Biyofilmin büyük bir bölümünü oluşturan ekzopolisakkaritler (EPS)
savunmada önemli rol oynayan moleküllerdir. Ekzopolisakkaritler
bulunduğu bakteriyi enflamatuar hücrelerin fagositozundan ve antibiyotik
etkisinden korurlar. Bir biyofilmin yapısı %97 su olmak üzere %2-5
mikroorganizma, %1-2 polisakkarid, %1-2 protein, %1-2 DNA ve
iyonlardan oluşmaktadır. Sistemin yapısına, mikroorganizmanın türüne ve
çevresel faktörlere bağlı olarak olgun bir biyofilmin oluşması birkaç saat ile
birkaç hafta arasında zaman alır(7).
Bu çalışmada GSBL pozitif suşlarda biyofilm oluşum oranlarının görülmesi
E.coli ‘de daha önce hiç denenmemiş bir yöntem olan BioTimer yönteminin
denenmesi sonuçların geleneksel yöntemle kıyaslanarak, antibiyotik
duyarlılık çalışmaları için model oluşumunun sağlanması amaçlanmıştır
GEREÇ VE YÖNTEM
GSBL pozitifliği CLSI kriterlerine uygun olarak çift disk sinerji yöntemi ile
araştırılmıştır. Bu amaçla beta laktamaz inhibitörü olan klavulanik asit
içeren disklerin 2 santim uzağına sefotaksim, sefoksitin diskleri koyulmuş
ve aralarında sinerji görülenler yani inhibisyon zonunda genişleme olanlar
GSBL pozitif kabul edilmiştir(8).
2
GSBL pozitif suşlardan biyofilm oluşumunu araştırmak için Mikroplak
yöntemi ve BioTimer yöntemi kullanılmıştır. Mikroplak yönteminde Triptik
Soy Agar’da (TSA) 1 gece inkübe edilerek üretilmiş bakteriler 1-2 koloni
olacak şekilde %0.25 glikozlu Triptik Soy Broth’a (TSB) pasajlanmıştır. 1824 saat inkübasyon sonrasında üreyen bakteriler 1/100 oranında
sulandırılarak her bakteri 3 kuyucuğa denk gelecek şekilde mikroplaklara
dağıtılmıştır. Hazırlanan plaklar 24 saat etüvde inkübe edilmiştir.
Kuyucuklardaki besiyeri çok kanallı pipetle boşaltılarak pH 7.2 fosfat
tamponlu su (PBS) ile 3 kez yıkanacak, tüm yıkanmış kuyucuklara %1’lik
(w/v) 200 µl kristal viyole dağıtılmış, 20 dakika oda sıcaklığında bekleyen
mikroplaklar 3 kez suyla yıkanmıştır. Kuyucuklara, %80 etanol ve %20
aseton karışımı 200 µl eklenmiş ve spektrofotometrik olarak
değerlendirilmiştir. Optik yoğunluklarına (OD) göre 1+ ile 4+ arasında
biyofilm oluşturma kantitasyonu yapılmıştır.
BioTimer yönteminde cam boncuklar kullanılmıştır. Besiyeri olarak
BioTimer-Fenol kırmızısı (BT-PR) besiyeri kullanılmıştır. Bu besiyerinde
21gr MHB+10gr glikoz+25gr Fenol kırmızısı, 1lt distile suyla karıştırılıp,
pH’sı 7.2’ye ayarlanmış 121oC’de 15 dakika otoklavlanmıştır(8).
Biyofilm oluşum miktarını belirlemek için öncelikle E.coli’ye özel
korelasyon çizgisi elde edilmiştir. Bunun için cam tüplere 1’er ml BT-PR
besiyeri dağıtılmış, birinci tüpte McFarland 0.5 ayarlanıp 1/10 oranında
sulandırılmış BT-PR besiyerindeki bakteri süspansiyonu 1 ml eklenmiştir.
Seri dilüsyonlar hazırlandıktan sonra 37oC’de inkübe edilen tüplerde,
düzenli aralıklarla renk değişimi kontrol edilerek hangi dilüsyonda hangi
zamanda renk değişimi gerçekleştiği not edilmiştir. Eş zamanlı olarak her
dilüsyondan MHB besiyerine seri pasajlar alınarak bakteri kolonileri
sayılarak mililitredeki koloni oluşturan birim (Colony Forming Unit-CFU)’ler
hesaplanmıştır. Böylece zamana karşı logCFU/ml olacak şekilde korelasyon
eğrisi elde edilmiştir.
BioTimer yönteminde 2 mm çapındaki steril cam boncuklar üzerinde
bakterilerin biyofilm oluşturması sağlanmıştır. Suşların taze pasajları
%0.25 glikozlu TSB besiyerinde üretilmiş ve aynı besiyerinde 1/100
oranında sulandırılıp mikroplaklara dağıtılmış ve üzerlerine boncuklar
eklenmiştir. Her suş için 3 adet cam boncuk hazırlanmıştır. Daha sonra
37°C’de çalkalamadan bir gece inkübe edilerek biyofilm oluşturulmuş cam
boncuklar steril tuzlu su solüsyonunda 3 kere yıkanmış ve yapışmamış
hücreler ayrılmıştır. Her suş için biyofilm oluşturmuş 3 boncuk yıkama
sonrası BT-PR besiyerine aktarılmış ve 37o’de inkübe edilip renk değişikliği
kontrol edilmiştir. Renk değişikliği gözle değerlendirilmiştir.
İstatiksel değerlendirme; grup ortancalarının karşılaştırılmasında MennWhitney U testi kullanılmıştır. P<0.05 düzeyi istatiksel olarak anlamlı kabul
edilmiştir. İstatiksel analiz SPSS 17.0 istatiksel paket programında
yapılmıştır.
Bu çalışma Başkent Üniversitesi Tıp ve Sağlık Bilimleri Araştırma Kurulu
tarafından onaylanmış (Proje no:DA11/14) ve Başkent Üniversitesi
Araştırma Fonunca desteklenmiştir
3
SONUÇLAR
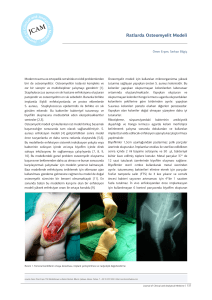
Çifti disk sinerjiyöntemi ile GSBL oluşturduğu saptanan 100 suş çalışmaya
dahil edilmiştir(Şekil 1)
Şekil 1. Çift dik sinerji yöntemi ile GSBL oluşturan E.coli suşu
Mikroplak yönteminde kullanılan plaklar sabit optik yoğunlukta (OD)
değerledirildiğinde OD<200 olan 90 suş biyofilm negatif, 200≤OD ≤400
olan 5 suş ve Entereccocus suşu biyofilm orta pozitif, OD>400 olan 5 suş
ise biyofilm kuvvetli pozitif olarak bulunmuştur(Şekil 3).
Her plak kendi içinde negatif kontrole göre değerlendirildiğinde OD ≤ ODNK
olan 32 suş biyofilm negatif, ODNK < OD ≤ (2xODNK) olan 55 suş biyofilm
zayıf pozitif, (2x ODNK) < OD ≤ (4x ODNK) olan 8 suş ve Entereccocus suşu
biyofilm orta pozitif, OD > (4x ODNK) olan 5 suş ise kuvvetli pozitif olarak
bulunmuştur.
Planktonik hücrelerde zamana karşı BT-PR besiyerinde renk değişimi
korelasyon eğrisi şekil 2’de verilmiştir.
Şekil 2. E.coli planktonik hücrelerinin BT-PR besiyerinde renk değişim zamanı ve bakteri
sayısı (logCFU/ml) korelasyon eğrisi
4
BioTimer yöntemi sonuçları ise gözle değerlendirilmiştir (Şekil 3).
Besiyerinde renk değişimi görülen kuyucuklar biyofilm pozitif, renk
değişimi olmayan kuyucuklar biyofilm negatif olarak saptanmıştır. Buna
göre suşların %74’ü biyofilm pozitif, %26’sı biyofilm negatif olarak elde
edilmiştir. Mikroplak yönteminde elde edilen OD değerleri ile Biotimer
testleri arasında istatiksel olarak güçlü bir ilişki olduğu görülmüştür (Tablo
1).
Şekil 3. E.coli suşlarının mikroplak yöntemi ve BioTimer yöntemi ile biyofilm oluşturmaları
Tablo 1. Mikroplak yönteminde elde edilen OD değerleri ile BioTimer yöntemi sonuçlarının
karşılaştırılması
Mikroplak Yöntemi
BioTimer Yöntemi
Pozitif
OD Medyan (min/max) 88.83 *
Çeyrekler arası sapma
(IQR)
*p<0.05
7.00*
(77.67/96.00)
BioTimer yöntemi
Negatif
158.21* (93.33/751.33)
53.00*
TARTIŞMA
GSBL
aracılı
direnç,
plazmidler
aracılığıyla
türler
arasında
aktarılabilmekte, hastanelerde salgınlar oluşturabilmekte ve mortalite
oranlarını arttırabilmektedir (4). GSBL direncini bakteriler arasında
taşıyan plazmidler, çoğunlukla diğer antibiyotiklere karşı direnci de
taşımaktadır (3). Bu enzimler geniş spektrumlu penisilinazların
türevleridir ve çoğu TEM ya da SHV enzimlerinden köken almaktadır (4).
Hibridizasyon deneyleri ile GSBL’lerin TEM-1, TEM-2 ve SHV-1 beta
laktamaz genlerinde meydana gelen basit nokta mutasyonları sonucunda
ortaya çıktığı saptanmıştır (1, 2).
Antibiyotiğin koruyucu dozları bu mikroorganizmaları kontrol ettiği halde
biyofilmi etkilemez. Kalıcı tıbbi cihazlar üzerinde gelişen biyofilmler sürekli
bir enfeksiyon odağı oluşturarak enfeksiyonun hematojen yolla yayılımı
açısından da her zaman bir risk kaynağı sayılmaktadır. Biyofilmin yapısının
ve
oluş
mekanizmalarının
daha
iyi
anlaşılması
muhtemelen
mikroorganizmaların potansiyel tedavi hedeflerini de ortaya çıkartacaktır.
5
GSBL pozitif suşlarda çoğu zaman tek antibiyotik seçeneği karpenemlaer
olarak karşımıza çıkmaktadır. Bu suşların aynı anda biyofilm oluşturması
ayrı bir problemdir. Çalışmamızda bu suşlarda yüksek oranda(%68, %74)
biyofilm oluşumu saptanmıştır.
E. coli’lerde biyofilm araştıran yeterli çalışma yoktur. Maya ve arkadaşları,
E. coli suşlarında %76.6 slime oluşumu ve suşların hidrofobisitesini %90
oranını saptamıştır. Bu iki faktörde biyofilm oluşumunda önemlidir(5).
Yapılan bir çalışmada E.coli izolatlarındaki biyofilm oluşum oranları,
patojen suşlarda çevre izolatlarına göre daha yüksek bulunmuştur(9).
Bizim çalışmamızda tüm suşlarımız klinik izolat olduğu için böyle bir
kıyaslama yapılmamıştır. Yang ve Zang(11) ise GSBL pozitif K.pneumoniae
suşlarında biyofilm oluşumunu (%82) negatiflere göre çok daha yüksek
oranda
(%13.4)
saptamıştır.
Çalışmamızda
GSBL
negatif
suş
kullanılmamıştır. GSBL pozitiflerde biyofilm oluşumu yüksek oranda
bulunmuştur. Bu diğer çalışmayla uyumlu ancak daha düşüktür. Bunun
sebebi bakterilerin farklı olmasına bağlanmıştır. GSBL pozitif E.coli’lerde
biyofilm araştıran çalışmaya ulaşılamamıştır. EAEC suşlarında (62 suş)
yapılan çalışmada 48 suşda (%77.4) biyofilm oluşumu saptanmış.
Çalışmamızdaki oranın bununla uyumlu olduğu görülmüştür(10). E.coli
suşlarında yapılan bir çalışmada; metod bağımlı (kullanılan besiyeri, süre,
hesaplama) olarak biyofilm oluşum oranlarının değişeceği bildirilmiştir(6)
ve bizim çalışmamızda da metoda bağlı olarak değişen %68 ve %74’lük
pozitif sonuç gözlemlenmiştir.
Mikroplak yöntemi çeşitli koşullardan etkilendiği için sabit OD ile
değerlendirmenin hata payı yüksek bulunmuştur. Negatif kontrol cutoff
esaslı değerlendirmeye göre mikroplak yöntemi ile karşılaştırıldığında
BioTimer yönteminin; duyarlılığı %100, özgüllüğü %81.2, pozitif prediktif
değeri %91.8 ve negatif prediktif değeri %100 olarak değerlendirilmiştir.
Değişik yüzeylerin biyofilm oluşumunu etkilediği görülmüştür. Yöntemler
arasındaki farklara değinilecek olunursa, E. coli’nin glikozu hızlı fermente
etmesi sebebi ile BioTimer yönteminde az sayıda bakteri yeterli iken,
Mikroplak yönteminde kuvvetli yapışma gerektiğinden dolayı, Biyofilmin
görünür hale gelmesi için çok sayıda bakteri gereklidir.
Çalışmamızda GSBL pozitif E.coli suşlarında yüksek oranda biyofilm
oluşumu saptanmıştır. Bu sonuçlar GSBL pozitif suşlarda ilk tercih olan
karbapenemlerin biyofilm üzerine etkisine bakılmasının tedavi başarısı
açısından önemli olduğunu düşündürtmüştür.
BioTimer
yöntemi
ile
tüm
boncuklarda
eşit
oranda
biyofilm
oluşturulduğunun gözlenmesi biyofilm duyarlılık çalışmaları açısından
önem
taşımaktadır.
GSBL
pozitif
E.coli
biyofilmlerine
karşı
karbapenemlerin etkinliğinin invitro ve invivo koşullarda araştırılması
başlıklı öğrenci projesi kapsamında yürüteceğimiz çalışma için yol gösterici
olmuştur.
Biyofilm araştırmalarında halen standart bir yöntem geliştirilmemiştir. Bu
çalışma E. coli suşlarında BioTimer yöntemi ile biyofilm araştıran ilk
çalışma olduğu için önemlidir. Çalışmamız bu yöntemin özellikle mikroplak
yönteminde saptanan OD değerleri ile kıyaslandığında güvenilir sonuçlar
verdiğini (p<0.05) göstermiştir.
6
KAYNAKLAR
1. Abdi-Ali A, Mohammadi-Mehr M, Alaei YA. Bactericidal activity of
various
antibiotics
against
biyofilm-producing
Pseudomonas
aeruginosa, International Journal of Antimicrobial Agents, 2006;
27(3):196-200.
2. Demir N. Gram negatif bakterilerde genişlemiş spektrumlu betalaktamaz (GSBL) üretimine katkıda bulunançeşitli risk faktörlerinin
araştırılması. Uzmanlık Tezi, 2006; Danışman: Serap Gençer. Dr. Lütfi
Kırdar Kartal Eğitim ve Araştırma Hastanesi, İnfeksiyon Hastalıkları ve
Klinik Mikrobiyoloji Kliniği.
3. Gür D:Beta-Laktamazlar,Flora 1997; 2 (Ek3)
4. Jacoby GA, Medeiros AA: More extended-spectrum beta-lactamases,
Antimicrob Agents Chemother. 1991; 35:1697.
5. Maya A.S et al. Phenotypic and Genotypic Characterization of
Extended Spectrum β- Lactamase Producing Escherichia coli Clinical
Isolates from Semiurban Area J Phar Res. 2011 4:4-10
6. Naves P, del Prado G et al. Measurement of biofilm formation by
clinical isolates of Escherichia coli is method-dependent. J Appl
Microbiol. 2008;105(2):585-90.
7. Olson ME, Ceri H, Douglas W. et.al. Biyofilm bacteria: formation and
comparative susceptibility to antibiotics, Can J Vet Res. 2002; 66(2):
86–92.
8. Pantanella F, Valenti P, Frioni A, Natalizi T, Coltella L, Berlutti F.
BioTimer Assay, a new method for counting Staphylococcus spp. in
biyofilm without sample manipulation applied to evaluate antibiotic
susceptibility of biyofilm. J Microbiol Methods. 2008; 75(3):478-84
9. Reisner A, Krogfelt KA et al. In vitro biofilm formation of commensal
and pathogenic Escherichia coli strains: impact of environmental and
genetic factors. J Bacteriol. 2006;188(10):3572-81.
10. Wakimoto N et al. Quantitative biofilm assay using a microtiter plate
to screen for enteroaggregative Escherichia coli. Am J Trop Med Hyg.
2004;71(5):687-90.
11. Yang & Zhang. Biofilm-forming Klebsiella Pneumoniae strains have
greater likelyhood of producing extended-spectrum β- Lactamases. J
Jhin. 2008; 369-371
7