Serbest
radikaller ve
reaktif oksijen
cisimleri
Yrd. Doç .Dr. Omca
DEMİRKOL
• Oksijen toksik bir gazdır. Bu
toksiditenin birincil sebebi oksijenin
hücre içi redüksiyonlarla oldukça
reaktif cisimlere veya serbest
radikallere dönüşmesidir. Ancak
serbest radikaller aerobik
metabolizmanın doğal bir ürünüdür.
• Hücre tarafından kullanılan oksijenin
2-3% si serbest radikallere
dönüştürülür.
• Organizmada normal metabolik
yolların işleyişi sırasında
• veya çevresel ajanlar (pestisidler,
aromatik hidrokarbonlar, toksinler,
çözücüler vb.), stres, radyasyon gibi
çeşitli dış faktörlerin etkisiyle serbest
radikaller meydana gelmektedir.
• Serbest radikaller dış orbitallerinde
ortaklanmamış elektron bulunduran,
kısa ömürlü, reaktif moleküllerdir.
• Serbest radikallerin en önemlileri
süperoksit radikali (O2 ●-), hidroksil
radikali (OH ●), singlet oksijen (1O2)
ve radikalik olmayan hidrojen
peroksit (H2O2) ve peroksinitrit
(ONOO-) dir.
• Hücrede oluşan reaktif oksijen türleri
(ROT), "antioksidan savunma
sistemleri" veya kısaca
"antioksidanlar" olarak bilinen
mekanizmalarla ortadan kaldırılırlar
• Ancak bazen hücresel savunma
mekanizması vasıtasıyla ortadan
kaldırılandan daha fazla ROT
oluşabilir. Organizmada Hücresel
savunma mekanizması vasıtasıyla
ortadan kaldırılandan daha fazla
ROT meydana gelmesi oksidatif
stres olarak tanımlanır.
• ROT’lar organizmada lipidler, nükleik
asitler, proteinler ve karbonhidratlar gibi
biyolojik moleküllerle kolayca reaksiyona
girebilirler. Bu yüzden yaşlanma, kanser,
kardiyovasküler hastalıklar, immün sistem
hastalıkları, katarakt, diyabet, böbrek ve
karaciğer hastalıkları gibi pek çok
hastalıktan sorumlu tutulurlar
• Oksitatif stres çalışmalarında serbest
radikallerin artışı veya antioksidan
savunma sistemlerinin yetersizliği
araştırılmaktadır. Bunun için plazma,
serum, eritrosit, doku örnekleri gibi
çeşitli materyallerde analiz yapmaya
uygun yöntemler geliştirilmiştir.
• Serbest radikaller son derece reaktif
ve kısa ömürlüdürler. Bu yüzden
direkt olarak ölçülmeleri zordur.
Serbest radikalleri direkt olarak ölçen
tek analitik teknik spin rezonans
spektrometresidir.
• Spin rezonans spektrometresi ileri
teknik donanım gerektirir, ayrıca çok
duyarlı olmaması ve mikromolar
düzeyde sabit konsantrasyonlarda
serbest radikaller gerektirmesi
nedeniyle kullanımı yaygın değildir.
• Serbest radikal üretimi artışının
belirlenmesi için bunların lipidlerle,
proteinlerle ve DNA ile reaksiyonları
sonucu oluşan çeşitli ürünlerin
ölçümü gibi indirekt yöntemler
kullanılır. Bu yöntemler arasında lipid
peroksidasyonunun son ürünlerinin
ölçümü en çok kullanılan yöntemdir.
Oksijen Toksisitesi
Oksijenin canlılardaki toksik
etkileri başlıca iki tür mekanizma
ile gerçekleşir:
Moleküler oksijenin bazı enzimleri
inhibe etmesi
Serbest oksijen radikalleri
Oksijen bazı enzimleri reaktif
türlerinden bağımsız olarak doğrudan
inhibe edebilir. Örneğin nitrojen
fiksasyonunu katalizleyen nitrojenaz
enzimleri ve CO2 fiksasyonunu
katalizleyen enzim olan ribuloz
bifosfat karboksilaz, oksijen
tarafından inhibe edilirler.
• Aerobik hayat için gerekli olan
oksijen molekülü solunum ve enerji
metabolizması için zorunlu olmasının
yanında birçok olumsuz sonuçlar da
meydana getirmektedir. Aerobik
organizmalar oksijenin bu olumsuz
etkileriyle de savaşmak
zorundadırlar.
• Fakat oksijenin esas toksik etkisi
reaktif türevlerinden
kaynaklanmaktadır. Oysaki bazal
düzeyindeki moleküler oksijen reaktif
değildir ve organik moleküllerle
rahatlıkla birlikte bulunabilir.
• Sadece insan ve diğer aerob canlılar
elekron transport zincirleri geliştirdiği
ve diğer enzim sistemleri bunu
kullandığı için oksijenin bu toksik
etkisini tolere edebilir.
• Bu özelliği, moleküler oksijenin
eşleşmemiş iki elektronunun paralel
dönmesiyle açıklanır ve bu dönme
sınırlaması radikal olmayan
bileşiklerle onun reaksiyona
girmesine etkili bir engel oluşturur.
• Bir serbest radikal herhangi bir
kimyasal yapıda (atom, iyon, veya
molekül) olabilir. Bu kimyasallar,
eşleşmemiş veya tek sayılı elektron
içerirler.
Radikaller Nasıl Oluşur?
Radikaller başlıca 3 temel mekanizma ile oluşur:
– Kovalent bağların homolitik kırılması ile: Yüksek
enerjili elektromanyetik dalgalar ve
yüksek sıcaklık (500-600 °C) kimyasal
bağların kırılmasına neden olur. Kırılma
sırasında bağ yapısındaki iki elektronun
her biri ayrı ayrı atomlar üzerinde
kalıyorsa, bu tür kırılmaya homolitik
kırılma denir ve her iki atom üzerinde de
paylaşılmamış elektron kalır. Organik
moleküllerdeki bağların heterolitik
kırılması durumunda zıt yüklü iyon çiftleri
oluşur ve bu türler de reaktiftir.
– Normal bir molekülün elektron kaybetmesi
ile: Radikal özelliği bulunmayan bir molekülden
elektron kaybı sırasında dış orbitalinde
paylaşılmamış elektron kalıyorsa, radikal formu
oluşur. Örneğin; askorbik asit, glutatyon ve
tokoferoller gibi hücresel antioksidanlar,
radikal türlere tek elektron verip radikalleri
indirgerken, kendilerinin radikal formu
oluşur.
Normal bir moleküle elektron transferi ile:
Örneğin, moleküler oksijenin tek elektron ile
indirgenmesi, radikal formu olan
süperoksidin oluşumuna neden olur.
• Son yıllarda oksijenden türemiş
serbest radiklaller ile çeşitli
hastalıklar arasındaki ilişki üzerine
yapılan çalışmaların sayısı giderek
artmaktadır.
• En basit serbest radikal hidrojen
elementinin bir atomudur. Serbest
radikal olarak sınıflandırılan hidrojen
atomu bir proton ve bir eşleşmemiş
elektron taşır.
Moleküler oksijenin
özellikleri
• Moleküler oksijen (O2), paralel spin
durumlu iki ortaklanmamış
(eşleşmemiş) elektrona sahiptir.
• Ortaklanmamış (eşleşmemiş) elektron
içeren atom, atom grubu veya moleküller
serbest radikal olarak tanımlanırlar.
• Serbest radikal tanımına göre moleküler
oksijen, bir biradikal (diradikal) olarak
değerlendirilir. Biradikal oksijen, radikal
olmayan maddelerle yavaş reaksiyona
girdiği halde diğer serbest radikallerle
kolayca reaksiyona girer.
• Ortaklanmamış (eşleşmemiş) elektron
içeren atom, atom grubu veya moleküller
serbest radikal olarak tanımlanırlar.
Ancak Fe3+, Cu2+, Mn2+ ve Mo5+ gibi geçiş
metalleri de ortaklanmamış elektronlara
sahip oldukları halde serbest radikal olarak
kabul edilmezler, fakat serbest radikal
oluşumunda önemli rol oynarlar.
• Serbest radikaller pozitif yüklü
(katyon), negatif yüklü (anyon) veya
elektriksel olarak nötral olabilirler.
• Bu maddelerin başka maddelerden
elektron kazanma eğilimi göstermesi,
maddeyi ileri derecede reaktif hale getirir.
• Bununla beraber singlet oksijen, H2O2 ve
NO gibi maddeler serbest radikal değildir.
• “Reactive Oxygen Species” terimi (ROS)
hem O2. – (süperoksid) ve OH. (hidroksil)
gibi serbest radikalleri hem de H2O2
(hidrojen peroksid) ve HOCl (hipokloröz
asit) gibi nonradikal oksijen derivelerini
tanımlar
Reaktif oksijen türleri
3 major tip ROT vardır. Bunlar:
• 1-Superoksit (O2•-),
• 2-Hidrojen perosit (H2O2)
• 3-Hidroksil (OH•)
Süperoksit
• Süperoksit, ATP üretimi sırasında
oluşur ve immün sistemde
üretildiğinde virüs, bakteri ve kanser
hücrelerini yok ettiği için faydalıdır.
• Büyük miktarda üretildiğinde ise lipit,
protein ve DNA hasarına neden olur.
Süperoksit radikali (O2⋅−)
• Süperoksit radikali (O2⋅−) hemen tüm
aerobik hücrelerde moleküler
oksijenin (O2) bir elektron alarak
indirgenmesi sonucu oluşur.
İndirgenmiş geçiş metallerinin
otooksidasyonu, süperoksit radikali
meydana getirebilir.
Elektron transfer reaksiyonlarıyla
oksidantların oluşumu
Süperoksit anyon radikali
• Süperoksit radikali kendisi direkt
olarak zarar vermez. Bu radikal
anyonun asıl önemi, hidrojen
peroksit kaynağı olması ve geçiş
metalleri iyonlarının indirgeyicisi
olmasıdır.
• Süperoksit radikali düşük pH
değerlerinde daha reaktifdir,
perhidroksi radikali (HO2•)
oluşturmak üzere protonlanır.
• Süperoksit radikali ile perhidroksi
(HO2•) radikali birbirleriyle
reaksiyona girince biri okside olur
diğeri indirgenir. Bu dismutasyon
reaksiyonunda moleküler oksijen ve
hidrojen peroksit meydana gelir.
• Süperoksit radikalinin fizyolojik bir serbest
radikal olan nitrik oksit (NO•) ile
birleşmesi sonucu bir reaktif oksijen türü
olan peroksinitrit (ONOO−) meydana gelir.
Peroksinitrit, nitrit (NO2−) ve nitrat (NO3−)
oluşturmak üzere metabolize edilir.
Peroksinitrit, azot dioksit (NO2•), hidroksil
radikali (OH•), nitronyum iyonu (NO2+)
gibi toksik ürünlere dönüşebilir ki nitrik
oksitin (NO•) zararlı etkilerinden
peroksinitrit sorumludur.
2-Hidrojen peroksit (H2O2)
• Süperoksitin dismutasyonu hidrojen
peroksit formasyonuyla sonuçlanır.
• Bazı oksidazlar direk olarak hidrojen
peroksitleri genere ederler.
Hidrojen peroksit (H2O2)
• Hidrojen peroksit (H2O2),
süperoksidin çevresindeki
moleküllerden bir elektron alması
veya moleküler oksijenin
çevresindeki moleküllerden iki
elektron alması sonucu oluşan
peroksitin iki proton (H+) ile
birleşmesi sonucu meydana gelir.
Hidrojen peroksit (H2O2)
• Biyolojik sistemlerde hidrojen
peroksidin asıl üretimi, süperoksidin
(O2⋅−) dismutasyonu ile olur. İki
süperoksit molekülü, süperoksidin
dismutasyonu reaksiyonunda iki
proton alarak hidrojen peroksit ve
moleküler oksijeni oluştururlar.
• Bu reaksiyon, radikal olmayan ürünler
meydana geldiğinden dismutasyon
reaksiyonu olarak bilinir, ya spontan
gerçekleşir ya da süperoksit dismutaz
(SOD) enzimi tarafından katalizlenir.
Spontan dismutasyon pH 4,8'de en
hızlıdır, enzimatik dismutasyon ise
spontan dismutasyonun nispeten yavaş
olduğu nötral ya da alkali pH'da daha
belirgindir.
• Hidrojen peroksit bir serbest radikal
olmadığı halde ROT kapsamına girer ve
serbest radikal biyokimyasında önemli bir
rol oynar. Çünkü Fe2+ veya diğer geçiş
metallerinin varlığında Fenton
reaksiyonu sonucu, O2⋅− varlığında
Haber-Weiss reaksiyonu sonucu en
reaktif ve zarar verici serbest oksijen
radikali olan hidroksil radikali (OH•)
oluşturur.
• Haber-Weiss reaksiyonu süperoksidin
direkt olarak H2O2 ile reaksiyonudur,
katalizörsüz reaksiyon oldukça yavaş
ilerler. Demirle katalizlenen ikinci
şekli ise çok hızlıdır. Bu reaksiyonda
önce ferri demir (Fe3+) süperoksit
tarafından ferro demire (Fe2+)
indirgenir. Sonra Fenton reaksiyonu
ile H2O2’den OH● ve OH- üretilir.
• Süperoksit radikalinin lipid solubilitesi
sınırlı olduğu halde hidrojen peroksit
lipid solubldur. Bu nedenle hidrojen
peroksit kendisinin oluştuğu yerden
uzakta olan fakat Fe2+ içeren
membranlarda hasar oluşturabilir.
Hidroksil iyonları
• Oldukça reaktif olan hidroksil iyonları
pürin ve pirimidinlerde değişikliğie
sebep olabilir, DNA iplikçiklerini
kırarak hasar oluşturur.
Hidroksil radikali (OH•)
• Hidroksil radikali (OH•) Fenton reaksiyonu
ve Haber-Weiss reaksiyonu sonucu
hidrojen peroksitten oluşmaktadır.
• Son derece reaktif bir oksidan radikaldir,
büyük olasılıkla ROT ların en güçlüsüdür.
Oluştuğu yerde tiyoller ve yağ asitleri gibi
çeşitli moleküllerden bir proton kopararak
tiyil radikalleri (RS•), karbon merkezli
organik radikaller (R•), organik peroksitler
(RCOO•) gibi yeni radikallerin oluşmasına
ve sonuçta büyük hasara neden olur.
• Suyun yüksek enerjili iyonlaştırıcı
radyasyona maruz kalması sonucu
da oluşur.
Singlet Oksijen (1O2)
• Moleküler oksijen (atmosferik
oksijen) dış orbitallerinde
paylaşılmamış iki elektron içerir. Bu
elektronlar, spinleri aynı yönde ve
farklı orbitallerde iken minimum
enerji seviyesindedirler.
• Diradikal oksijenin elektronlarından
birinin enerji alarak kendi spininin
ters yönünde olan başka bir orbitale
yer değiştirmesiyle singlet oksijen
oluşur. Singlet oksijen, eşleşmemiş
elektronu olmadığı için radikal
olmayan reaktif oksijen molekülüdür,
delta ve sigma olmak üzere iki şekli
vardır.
Singlet Oksijen
Delta O2
Sigma O2
O2
Moleküler oksijen
H2O + OH•
Hidroksil radikali
Süperoksit radikali
(süperoksit anyonu)
H2O2
Hidrojen peroksit
H2O
Su
Reaktif nitrojen cisimleri
(NOS)
• Nitrik oksit (NO), L-argininin Lcitrulin’e nitrik oksit sentaz
(NOS)tarafından enzimatik
dönüşümü sırasında sentezlenir
• Eşlenmemiş elektronuyla oldukça
yüksek reaktiviteye sahip olan NO,
protein, karbonhidrat, nükleotit ve
lipitlerde hasara neden olur.
• Bunun dışında hücre ve dokuları da
hasara uğratır.
Serbest oksijen
radikallerinin etkileri
• Reaktif oksijen türlerinin (ROT)
oluşumu enflamasyon, radyasyon,
yaşlanma, ozon (O3) ve azot dioksit
(NO2•), kimyasal maddeler ve ilaçlar
gibi bazı uyarıların etkisiyle artar.
• Serbest radikaller hücrelerin lipit,
protein, DNA, karbonhidrat ve enzim
gibi tüm önemli bileşiklerine etki
ederler.
• Süperoksit radikali (O2⋅−) ve hidroksil
radikali (OH•) sitoplazma,
mitokondri, nükleus ve endoplazmik
retikulum membranlarında lipid
peroksidasyonunu başlatır.
Membranlarda lipid peroksidasyonu
meydana gelmesi sonucu membran
permeabilitesi artar.
• Serbest radikallerin etkisiyle
proteinlerdeki sistein sülfhidril
grupları ve diğer amino asit kalıntıları
okside olarak yıkılır, nükleer ve
mitokondriyal DNA okside olur.
• Serbest oksijen radikallerinin tüm bu
etkilerinin sonucunda hücre hasarı
olur. Hücrede reaktif oksijen
türlerinin (ROS) ve serbest
radikallerin artışı hücre hasarının
önemli bir nedenidir
Serbest radikallerin lipidlere
etkileri
• Lipidler serbest radikallerin etkilerine
karşı en hassas olan
biyomoleküllerdir. Hücre
membranlarındaki kolesterol ve yağ
asitlerinin doymamış bağları, serbest
radikallerle kolayca reaksiyona
girerek peroksidasyon ürünleri
oluştururlar.
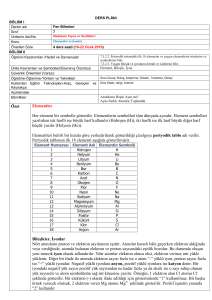
• Poliansatüre yağ asitlerinin oksidatif
yıkımı lipid peroksidasyonu olarak
bilinir.
• Lipid peroksidasyonu kendi kendini
devam ettiren zincir reaksiyonu
şeklinde ilerler ve oldukça zararlıdır
• Hücre membranlarında lipid serbest
radikalleri (L•) ve lipid peroksil
radikallerinin (LOO•) oluşması,
reaktif oksijen türlerinin (ROS) neden
olduğu hücre hasarının önemli bir
özelliği olarak kabul edilir.
• Serbest radikallerin sebep olduğu
lipid peroksidasyonuna
"nonenzimatik lipid
peroksidasyonu" denir.
• Hücre membranlarında lipid
peroksidasyonuna uğrayan başlıca yağ
asitleri poliansatüre yağ asitleridir. Lipid
peroksidasyonu genellikle yağ asitlerindeki
konjuge çift bağlardan bir elektron içeren
hidrojen atomlarının çıkarılması ve bunun
sonucunda yağ asidi zincirinin bir lipid
radikali niteliği kazanmasıyla başlar.
• Lipid radikali (L•) dayanıksız bir bileşiktir
ve bir dizi değişikliğe uğrar. Lipid
radikallerinin (L•) moleküler oksijenle (O2)
etkileşmesi sonucu lipid peroksil radikalleri
(LOO•) oluşur. Lipid peroksil radikalleri
(LOO•), membran yapısındaki diğer
poliansatüre yağ asitlerini etkileyerek yeni
lipid radikallerinin oluşumuna yol açarken
kendileri de açığa çıkan hidrojen
atomlarını alarak lipidperoksitlerine
(LOOH) dönüşürler ve böylece olay kendi
kendini katalizleyerek devam eder.
• Lipid peroksidasyonu sonucu oluşan lipid
peroksitlerinin (LOOH) yıkılımı geçiş
metalleri iyon katalizini gerektirir. Plazma
membranı ve subsellüler organel lipid
peroksidasyonu serbest radikal
kaynaklarının hepsiyle uyarılabilir ve geçiş
metallerinin varlığında artar. Lokal olarak
hidrojen peroksitten (H2O2) Fenton
reaksiyonu sonucu hidroksil radikali (OH•)
oluşması zincir reaksiyonunu başlatabilir.
• Lipid peroksitleri (LOOH) yıkıldığında
çoğu biyolojik olarak aktif olan
aldehitler oluşur. Bu bileşikler ya
hücre düzeyinde metabolize edilirler
veya başlangıçtaki etki alanlarından
diffüze olup hücrenin diğer
bölümlerine hasarı yayarlar.
• Üç veya daha fazla çift bağ içeren
yağ asitlerinin peroksidasyonunda
malondialdehit (MDA) meydana gelir.
Malondialdehit (MDA)
MDA
• Malondialdehit (MDA) kanda ve
idrarda ortaya çıkar, yağ asidi
oksidasyonunun spesifik ya da
kantitatif bir indikatörü olmamakla
beraber lipid peroksidasyonunun
derecesiyle iyi korelasyon gösterir..
• Stabil olmayan lipit peroksitlerinin
indirgenmiş ürünüdür. Bu lipit
peroksidasyon yan ürünü oksidatif
stresin neden olduğu lipit
peroksidasyon derecesini gösterdiği
için oksidatif stres çalışmalarında
ölçülür