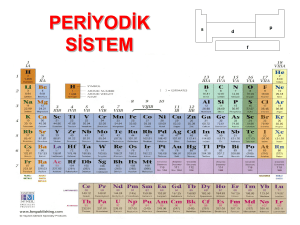
s, p, d Elementleri
Hidrojen
1A Grubu: Alkali metaller
2A Grubu: Toprak Alkali Metaller
3A Grubu: Toprak Metalleri
4A Grubu
5A Grubu
6A Grubu: Kalkojenler
7A Grubu: Halojenler
B Grubu: Geçiş Metalleri
f Elementleri
Lantanitler ve Aktinitler
Asal Gazlar
8A Grubu
ELEMENTLERİ TANIYALIM
Hidrojen (1𝒔𝟏 )
Hidrojen için periyodik tabloda tamamıyla uygun bir yer yoktur.
Geleneksel olarak 1A grubunda bulunur.
Alkali Metaller gibi s orbitalinde tek bir elektron vardır.
Bileşiklerinde (+1) ve (-1) değerlik alabilir.
İyonik hidritler suyla reaksiyona girerek hidrojen gazı ve metal hidroksit oluştururlar.
2NaOH (k) + 2H2O (s) → 2NaOH (suda) + H2 (g)
Hidrojenin en önemli bileşiği sudur.
2H2 (g) + O2 (g) → 2H2O (s)
ELEMENTLERİ TANIYALIM
1A Grubu Elementleri ( ns1 , n ≥ 2 )
1A grubu elementlerine alkali metaller de denir.
Li
Na
Bileşiklerinde (+1) değerlik alırlar.
s orbitalinde tek bir elektronu vardır.
Çok aktif olduklarından suyla reaksiyona girerek hidrojen gazı ve metal hidroksitleri
K
oluştururlar.
Rb
2M (k) + 2H2O (s) → 2MOH (suda) + H2 (g) (M: Alkali Metal)
Cs
Havayla etkileştiklerinde, oksijenle birleşerek oksitleri oluştururlar.
Fr
4Li (k) + O2 (g) → 2Li2O (k)
ELEMENTLERİ TANIYALIM
1A Grubu Elementleri ( ns1 , n ≥ 2 )
Li
Na
Diğer alkali metallerin hepsi oksitler ve peroksitler (O2-2 iyonu
içeren) oluştururlar
K
2Na (k) + O2 (s) → 2Na2O2 (k)
Rb
Potasyum, rubidyum ve sezyum, süperoksitler (O2- iyonu içeren)
de oluştururlar.
Cs
Fr
K (k) + O2 (g) → KO2 (k)
Alkali metallerin oksitleri bazik özellik gösterirler.
ELEMENTLERİ TANIYALIM
2A Grubu Elementleri ( ns2 , n ≥ 2 )
Be
Mg
Ca
Toprak alkali metaller olarak ta adlandırılırlar.
Alkali metallerden daha az reaktiftirler.
Bileşiklerinde (+2) değerlik alırlar.
Metalik karakterleri yukarıdan aşağıya doğru inildikçe artar.
Pek çok berilyum bileşiği (BeH2, BeCl2, gibi berilyum halidler) ve bazı magnezyum
Sr
Ba
Ra
bileşikleri (MgH2 gibi) iyoniklikten çok moleküller bileşiklerdir.
Be ve Mg yüksek sıcaklıkta oksijenle oksit (BeO, MgO) oluştururken, Ca, Sr ve Ba oda
sıcaklığında oksit oluşturabilirler.
2Mg (k) + O2 → 2MgO
ELEMENTLERİ TANIYALIM
2A Grubu Elementleri ( ns2 , n ≥ 2 )
Be
Oksitleri, BeO amfoter diğer oksitler ise bazik özellik gösterirler.
Be su ile reaksiyona girmezken, Mg su buharıyla çok yavaş bir tepkime vermektedir, Ca, Sr,
ve Ba ise soğuk su ile tepkime vererek H2 açığa çıkarırlar.
Mg
Ba (k) + 2H2O (s) → Ba(OH)2 (suda) + H2 (g)
Ca
Sr
Ba
Ra
Mg sulu çözeltilerde asitlerle reaksiyona girer ve hidrojen gazı açığa çıkar.
Mg (k) + 2H+ (suda) → Mg2+ (suda) + H2 (g)
Ca, Sr ve Ba da sulu asit çözeltilerinde tepkimeye girerek hidrojen gazı oluştururlar. Fakat, bu
metaller suyla da reaksiyona girdiklerinden iki farklı reaksiyon aynı anda olur.
ELEMENTLERİ TANIYALIM
3A Grubu Elementleri ( ns2np1, n ≥ 2 )
B
Al
Ga
Grubun ilk üyesi olan bor (B) yarı-metal özellik gösterir ve ikili iyonik bileşik oluşturmaz.
Suya ve oksijene karşı reaktif değildir.
Diğer üyeleri ise metaldir.
Al havayla temas ettiğinde alüminyum oksit oluşturur.
4Al (k) + 3O2 (g) → 2Al2O3 (k)
Üzeri koruyucu alüminyum oksitle kaplanmış alüminyum, alüminyum elementinden daha az
In
Tl
reaktiftir.
Alüminyum sadece (+3) yüklü iyon oluşturur. Amfoter özellik gösterir. Asitler ve bazlarla
tepkime vererek H2 gazı açığa çıkarırlar.
2Al (k) + 6HCl → AlCl3 + 3H2 (g)
………………..Asit
2Al (k) + 6NaOH → Na3AlO3 + 3H2 (g) ………………..Baz
ELEMENTLERİ TANIYALIM
3A Grubu Elementleri ( ns2np1, n ≥ 2 )
Diğer 3A grubu metalleri hem (+1) ve hem de (+3) yüklü iyonlar oluştururlar.
B
Al
Gruptan aşağıya doğru inildikçe (+1) yüklü iyonların (+3) yüklü iyonlardan daha
kararlıdırlar.
Gruptaki metaller pek çok moleküler bileşik de oluştururlar. Al’in hidrojenle
Ga
In
Tl
bileşiği AlH3 gibi.
Periyodik tabloda soldan sağa doğru gidildikçe metalik karakterden ametalik
karaktere doğru bir kayma olur.
ELEMENTLERİ TANIYALIM
4A Grubu Elementleri ( ns2np2, n ≥ 2 )
C
Si
Grubun ilk üyesi karbon ( C) ametaldir. Karbonun grafit ve elmas olmak üzere iki allotropu
vardır.
Silisyum ve germanyum yarı – metaldirler ve iyonik bileşik oluşturmazlar.
Bu grubun metal üyeleri Sn ve Pb amfoter özellik gösterirler, asit ve bazlarla tepkimeye
Ge
girerek hidrojen gazı açığa çıkarırlar.
Sn (k) + HCl (suda) → SnCl2 (suda) + H2 (g)
Sn
Pb
Sn (k) + NaOH (suda) → Na2SnO2 + H2 (g)
4A grubu elementleri, bileşiklerinde +2 ve +4 değerlik alabilirler. Karbon ve silisyum için +4
değerlik daha kararlıdır.
Örneğin:
CO2, CO den daha kararlıdır. SiO2 kararlı bir bileşiktir fakat SiO normal koşullarda mevcut değildir.
Kalay (Sn) bileşiklerinde +4 değerlik, +2 değerlikten biraz daha fazla kararlıdır.
Kurşun (Pb) bileşiklerinde +2 değerlik tartışmasız daha kararlıdır.
ELEMENTLERİ TANIYALIM
5A Grubu Elementleri ( ns2np3, n ≥ 2 )
5A grubu elementlerinden azot ve fosfor ametal, arsenik ve antimon yarı-metal bizmut ise
metaldir.
Azot elementi iki atomlu bir gazdır (N2). Çeşitli oksitler oluşturur. (NO, N2O, NO2, N2O4 ve
N
P
As
N2O5). Bunlar arasında sadece N2O5 katı diğerleri gazdır.
Fosfor molekülü P4 halindedir. En önemli iki oksidi P4O6 ve P4O10 dur.
Fosforun en önemli allotropları beyaz fosfor (P4) ve polimer yapısında olan kırmızı fosfordur
Sb
(P4)n . Kırmızı fosfor, beyaz fosfordan daha kararlıdır.
nP4 (beyaz fosfor) → (P4)n (kırmızı fosfor)
Bi
Arsenik antimon ve bizmutun geniş, üç boyutlu yapıları vardır. Bizmut, kendinden önceki
gruplardaki metallerden çok daha az reaktif bir metaldir.
ELEMENTLERİ TANIYALIM
6A Grubu Elementleri ( ns2np4, n ≥ 2 )
O
S
Grubun ilk üç elementi (oksijen kükürt ve selenyum) ametaldir. Son ikisi ise (tellür ve
polonyum) yarı-metaldir.
Oksijen diatomik (O2) bir moleküldür. Oksijenin iki allotropu (O2 ve O3) bulunmasına karşın
oksijen molekülünden söz edildiğinde O2 kastedilir. Ozon O3, O2 den daha kararsızdır.
Se
Te
Po
Ozon
Oksijen üç çeşit oksit oluşturur; Oksit O-2, peroksit O2-2 ve süperoksit O2-
ELEMENTLERİ TANIYALIM
6A Grubu Elementleri ( ns2np4, n ≥ 2 )
O
Elementel kükürdün ve selenyumun molekül formülleri sırasıyla S8 ve Se8 dir.
Kükürtün çeşitli allotropları vardır. Bunlar; Rombik kükürt (S8) ve monoklinik kükürt (S8)
rombik kükürt termodinamik açıdan daha kararlıdır.
S
Se
Te
Po
Kükürtün önemli bileşikleri SO2, SO3 ve H2S dir. Kükürt trioksit suyla reaksiyona girdiğinde
sülfirik asit meydana gelir
SO3 (g) + H2O (s) → H2SO4 (suda)
ELEMENTLERİ TANIYALIM
7A Grubu Elementleri ( ns2np5, n ≥ 2 )
F
Cl
Br
Halojenlerin hepsi genel formülleri X2 olan ametaldir. Burada X, bir halojeni temsil eder. Çok
reaktif olduklarından doğada diatomik halde bulunurlar. Flor çok reaktiftir ve suyla birleşerek
oksijen meydana getirir.
2F2 (g) + 2H2O (s) → 4HF (g) + O2 (g)
Bileşiklerinde (-1 ve +7 ye kadar) değerlik alabilirler. Flor ise sadece (-1) değerlik alır.
Oda koşullarında; flor ve klor gaz, brom sıvı ve astantin ise katı halde bulur.
I
At
Halojenler kendi aralarında (ICl ve BrF3) veya başka gruplardaki ametallerle (NF3, PCl5 ve SF6
gibi) birçok molekülere bileşikler oluştururlar.
Hidrojenle reaksiyona girerek hidrojen hallürleri meydana getirirler;
H2 (g) + X2 (g) → 2HX (g)
Hidrojen hallürler suda çözünerek hidrohalik asitleri oluştururlar. (HF, HCl ve HBr)
ELEMENTLERİ TANIYALIM
8A Grubu Elementleri ( ns2np6, n ≥ 2 )
He
Ne
Bütün asal gazlar tek atomludur.
İyonlaşma enerjileri bütün elementler içinde en yüksek olanlardır.
Bileşik oluşturmaya yatkın değiller. Son zamanlarda
ve Kr‘nun bazı bileşikleri
sentezlenmiştir. (XeF6, XeO3, KrF2)
Ar
Kr
Xe (g) + PtF6 (g) → XePtF6 (k)
Asal gaz içeren bileşiklerin hiçbir ticari uygulaması yoktur ve doğada olan biyolojik olaylarda
yer almazlar.
Xe
Rn
Helyumun, neonun ve argonun bilinen hiçbir bileşiği yoktur.
ELEMENTLERİ TANIYALIM
B Grubu Elementleri ( ns (n-1)d, n ≥ 4 )
Sc
Ti
v
Cr
Mn
Fe
Co
Ni
Cu
Zn
Y
Zr
Nb
Mo
Tc
Ru
Rh
Pd
Ag
Cd
La
Hf
Ta
W
Re
Os
Ir
Pt
Au
Hg
Ac
Rf
Db
Sg
Bh
Hs
Mt
Ds
Periyodik sistemde s ve p bloklarının arasında bulunurlar. Bu elementlere geçiş elementleri
denir. Tamamı metal olduğu için ayrıca geçiş metalleri olarak da bilinirler.
Atom numarası 21 olan skandiyum (Sc) elementi d blokunun ilk elementi olarak önemlidir.
Bu elementler bileşiklerinde (+1) ile (+7) arasında çok farklı değerlikler alabilmektedir.
Geçiş metalleri saf hâlde kendi aralarında metalik bağ oluştururken ametallerle yaptıkları
bileşiklerinde iyonik bağ oluştururlar.
ELEMENTLERİ TANIYALIM
Lantanitler ve Aktinitler( ns (n-1)d, n ≥ 5 )
Ce
Pr
Nd
Pm
Sm
Eu
Gd
Tb
Dy
Ho
Er
Tm
Yb
Lu
Th
Pa
U
Np
Pu
Am
Cm
Bk
Cf
Es
Fm
Md
No
Lr
Temel hâl elektron dizilimleri yazıldığında son orbitali f olan elementler f bloku elementleridir.
Tamamı metaldir ve iç geçiş metalleri de denir.
6. periyotta lantan (La) elementinden sonra gelen 14 element (atom numarası 58’den başlayıp 71’i
de kapsayan) lantanitler (nadir toprak metalleri) adını alır.
7. periyotta aktinyum (Ac) elementinden sonra gelen 14 element de (atom numarası 90’dan
başlayıp 103’ü de kapsayan) aktinitler adını alır.
ELEMENTLERİ TANIYALIM
Lantanitler ve Aktinitler( ns (n-2)f, n ≥ 5 )
Lantan (La) elementinde 6s orbitali dolduktan sonra yeni elektronun 4f orbitaline
yerleşmesi gerekir.
Ancak 5d ve 4f orbitallerinin enerjileri birbirine çok yakındır.
Lantanın 4f orbitalinin enerjisi 5d orbitalinden biraz daha yüksektir. Bu yüzden
lantanın elektron dağılımı [Xe] 6s2 4f1 yerine [Xe] 6s2 5d1 yapısındadır.
Godalinyum (Gd) elementinin elektron dağılımının [Xe] 6s2 4f8 yerine [Xe] 6s2 4f7 5d1
şeklindedir. Bunun sebebi yarı dolu orbitallere sahip küresel simetrik 4f7
orbitallerinin fazladan kararlılık sağlamasıdır.
Kaynakça:
CHANG, Raymond, Fen ve Mühendislik Bölümleri için Kimya, Beta Yayınları, İstanbul 2000
BADUR, Hilmi, Kimya 11Sınıf Ders Kitabı, Evrensel İletişim Yayınları, Ankara 2015