PERİYODİK TABLO
Maddenin temel birimi atomlar. Tek bir cins atomdan oluşmuş, kimyasal tekniklerle
ayrıştırılamayan ya da farklı maddelere dönüştürülemeyen saf maddelereyse "element"
adı veriliyor. Dünya üzerinde bilinen elementlerin belirli bir şekilde yerleştirildiği sistem,
periyodik tablo olarak adlandırılıyor.
Periyodik tablo bize neler anlatıyor?
Periyodik tablodaki elementler nasıl isimlendiriliyor?
Periyodik tabloyu kim hazırladı?
Hakkında bilgi edinmek istediğiniz grubun ya da elementin üzerine tıklayınız.
1A 2A * 3B 4B 5B 6B 7B 8B 8B 8B 1B 2B 3A 4A 5A 6A 7A 8A
*
*
*
*
**
Elementlerin, soldan sağa ve yukarıdan aşağıya doğru artan atom numaralarına göre
diziliminden oluşan bu tabloda, yatay sıralara "periyot", dikey sütunlaraysa "grup" adı
veriliyor.
Periyotlar ve gruplar neleri ifade ediyor?
Lantanid ve aktinidler neden ayrı 2 sıra halinde gösteriliyor?
Periyodik Tablo Gurup Elementlerin Kolay Öğrenilme Yolu
PERİYODİK ÇİZELGE
METALLER
1/A
GRUBU
2/A GRUBU
AMETALLER
3/A
GRUBU
4/A
GRUBU
5/A
GRUBU
6/A
GRUBU
SOYGA
ZLAR
7/A
GRUBU
8/A
GRUBU
HERGE
LE
BEN
BEN
CİVCİVİ
NE
O
FİNO
Be=BERİLY
UM
B=BOR
C=KARBO
N
N=AZOT
O=OKSİJ
EN
F=FLOU
R
LİSESİNİ
N
MAĞAZAD
A
ASLINDA
SİZE
PARA
SENİN
CİVCİVİ
N
Li=LİTYU
M
Mg=MAGN
EZYUM
Al=ALÜMİ
NYUM
Si=SİLİSYU
M
P=FOSF
OR
S=KÜKÜ
RT
NANKÖR
ÇANTA
GABAĞIN
GETİRİRK
EN
AŞIĞI
ŞEHİR
Na=SODY
UM
Ca=KALSİY
UM
Ga=GALY
UM
As=ARS
ENİK
Se=SELE
NYUM
KİMYACI
SI
SATARKEN
İYİSİNİ
SINIFA
SABRİ
TEPESİN
DEKİ
St=STRONS
İYUM
İn=İNDİY
UM
Sn=KALAY
Sb=ANT
İMON
BABAMA
TARTMA
M
PİSLEDİ
HAYDAR
PAŞA
H=HİDR
OJEN
K=POTAS
YUM
RABİANI
N
Rb=RUBİ
Ba=BARYU
M
Ta=TALY
Ge=GERM
ANYUM
Pb=KURŞU
N
Cl=KLO
R
BURNU
NU
Br=BRO
M
POLONY
ALI
Bi=BİZ
Po=POLO
NECİP
Ne=NEO
N
ARSIZ
Ar=ARG
ON
ISIRDI
KERİMİ
I=IYOT
Kr=KRİP
TON
ATTI
KESERL
E
Te=TELL
ÜR
BİZİMKİ
Sİ
He=HEL
YUM
Ast=AST
ATİN
Xe=KSE
DYUM
CESEDİNİ
Ce=SEZY
UM
UM
MUNT
NYUM
NON
RASTLADI
M
RENDEL
EDİ
Ra=RADYU
M
Rd=RAD
ON
FIRLATTI
Fr=FRAN
SİYUM
1/A-2/A-3/A grubu elementleri metaldir.Sadece Hidrojen atomu 1/A grubu elementidir,fakat
ametaldir.
4/A-5/A-6/A/7/A grubu elementleri ametaldir.
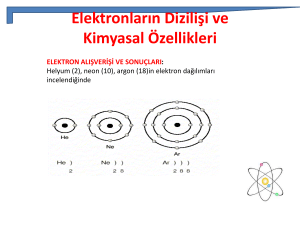
8/A grubu soygazdır (asalgazdır),elementlerinin son yörüngesinde 8e vardır.Sadece
Helyumun yörüngesinde 2 elektron vardır,fakat soygaz özelliktedir.
Periyodik Cetvel Ve Özellikleri
Elementler benzer özelliklerine göre sınıflandırılırlar.Elementlerin benzer özelliklerine göre sınıflandırılmasıyla
oluşturulan tabloya periyodik cetvel denir. Periyodik cetvelde, elementler artan atom numaralarına göre dizilmiş ve
benzer özellikteki elementler alt alta gelmiştir. Periyodik cetvele periyodik tablo ya da periyodik çizelge de denir.
Periyodik cetveli oluşturan yatay sıralara periyot adı verilir.
Yatay sıralarda atom numaraları arttıkça, elementlerin fiziksel ve kimyasal özellikleri değişir. Periyodik cetveldeki düşey
sütunlara grup denir.
Aynı gruptaki elementler benzer kimyasal özellikler gösterir.Periyodik cetvelde 8 tane A ve 8 tane B olmak üzere 16
tane grup vardır. Periyodik cetvel 18 sütundan oluşur. B gruplarından üç tanesi birden 8B olarak isimlendirilir.
Periyodik cetveldeki ilk sütuna 1A grubu denir.Son sütunu ise 8A grubu oluşturur.1 A grubu elementlerine alkali
metaller adı verilir.
Hidrojen 1 A grubunda olduğu hâlde alkali metaller grubuna girmez. 7 A grubu elementlerine halojenler, 8A grubu
elementlerine soy gazlar adı verilir.
Grup ve Periyodun Bulunması
Bir elementin atom numarası biliniyorsa, bu elementin grup ve
periyodu bulunabilir.
Örneğin 7N elementinin elektronlarının dağılımı şöyledir:
7N ) )
25
Burada en son enerji seviyesindeki elektron sayısı, grup numarasını;
enerji seviyelerinin sayısı ise periyot numarasını verir.
Bu sonuçlara göre, 7N elementi 2. periyotta 5 A grubundadır.
Örnek
17Cl elementinin periyot ve grup numarasını bulunuz.
Değerlik Elektron Sayısı
Nötr bir atomun son enerji düzeyindeki elektron sayısına, değerlik elektron sayısı denir.
Gruplara göre elementlerin değerlik elektron sayıları şöyledir:
Elementlerin Sınıflandırılması
Elementler, metaller, ametaller, yarı metaller ve soy gazlar olmak üzere sınıflara ayrılır.
Metallerin Genel Özellikleri
Periyodik çizelgenin sol tarafında bulunurlar.
Parlak ve serttirler.
Şekil verilebilirler, tel veya levha hâline gelebilirler.
Oda sıcaklığında katı hâlde bulunurlar. Civa (Hg) hariç.
Elektriği ve ısıyı iyi iletirler.
Bileşik oluştururken elektron verirler. Elektron verince (+) pozitif yüklü olurlar.
Kendi aralarında bileşik oluşturmazlar.
Ametallerin Genel Özellikleri
Periyodik çizelgenin sağ tarafında bulunurlar.
Mat görünüşlüdürler.
Vurulunca kırılabilirler, şekil verilemezler.
Grafit hariç elektrik ve ısıyı iyi iletmezler.
Oda sıcaklığında brom sıvı, karbon, kükürt ve bor katı, diğerleri gaz hâldedir.
Metallerle yaptıkları bileşiklerde (–) negatif yüklüdürler.
Kendi aralarında bileşik oluşturabilirler.
Yarı Metaller
Periyodik çizelgede metallerle ametalleri ayıran zig-zag çizginin sağ ve solunda bulunurlar.
Bazen metal, bazen ametal özellik gösterirler.
Bor, silisyum, germanyum, arsenik, antimon, tellür, polonyum ve astatin yarı metallerdir.
Soy Gazlar
Kararlı yapıya sahiptirler. Elektron alma ve verme eğilimleri yoktur.
Başka maddelerle reaksiyona girmezler.
Oda sıcaklığında gaz hâlde bulunurlar.
Periyodik çizelgenin en sağında bulunurlar.
Periyodik tablonun ortasında yer alan B Grubu elementlerine geçiş elementleri denir. Bunların içinde ağır metaller
bulunur.
Element kütlelerinin akb cinsinden gösterilmesi:
Periyodik tabloda elementlerin kütleleri yazılırken izotopları da göz önünde bulundurulur. Bir elementin kütlesi, izotop
kütleleri göz önüne alınarak hesaplanır.
Klor elementi tabiatta % 75 oranında 35Cl şeklinde, % 25 oranında da 37Cl izotopları şeklinde bulunur. Cl elementinin
ortalama kütlesi şöyle hesaplanır:
Klor elementinin atom kütlesi
Klor elementinin ortalama kütlesi 35,5 akb dir. Bu yüzden Klor elementi periyodik tabloda 35,5Cl şeklinde gösterilir.
75/100 x 35 + 25/100 x 37 = 35,5 akb
1. Ametalik özellik hangi elementte en fazladır?
A)X B)Y C) Z D) T
2. Metalik özellik hangi elementte en fazladır?
A)X B)Y C) Z D) T
3. Hangi element kararlı yapıdadır?
A)X B)Y C) Z D) T
4. Değerlik elektron sayısı ile ilgili olarak aşağıdakilerden
hangisi yanlıştır?
Element Değerlik e– sayısı
A) X 1B) Y 5 C) Z 2 D) T 0
5. Atom numarası en küçük olan element hangisidir?
A)X B)Y C) Z D) T