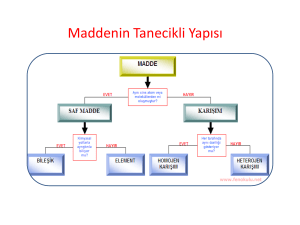
Maddenin Tanecikli Yapısı
advertisement
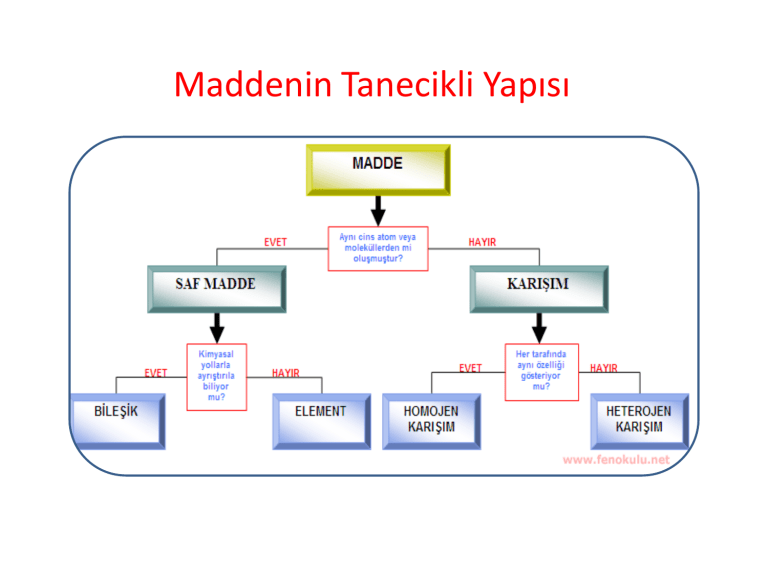
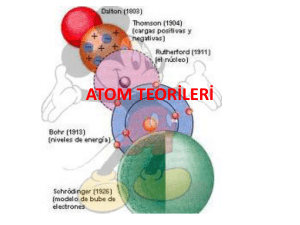
Maddenin Tanecikli Yapısı Maddenin Tanımı • Kütlesi olan ve boşlukta yer kaplayan her şeye madde denir. Cisim nedir? • Maddenin şekil almış halidir. Maddenin Halleri Maddeler doğada 3 halde bulunur: – Katı maddeler – Sıvı maddeler – Gaz maddeler Katı Maddeler • Belirli bir şekli olan, sıkıştırılamayan fakat genleşebilen maddelere katı madde denir. • Katı maddenin tanecikleri hareketsizdir. Sıvı Maddeler • Belirli bir şekli olmayan fakat bulunduğu kabın şeklini alan sıkıştırılamayan ama genleşebilen akışkan maddelere sıvı maddeler denir. Gaz Maddeler • Belirli bir şekli olmayan fakat bulunduğu kabın şeklini alan sıkıştırılabilen ve genleşebilen uçucu maddelere gaz maddeler denir. Gaz maddeler kapalı kaplarda bulundurulmalıdırlar. Maddenin Plazma Hali • Maddeler çok düşük veya çok yüksek sıcaklıklarda plazma halinde olabilir. Bu hal maddenin 4. hali olarak adlandırılabilir. Elektrik kıvılcımları, lavlar, alev, ateş ve yıldızlar plazmaya örnek verilebilir. Maddelerin Sıkışma Özelliği • Tanecikleri arasında boşluk olan maddeler kuvvet etkisi ile sıkıştırılabilir. Bu maddeler ise sadece gaz maddeleridir. Maddelerin Genleşme Özelliği • Katı, Sıvı ve Gaz taneciklerinin sıcaklık arttıkça hareketleri hızlanır. Bu durumda kapladıkları yer artar. • Genleşme ile termometre, uçan balon gibi aletler yapılmıştır. Maddelerin Özellikleri Madenin Hal Değişimi Maddenin En Küçük Birimi Maddenin en küçük yapı birimine atom denir. Atom küre şeklindedir ve elektrikli yapıya sahiptir. Atom, kelime anlamı olarak bölünemez, parçalanamaz anlamındadır. Atomlar ancak elektron mikroskobuyla görülebilirler. Atomun Tarihçesi Atom hakkında Democritus, Dalton, Thomson, Rutherford, Bohr ve De Broglie isimli bilim adamları ve filozoflar görüşlerini ortaya koymuşlar ve günümüzdeki atom modeli ortaya çıkmıştır. Democritus Atom Teorisi : • Atom hakkında ilk görüş M.Ö. 400’lü yıllarda Yunanlı filozof Democritus tarafından ortaya konmuştur. Democritus, maddenin taneciklerden oluştuğunu savunmuş ve bu taneciklere atom adını vermiştir. Democritus, atom hakkındaki görüşlerini deneylere göre değil varsayımlara göre söylemiştir. Democritus Atom Teorisi : • Democritus’ a göre; Madde parçalara ayrıldığında en sonunda bölünemeyen bir tanecik elde edilir ve bu tanecik atomdur. Bütün maddeler aynı tür atomlardan oluşur. Maddelerin farklı olmasının nedeni maddeyi oluşturan atomların sayı ve dizilişi biçiminin farklı olmasıdır. Atom görülemez. Atom görülemediği için bölünemez. John Dalton : • Atom hakkında ilk bilimsel görüş 1803 – 1808 yılları arasında İngiliz bilim adamı John Dalton tarafından ortaya atılmıştır. John Dalton Dalton’un Atom Modeli John Dalton : • Dalton’ a göre; Maddenin en küçük yapı taşı atomdur. (Maddeler çok küçük, bölünemez, yok edilemez taneciklerden oluşur.) Atomlar parçalanamaz. Atom içi dolu küre şeklindedir. Bütün maddeler farklı tür atomlardan oluşmuştur. Maddelerin birbirlerinden farklı olmasının nedeni maddeyi oluşturan atomların farklı özellikte olmasıdır. Bir maddeyi oluşturan atomların tamamı birbirleriyle aynı özelliklere sahiptir. John Joseph Thomson : • Atomun yapısı hakkında ilk model 1898 yılında Thomson tarafından ortaya konmuştur. Thomson atom modeli bir karpuza yada üzümlü keke benzer. • Thomson’ a göre; – Atom küre şeklindedir. (Çapı 10–8 cm) – Atomda (+) ve (–) yüklü tanecikler bulunur. – Thomson’a göre atom; dışı tamamen pozitif yüklü bir küre olup negatif yüklü olan elektronlar kek içerisindeki gömülü üzümler gibi bu küre içerisine gömülmüş haldedir. Ernest Rutherford: Atomun çekirdeğini ve çekirdekle ilgili birçok özelliğin ilk defa keşfeden bir bilim adamıdır. – Elektronlar çekirdek etrafında dairesel yörüngelerde sürekli dolanırlar. – Elektronların bulunduğu hacim çekirdeğin hacminden çok büyüktür. – Çekirdekteki yük sayısı, elektron sayısına eşittir. Niels David Bohr : Bohr atom teorisi hidrojenin yayınma spektrumuna dayanılarak açıklanır. Bohr’ a göre; – Elektronlar çekirdek etrafında belirli enerjiye karşılık gelen belirli uzaklıklarda bulunur. – Yüksek enerji düzeyinde bulunan elektron, düşük enerji düzeyine geçerse fotonlar halinde ışık yayarlar. – Kararlı hallerin tamamında elektronlar çekirdek etrafında dairesel yörünge izlerler. Modern Atom Modeli: Atomda belirli bir enerji düzeyi vardır. Elektron ancak bu düzeyden birinde bulunabilir . – Elektron bir enerji düzeyindeki hareketi sırasında çevreye ışık yaymazlar. – Atoma iki düzey arasındaki fark kadar enerji verilirse elektron daha yüksek enerji düzeyine geçer. – Atoma verilen enerji kesilirse elektron enerjili düzeyinde kalamaz daha düşük enerji düzeyinden birine geçer. Bu sırada iki düzey arasındaki fark kadar enerjiyi ışık şekline çevreye verir.