002. Asim kurjak
advertisement

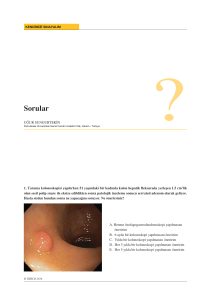
TEK GEN HASTALIKLARINDA PRE‹MPLANTASYON GENET‹K TANI Semra Kahraman, Hüseyin Karaday›, Güvenç Karl›kaya, Semra Sertyel, Necati F›nd›kl›, Yaman Sa¤lam ‹stanbul Memorial Hastanesi, Yard›mc› Üreme Teknikleri ve Üreme Geneti¤i Merkezi, ‹stanbul, Türkiye skahraman@superonline.com.tr Son y›llarda genetik bilimindeki geliflmeler sayesinde birçok genetik kökenli hastal›k implantasyon öncesi dönemde embriyo üzerinde tan›mlanabilmektedir. Embriyolar›n rahim içerisine transferinden önce gerçeklefltirilen genetik analiz sonras› anomali tafl›mad›¤› tespit edilen embriyolar›n anne aday›na transferine imkan tan›yarak sa¤l›kl› gebelik elde edilmesini amaçlayan bu yönteme gebelik öncesi genetik tan› (Preimplantasyon Genetik Tan›-PGT) ad› verilmektedir. PGT tahliye ile sonland›r›lan gebeliklerde yaflanabilecek psikolojik, fizyolojik ve ard›fl›k tahliye ifllemleri sonucunda oluflabilen infertilite problemlerinin önlenmesi yönünde prenatal tan›n›n erken bir formasyonu olarak kabul edilmektedir. Özellikle çiftlerin belirli bir genetik hastal›k yönünden tafl›y›c› bulunmas› durumunda PGT yöntemi ile hastal›k tafl›yan embriyolar›n elimine edilmesi ve sa¤l›kl› embriyolar›n transferi ile sa¤l›kl› çocuk sahibi olmak mümkündür. Günümüzde PGT uygulamalar› iki farkl› yaklafl›m olarak gerçeklefltirilmektedir: Bunlardan ilki özellikle ilerlemifl maternal yafl, tekrarlayan erken dönem gebelik kay›plar›, tekrarlayan implantasyon baflar›s›zl›klar›, fliddetli erkek infertilitesi ve translokasyon tafl›y›c›s› oldu¤u tespit edilmifl çiftlerde, artan anöploidi oranlar› nedeni ile uygulanan PGT-AT (Aneuploidy Detection-Anöploidi Tan›mlamas›) yöntemidir. Bu yöntemde oosit veya erken geliflim dönemi embriyolar›ndan kutup cisimcikleri veya blastomer(ler) al›nmak sureti ile, belirli kromozomlar floresan in situ hibridizasyon (FISH) yöntemi ile say›sal ve yap›sal olarak incelenerek, kromozomal yönden normal bulunan embriyolar transfer iflleminde kullan›lmaktad›r. PGT-TGH (Single Gene Disorders-Tek Gen Hastal›klar›) uygulamalar›nda ise, çiftlerden biri veya her ikisi genetik geçiflli hastal›k tafl›y›c›s› (otozomal dominant, otozomal resesif veya X’e ba¤l›) olarak tespit edildi¤i durumlarda, mutasyon veya kromozom anomalileri embriyolarda polimeraz zincir reaksiyonu (PCR) ve dizi analizi gibi moleküler yöntemler kullan›larak tespit edilmekte ve çiftlerin sa¤l›kl› çocuk sahibi olmalar› sa¤lanmaktad›r. Tek Gen Hastal›klar›nda PGT uygulamalar› ile günümüze kadar gerçeklefltirilen yaklafl›k 1500 siklusta 300’den fazla sa¤l›kl› gebelik elde edilmifltir. Gün geçtikçe artan say›da gen dizilerinin ve genetik geçiflli hastal›klar›n tan›mlanmas›, tek gen hastal›klar›nda PGT uygulamalar› endikasyonlar›n› artt›rmaktad›r. Tek Gen Hastal›klar›nda PGT endikasyonlar›ndan bir k›sm› Tablo 1’de verilmifltir. PGT sadece tek gen hastal›klar› için de¤il, ailesel kansere yatk›nl›k (ailesel adenomatoz polipozis koli, meme kanseri, retinoblastoma, Li- Fraumeni Sendromu vb.), HLA genotiplemesi ve di¤er farkl› (Konjenital sa¤›rl›k, Akondroplazi, Otizm) endikasyonlar içinde uygulanmaktad›r. 91 Kahraman S, Karaday› H, Karl›kaya G, Sertyel S, F›nd›kl› N, Sa¤lam Y Tablo 1. PGT-SGD uygulanabilen genetik geçiflli hastal›klardan baz›lar› β-Talasemi HLA Genotiplemesi Orak Hücre Anemisi Spinal Musküler Distrofi Fankoni Anemisi Hemofili A ve B Multiple Epiphyseal Displazia Akondroplazi Retinitis Pigmentoza Retinoblastoma Adrenolokodistrofi Hurler Sendromu OCT Alport Hastal›¤› Hipofosfatazya 3-hydroxyacyl-coa Dehidrogenaz Machado-Joseph Hastal›¤› Koroideremi Incontinentia Pigmenti Adrenolökodistrofi CDG1C Konjenital adrenal hiperplazi Stickler Sendromu Crouzon Sendromu X-linked, agammaglobulinemi (XLA) FG Sendromu tafl›y›c›l›¤› Oro-facial-digital syndrome type 1 Crouzon Sendromu Genodermatozis (PKP1) Sitrullinemi Kelley-Seegmil Sendromu Pelizaeus Merzbacher Hiperinsülinemik hipoglisemi PHH1 Bloom hastal›¤› FAP-Gardner CF+XL mental retardasyon (X2) Kistik Fibrozis Miyotonik Distrofi Duchenne Musküler Distrofi Epidermolizis Bullosa Fenilketonüri (PKU) X-linked Hidrosefali Gaucher Hastal›¤› Frajil X Huntington Hastal›¤› Hunter Sendromu Tay-Sach’s Hastal›¤› Alfa-1-antitripsin Eksikli¤i Lesch Nyhan Sendromu Marfan Hastal›¤› Glikojen Depo Hastal›¤› X-linked otizm RhD sensitizasyonu Osteogenezis imperfekta Deri frajilitesi Tüberoskleroz Nörofibromatoz ZFX/ZFY Spinal ve Bulbar musküler atrofi DAZ delesyonu Ataxia Telanjiektazi Familyal Amyloidotic Polinöropati Charcot-Marie-Tooth Tip IA Holoprozensefali (SSH gen) X-linked epilepsi (paternal side) Junctional epidermolizis bülloza Fabry’s Hastal›¤› Anemi tafl›y›c›lar› Santral kor hastal›¤› PGT ile kombine HLA doku tiplemesi uygulamalar›, PGT yöntemini sadece tan› amaçl› veya etkilenmifl gebelik eldesini önleyici bir yöntem olmaktan ç›karm›fl, ayr›ca tedavi amac›yla da kullan›labilen bir yöntem haline getirmifltir. Temel amaç, bir yandan etkilenmemifl embriyo seçimi ile sa¤l›kl› bir bebe¤in dünyaya getirilmesi, di¤er yandan da HLA uyumu nedeni ile allogenik hematopoetik kök hücre transplantasyonu uygulamas› ile hasta kardefl için tümüyle tedavi imkan› sa¤lanmas›d›r. Sonuçlar özellikle b-Talasemi olgular›nda bu yöntemle elde edilen kök hücrelerin nakli sonras› e¤er hasta çocukta hepatomegali ve portal fibrozis geliflmemifl ise %90 oran›nda baflar› sa¤lanabilece¤ini göstermektedir. Gerek anöploidi tan›mlamas›, gerekse tek gen hastal›klar›nda tan›mlama için gerekli olan kutup cisimcikleri ve blastomerler biyopsi ifllemi ile elde edilmektedir. PGT uygulamalar›n›n baflar›s› ve sa¤l›kl› gebelik eldesi tan›n›n do¤rulu¤u kadar biyopsi ifllemi sonras› embriyolar›n etkilenmeden iyi geliflimine de ba¤l›d›r. Bu nedenle biyopsi ifllemlerinin embriyonik geliflimin en az düzeyde etkilenebilece¤i, ayni zamanda da tan› için 92 Tek Gen Hastal›klar›nda Preimplantasyon Genetik gerekli sürenin sa¤lanaca¤› dönemde uygulanmas› gerekir. Kutup cisimcikleri biyopsisi oosit toplama iflleminden hemen sonra (1. kutup cisimci¤i biyopsisi) fertilizasyon de¤erlendirmesinden sonra (2. kutup cisimci¤i biyopsisi), embriyo biyopsi ifllemi ise embriyo gelifliminin 3. günü 7-8 blastomer aflamas›nda uygulanmaktad›r. Daha az say›da blastomer içeren embriyolarda uygulanan biyopsi iflleminin embriyo geliflimini büyük oranda aksatt›¤› veya durdurdu¤u yap›lan çal›flmalarda gösterilmifltir. Figür 1.de kutup cisimcikleri biyopsisi ve embriyo biyopsi ifllemi görülmektedir. A B Figür 1. a) A. 1.nci kutup cisimci¤i biyopsisi; B. Fertilize oosit; C,D. 1.nci ve 2.nci kutup cisimcikleri biyopsisi b) A. Embriyo biyopsi ifllemi için uygun klivaj dönemi embriyo; B,C,D. Embriyo biyopsi ifllemi. Biyopsi ifllemi sonras› elde edilen kutup cisimcikleri veya blastomer(ler) steril koflullarda tüpler içerisine al›narak litik solüsyonlar yard›m› ile çekirdek içerisindeki blastomere ait DNA yap›s›n›n iflleme uygun hale getirilmesi sa¤lan›r. Tek Gen Hastal›klar›nda PGT uygulamas› gerçeklefltirmek için multipleks, nested ve fluoresan PCR teknikleri DNA analizi için kullan›lan ara yöntemlerdendir. Ad› geçen PCR teknikleri ile ço¤alt›lan ilgili gen bölgesi, restriksiyon enzim analizi, dizi analizi veya minisequencing yöntemleri kullan›larak hastal›k tafl›y›p tafl›mamas› yönünden de¤erlendirilir. Figür 2’de dizi analizi ve minisequencing yöntemleri kullan›larak tespit edilen b-globin genine ait IVS-I-110G>A mutasyonu görülmektedir. Hastal›k tafl›mad›¤› tespit edilen embriyolar bulunduklar› geliflim günü ve hasta özellikleri dikkate al›narak embriyo transferi iflleminde kullan›lmaktad›r. Tek gen hastal›klar›nda PGT uygulamalar› son derece iyi organize edilmesi ve önceden detayl› planlanmas› gereken ifllemlerdir. Bu nedenle klinik, in vitro fertilizasyon ve genetik laboratuar› birimlerinin uygulamalar için özel tasarlanm›fl teknik altyap› ve bilgi birikimine sahip olmas› ve konusunda deneyimli personel taraf›ndan idare edilmesi gerekmektedir. Uygulamalar s›ras›nda uyulmas› gereken temel kurallar ve 93 Kahraman S, Karaday› H, Karl›kaya G, Sertyel S, F›nd›kl› N, Sa¤lam Y parametreler PGDIS (Uluslararas› Preimplantasyon Genetik Tan› Derne¤i) ve ESHRE Preimplantasyon Genetik Tan› Konsorsiyumu taraf›ndan detayl› olarak belirtilmektedir. Teknik altyap› eksikli¤i veya ifllem s›ras›nda oluflan suboptimal koflullar uygulaman›n ve gerçeklefltirildi¤i YÜT siklusunun baflar› flans›n› etkilemektedir. Tek gen hastal›klar›nda gerçeklefltirilen PGT uygulamalar› s›ras›nda en s›k gözlenen problemler kontaminasyon, ADO (Alelik Drop-Out-alellerden sadece birinin amplifikasyonu) problemleridir. Laboratuar içerisinde ve çal›flma alanlar›nda özel k›yafetler ve önlemler sayesinde kontaminasyon ihtimalini en aza indirmek mümkündür. Günümüzde gerek ADO gerekse kontaminasyonu önlemek için teknik içerisinde gerçeklefltirilecek de¤ifliklikler ve ilave metodlar da uygulanmakta ve bu problemlerden do¤abilecek negatif etkiler en aza indirilmektedir. Tek gen hastal›klar›nda PGT uygulamalar› ile kombine gerçeklefltirilen HLA doku tiplemesi ifllemleri ise daha detayl› ifllemler ve ileri düzeyde deneyim ve teknolojik imkanlar gerektirmektedir. ‹fllem öncesi çiftler ve hasta çocuk üzerinde mutasyon tafl›d›¤› belirlenen aleller ve HLA gen bölgesinde yer alan polimorfik STR iflaretçileri kullan›larak öncül genetik testler yap›l›r. Testlerin sonucunda hem incelenen genetik hastal›k hem de doku uygunlu¤u yönünden en güvenli flartlar ve uygun haplotipler belirlenerek çift YÜT siklusuna al›n›r. Siklus s›ras›nda elde edilen embriyolar, tek gen hastal›klar›nda gerçeklefltirilen PGT uygulamalar›nda oldu¤u gibi incelenerek sa¤l›kl› ve hastal›k tafl›yan kardefl ile ayni doku uyumuna sahip embriyolar embriyo transferi ifllemi için belirlenir. Figür 3’te merkezimizde tedaviye al›nan iki farkl› olguda (Wiscott Aldrich Sendromu ve b-talasemi) HLA doku tiplemesi için kullan›lan STR iflaretçileri, ifllem için uygun olan ve olmayan haplotip örnekleri ile uygun haplotipler kullan›larak gerçeklefltirilen embriyo ve hasta çocuk HLA doku uyumu analizi sonucu görülmektedir. DNA Sequencing C T A T T N Heterozigot IVSI - 110 G →A Minisequencing G T C Heterozigot IVSI - 110 G →A N Figür 2. Konvansiyonel DNA dizi analizi ve minisequencing teknikleri ile (IVS-I-110 G>A) β-talasemi mutasyonunun taranmas› Bugüne kadar dünya genelinde uygulanan 150’den fazla PGT ile kombine doku tiplemesi uygulamas› ve ifllem sonras› elde edilen sa¤l›kl› gebelikler yöntemin güvenli bir tedavi metodu olarak kullan›labilece¤ini göstermektedir (Tablo 2). Bununla birlikte hasta veya siklus ile iliflkili parametrelere ba¤l› olarak baflar› flans› de¤iflebilmektedir. Teorik olarak incelenen embriyonun otozomal resesif bir hastal›k yönünden sa¤l›kl› ve HLA genotipi yönünden uyumlu olma olas›l›¤› %18’dir. Bu oran ile ba¤lant›l› olarak merkezimizde gerçeklefltirilen uygulamalar klinik ve siklus seyri yönünden incelendi¤inde, elde edilen baflar›l› sonuçlar›n büyük ölçüde over rezervi ve maternal yafl ile ba¤lant›l› oldu¤u, artan yafl ve düflük over rezervi olgular›nda baflar› flans›nda azalma gözlenebilmektedir. ‹stanbul Memorial Hastanesi Yard›mc› Üreme Teknikleri (YÜT) ve Üreme Geneti¤i Merkezinde gerçeklefltirilen Tek Gen Hastal›klar›nda PGT uygulamalar›na ait sonuçlar Tablo 3’te görülmektedir. 94 Tek Gen Hastal›klar›nda Preimplantasyon Genetik A HLA STR Makerlar› Telomer HLA STR markerlar› Telomer D6S276 MOG-CA D6S510 D6S265 HLA-BC MIB TNF-α D6S273 D3A DRA-CA DQCAR II D6S439 D6S291 194 218 156 120 139 163 99 140 205 122 118 126 156 220 222 160 118 130 186 107 142 202 133 132 122 160 HBB geni ve markerlar› Telomer D11S4146 D11S988 D11S4181 HBB D11S1760 D11S1338 Anne 162 120 109 IVSI-110 111 130 208 220 158 122 132 167 109 138 214 137 126 116 158 HBB geni ve markerlar› Telomer Baba 156 126 105 N 107 134 160 132 116 IVSII-745 103 136 168 124 111 N 105 132 D11S4146 D11S988 D11S4181 HBB D11S1760 D11S1338 Sentromer Sentromer D6S276 MOG-CA D6S510 DS265 HLA-BC MIB TNF-α D6S273 D3A DRA-CA DQCAR II D6S439 D6S291 198 230 140 114 128 184 103 144 200 130 122 122 166 Sentromer Sentromer HLA geni ve markerlar› D11S4146 162 D11S988 120 D11S4181 109 HBB -110 D11S1760 111 D11S1338 130 Embriyo 1 160 132 116 -745 103 136 162 120 109 -110 111 130 Embriyo 2 168 124 111 N 105 132 156 126 105 N 107 134 Embriyo 3 160 156 132 126 116 105 IVSII-745 N 103 107 136 134 Embriyo 6 168 124 111 N 105 132 156 126 105 N 107 134 Embriyo 7 168 124 111 N 105 132 156 126 105 N 107 134 HBB geni ve markerlar› Embriyo 8 160 132 116 IVSII-745 103 136 162 120 109 -110 111 130 160 132 116 -745 103 136 D11S4146 D11S988 D11S4181 HBB D11S1760 D11S1338 HLA STR markerlar› HLA STR markerlar› D6S276 MOG-CA D6S510 D6S265 HLA-BC MIB TNF-α D6S273 D3A DRA-CA DQCAR II D6S439 D6S291 194 218 156 120 139 163 99 140 205 122 118 126 156 208 220 158 122 132 167 109 138 214 137 126 116 158 220 222 160 118 130 186 107 142 202 133 132 122 160 Hasta çocuk B 198 230 140 114 128 184 103 144 200 130 122 122 166 220 222 160 118 130 186 107 142 202 133 132 122 160 Tafl›y›c› Uyumsuz 208 220 158 122 132 167 109 138 214 137 126 116 158 194 218 156 120 139 163 99 140 205 122 118 126 156 Tafl›y›c› Uyumsuz 208 220 158 122 132 167 109 138 214 137 126 116 158 194 218 156 120 139 163 99 140 205 122 118 126 156 208 220 158 122 132 167 109 138 214 137 126 116 158 194 218 156 120 139 163 99 140 205 122 118 126 156 208 220 158 122 132 167 109 138 214 137 126 116 158 194 218 156 120 139 163 99 140 205 122 118 126 156 Normal Normal Tafl›y›c› Uyumlu (ET) Uyumlu (ET) Uyumlu (ET) 198 230 140 114 128 184 103 144 200 130 122 122 166 D6S276 MOG-CA D6S510 D6S265 HLA-BC MIB TNF-α D6S273 D3A DRA-CA DQCAR II D6S439 D6S291 Hasta Uyumsuz HLA STR markerlar› HLA STR markerlar› Telomer D6S276 MOG-CA D6S510 D6S265 HLA-BC TNF-α D6S273 DRA-CA TAP-1 D6S439 D6S291 D6S426 Telomer 216 220 151 120 107 117 140 119 204 125 125 158 212 214 149 116 116 109 142 129 202 117 113 162 WAS geni ve markerlar› Anne 220 226 140 114 120 121 146 127 198 121 130 160 WAS geni ve markerlar› Baba Telomer Telomer 117 107 N 164 208 DXS6941 DXS722 WAS DXS1240 DXS1470 120 113 N 160 214 114 109 Y107H 156 202 DXS6941 DXS722 WAS DXS1240 DXS1470 Sentromer Sentromer 218 218 155 110 130 105 144 135 200 119 120 156 Sentromer Sentromer WAS geni ve markerlar› DXS6941 DXS722 WAS DXS1240 DXS1470 Embriyo 5 114 109 Y107H 156 202 Embriyo 11 117 107 N 164 208 120 113 N 160 214 114 109 Y107H 156 202 Embriyo 14 117 107 N 164 208 114 109 Y107H 156 202 Embriyo Embriyo 18 18 WAS geni ve markerlar› DXS6941 DXS722 WAS DXS1240 DXS1470 114 109 Y107H 156 202 HLA STR markerlar› HLA STR markerlar› D6S276 MOG-CA D6S510 D6S265 HLA-BC TNF-α D6S273 DRA-CA TAP-1 D6S439 D6S291 D6S426 D6S276 MOG-CA D6S510 D6S265 HLA-BC TNF-α D6S273 DRA-CA TAP-1 D6S439 D6S291 D6S426 216 220 151 120 107 117 140 119 204 125 125 158 220 226 140 114 120 121 146 17 198 121 130 160 Hasta çocuk 212 214 149 116 116 109 142 129 202 117 113 162 220 226 140 114 120 121 146 17 198 121 130 160 212 214 149 116 116 109 142 129 202 117 113 162 218 218 155 110 130 105 144 135 200 119 120 156 216 220 151 120 107 117 140 119 204 125 125 158 220 226 140 114 120 121 146 17 198 121 130 160 216 220 151 120 107 117 140 119 204 125 125 158 220 226 140 114 120 121 146 17 198 121 130 160 Normal erkek Tafl›y›c› k›z Tafl›y›c› k›z Hasta erkek HLA Uyumsuz HLA Uyumsuz HLA Uyumlu (ET) HLA Uyumlu D6S276 MOG-CA D6S510 D6S265 HLA-BC TNF-α D6S273 DRA-CA TAP-1 D6S439 D6S291 D6S426 Figür 3. a) Wiscott Aldrich Sendromu tafl›y›c›s› olguda HLA doku tiplemesi için kullan›lan STR iflaretçileri. b) β-talasemi tafl›y›c›s› olguda HLA doku tiplemesi için kullan›lan STR iflaretçileri 95 Kahraman S, Karaday› H, Karl›kaya G, Sertyel S, F›nd›kl› N, Sa¤lam Y Günümüzdeki imkanlar do¤rultusunda DNA baz analizi yap›labilen tüm genetik hastal›klar› embriyoda tan›mlamak mümkündür. Ayr›ca teknik aç›dan bak›ld›¤›nda, bugün PGT ifllemlerinde kullan›lan dizi analizi cihazlar› ile gerçeklefltirilen ve s›n›rl› say›da DNA bölgesinin incelenmesine izin veren protokollerin yerlerini yak›n gelecekte DNA mikroçip teknolojisine b›rakmas› ile, yüzlerce hastal›k veya anomalinin biyopsi ifllemi sonras› elde edilen tek bir blastomerde eflzamanl› olarak tan›mlanabilmesi mümkün görünmektedir. Ülkemizde her y›l talasemi, anemi gibi kal›tsal hastal›k tafl›yan yüzlerce çocuk dünyaya gelmektedir. Bu olgularda günümüz koflullar›nda sa¤lanabilen nihai çözüm kordon kan› veya kemik ili¤i nakli ifllemleridir. Her ne kadar tedavide baflar› flans› yüksek olsa da, nakil için gereken hasta çocuk ile doku uyumu gösteren materyal son derece k›s›tl›d›r. Tek gen hastal›klar›nda PGT ifllemleri ile kombine gerçeklefltirilen HLA doku tiplemesi uygulamalar› sayesinde, çiftler hem sa¤l›kl› bir çocuk sahibi olabilmekte hemde yeni do¤an çocuk hasta kardefli için tedavi umudu olabilmektedir. Bu uygulamalar ile yak›n zamana kadar tan› amaçl› kullan›lan PGT teknikleri önemli ve potansiyel bir tedavi arac› haline de gelmifltir. Tablo 2. Mart 2004 tarihi itibariyle Dünya genelinde günümüze kadar gerçeklefltirilen PGT-TGH ve kombine HLA uygulamalar› Endikasyon Fankoni Anemisi Talasemi X’e ba¤l› hiper IgM Wiscott-Aldrich Sendromu X’e ba¤l› hipohidrotik ektodermal displazi X’e ba¤l› adrenolökotrofi Diamond-Blackfan anemisi Aplastik anemi Lösemi TOPLAM Siklus 39 61 5 2 1 1 4 2 32 147 Gebelik 5 7 2 1 1 0 2 0 7 25 Tablo 3. ‹stanbul Memorial Hastanesi YÜT ve Üreme Geneti¤i Merkezinde May›s 2003- Ocak 2005 tarihleri aras›nda gerçeklefltirilen PGT-TGH ve kombine HLA doku tiplemesi uygulamalar›. a. Endikasyonlara göre da¤›l›m Endikasyon ß talasemi Orak Hücre Anemisi San Filippo Hastal›¤› Mukopolisakaridoz G6PD FMF NF1 Spinal Musküler Atrofi Kistik Fibroz ß talasemi+HLA Wiskott-Aldrich + HLA Blackfan-Diamond + HLA ALL (HLA Tiplemesi) TOPLAM 96 b) Genel siklus verileri Siklus 7 5 2 1 1 2 1 4 2 43 1 2 3 74 Siklus say›s› 74 Kad›n yafl› MII oosit say›s› Fertilizasyon oran› (%) ET yap›lan siklus say›s› ET iptal edilen siklus say›s› Transfer edilen embriyo say›s› Gebelik oran› (%) 31.4 12.4 86 49 25 116 32.7 (16/49) Tek Gen Hastal›klar›nda Preimplantasyon Genetik Referanslar 1. Fiorentino F, Biricik A, Karadayi H, Berkil H, Karlikaya G, Sertyel S, Podini D, Baldi M, Magli MC, Gianaroli L, Kahraman S.. 2004 Development and clinical application of a strategy for preimplantation genetic diagnosis of single gene disorders combined with HLA matching. Molecular Human Reproduction 9, 399-410. 2. Kahraman S, Karlikaya G, Sertyel S, Karadayi H, Findikli N. 2004 Clinical aspects of preimplantation genetic diagnosis for single gene disorders combined with HLA typing. Reproductive Biomedicine Online 9,529-532 3. Kuliev A and Verlinsky Y. 2004a Thirteen years’ experience of preimplantation diagnosis: report of the Fifth International Symposium on Preimplantation Genetics. Reproductive BioMedicine Online 8, 229-235. 4. Kuliev A and Verlinsky Y. 2004b. Preimplantation HLA typing and stem cell transplantation: report of International Meeting, Cyprus 27-28 March 2004. Reproductive BioMedicine Online 9, 205-209 5. Rechitsky S, Kuliev A, Tur-Kaspa I, Morris R, Verlinsky Y. 2004 Preimplantation genetic diagnosis with HLA Matching. Reproductive BioMedicine Online 9, 210-221. 6. Van de Velde H, Georgiou I, De Rycke M, Schots R, Sermon K, Lissens W, Devroey P, Van Steirteghem A, Liebaers I.. 2004 Novel universal approach for preimplantation genetic diagnosis of b-thalassaemia in combination with HLA matching of embryos. Human Reproduction 19, 700-708. 7. Verlinsky Y, Cohen J, Munne S, Gianaroli L, Simpson JL, Farraretti AP, Kuliev A 2004 Over a decade of experience with preimplantation genetic diagnosis. Fertility and Sterility 82,302-303 8. Verlinsky Y, Rechitsky S, Schoolcraft W, Strom C, Kuliev A. 2001 Preimplantation diagnosis for Fanconi anemia combined with HLA matching. JAMA 285, 3130-3133. 97