https://hasanfirat.com 1 ASİTLER VE BAZLAR KONU ANLATIMI-3
advertisement

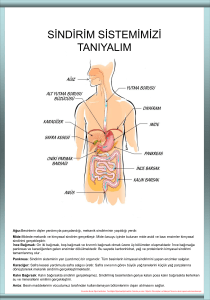
ASİTLER VE BAZLAR KONU ANLATIMI-3 1 SİNDİRİM SİSTEMİ ve ASİTLER-BAZLAR Besinler genel olarak karbonhidratlar, proteinler ve yağlar olmak üzere 3 ana sınıfa ayrılır. Besin maddelerinin kana geçebilecek kadar küçük moleküllere ayrılması olayına "sindirim" denir. Sindirim olayı temel olarak mekanik ya da kimyasal sindirim olmak üzere iki şekilde gerçekleşir. Ağızdaki sindirim genellikle mekanik olarak, çiğneyerek gerçekleşir. Karbonhidratlar ağızdaki tükürük bezlerinden salgılanan amilaz enzimi ile de parçalanır. Amilaz enzimi ağzın nötr olmasından dolayı çalışmakta ve karbonhidrat sindirimi ağızda başlayabilmektedir. Ağızda parçalanamayan karbonhidrat midede sindirilemez. Çünkü midenin pH değeri 1,5 civarında olduğundan midedeki amilaz etkisiz durumda olur. Karbonhidrat bu nedenle mideden oniki parmak bağırsağına geçerek hidrolize uğrar ve glikoza dönüşür. (Karbonhidrat + su → Glikoz) Diş sağlığı açısından da ağzımızın asidik olmaması gereklidir. Asidik gıdalar dişlerin yapısını bozarak, çürümelerine neden olmaktadır. Bu nedenle diş macunları, ağız çalkalama çözeltileri bazik özelliktedir. Proteinlerin sindirimi midede başlar. Midede salgılanan pepsin enzimi proteinleri parçalayarak polipeptitlere ayırır. Midede salgılanan asit "mide asidi" olarak bilinen HCl asididir. Midenin asidik ortamdan zarar görmesini midenin iç yüzeyinde bulunan "mukus" engeller. Midede protein sindirimi tamamlanmaz, oluşan polipeptitler oniki parmak bağırsağına geçerek pankreas tarafından salgılanan tripsin enzimi ile bazik ortamda dipeptit ve amino asitlere dönüşürler. Oluşan dipeptitler de ince bağırsak tarafından salgılanan erepsin enzimi ile amino asitlere ayrışır. Yağların sindirimi oniki parmak bağırsağında başlar ve sonlanır. Yağlar safra suyuyla mekanik olarak sindirilir ve yağ damlacıklarına dönüşür. Yağ damlacıkları lipaz enzimi ile bazik ortamda sindirilerek gliserin ve yağ asidine dönüşür. Kola, gazoz gibi gazlı içecekler şekerli sudan yüksek basınç altında CO2 gazı geçirilerek elde edilirler. CO2 gazının suda çözünmesi ile asidik bir çözelti elde edilir: CO2(g) + H2O(s) H+(suda) + HCO- 3(suda) Bu nedenle gazlı içeceklerin içilmesi ile vücudumuzdaki asitbaz dengesi bozulur, diş çürüklerine ve kemik erimesine neden olur. Gazlı içeceklerin tüketimi sonucunda sıkça tuvalete çıkılır ve vücudun su kaybı fazla olur. Asitli İçecekler; ●● Diş çürümelerine●● Kemik erimelerine●● Böbrek taşı oluşmasına ●● Sindirim sistemi sorunlarına neden olur. Maden suyu, vücudumuz için gerekli olan bir çok minerali içerir. Ancak maden suyu ve soda içecekleri asitlik derecesi yüksek içeceklerdir. Bu yüzden, gastrit, ülser gibi sindirim sorunu olan kişilerin ve içerdiği zengin Na+ (Sodyum iyonu) iyonu nedeni ile hipertansiyon hastalarının maden suyu ve sodayı fazla tüketmemeleri gerekmektedir. Yanlış beslenme alışkanlıkları ve psikolojik etkenler mide asidinin aşırı salgılanmasını sağlar. Böylece gastrit, ülser gibi mide hastalıkları da ortaya çıkabilir. Bu durumdaki hastalar midelerinin pH değerlerini artırıcı ilaçlar kullanırlar. Kullanılan mide ilaçları bazik özelliktedir. Magnezyum, sodyum ve kalsiyum elementlerinin hidroksit, karbonat ve bikarbonatlı bileşikleri baziktir. Mg(OH)2, NaOH, Ca(OH)2, NaHCO3 …). Magnezyum hidroksit bir antasittir ve mide asidini nötralize eder. Temizlik Malzemesi Kullanmanın Sağlık, Çevre ve Tesisat Açısından Önemi Asit ve bazlarla çalışırken sağlık ve güvenlik açısından oldukça dikkatli davranmak gerekir. Günlük yaşantımızda başta temizlik amaçlı kullandığımızda bir çok ürün aslında asit veya baz kaynaklı çözücülerdir; Kullandığımız mutfak eşyaları ve mutfaktaki yüzeyler zamanla yağlanır. Yağlanmayı gidermek için baz kaynaklı NaOH içeren malzemeler kullanılır. Ev ve iş yerlerinde keratin yapılı kıllar ve yağımsı kıvama sahip olan kirleticiler lavaboların tıkanmasına neden olur. Tıkanıklığın giderilmesi için tıkanıklığa neden olan maddeleri çözen NaOH, KOH bazları sıcak su ile birlikte kullanılır. Şebekelerde kullanılan sular sertlik yapan Ca2+ ve Mg2+ iyonlarını içerirler. Zamanla bu iyonlar CaCO3 ve MgCO3 şeklinde kireçlenerek su borularının tıkanması, ütü, çamaşır ve bulaşık makinelerinin rezistanslarının verimli çalışmalarını engeller. Bu sorunu gidermek için HCI kaynaklı kireç çözücüleri kullanırız. Yine kireçlenmenin neden olduğu tuvalet taşlarındaki kirlilik de H2SO4 ve HCI gibi asit kaynaklı ürünlerle giderilir. Evsel temizlik maddeleri anlatıldığı üzere kuvvetli bazik veya asidik özellik taşır. Bu nedenle temas ettikleri dokuda ciddi hasarlara neden olurlar. Sindirim sistemini tahriş edebilir, gözde ve ciltte yanıklara yol açabilirler. Bu nedenle kullanılmaları sırasında temastan kaçınılmalı, çocukların ulaşamayacağı yerlerde muhafaza edilmeleri sağlanmalıdır. Aynı şekilde aşırı miktarlarda kullanılan deterjan gibi temizlik malzemeleri, lavabo açıcıları ve tıkanan tuvalet borularını açmak için kullanılan maddelerin aşındırma etkisi nedeniyle gider borularının yapısını bozup, onların aşınmasına ya da delinmesine neden olabilir. Kullanılan temizlik malzemeleri doğaya karıştıklarında tatlı su kaynaklarını, yer altı sularını ve tarım topraklarını kirletebilir. Çünkü bunların doğada mikroorganizmalar tarafından parçalanma süresi onlarca yıl alabilir. Çamaşır suyu bazik özellik gösteren NaCIO çözeltisidir. Hem bir maddeyi beyazlatmak ve ağartmak amacıyla hem de hijyen de kullanılan bir kimyasal maddedir. Çamaşır suyunun amonyak içeren temizleyicilerle karıştırılması oldukça zehirli olan CI2 gazının açığa çıkmasına neden olabilir. Ayrıca çamaşır suyunun, tuz ruhu veya kireç, pas sökücülerle karıştırılması ölümcül zehirlenmelerle sonuçlanabilir. Evlerde bulunan kimyasalları tanır ve dikkatli kullanırsak; kireçlenen çaydanlıkları, tıkanan lavaboları kolaylıkla açabiliriz. Çaydanlık dibinde biriken CaCO3 ve MgCO3 tuzları baziktir. Bu tortuları çözmek için sirke ya da limon tuzu kullanılabilir. Çamaşır ya da bulaşık makinelerindeki kireçlenmeyi önlemek için deterjan gözüne her yıkamada bir çay bardağı sirke koyulması yeterlidir. Ayrıca metal eşyaların pasını açabilmek için tuz ruhu kullanılabilir. https://hasanfirat.com ASİTLER VE BAZLAR KONU ANLATIMI-3 2 Ev temizliğinde çamaşır sodası, karbonat, uçucu bitkisel yağlar, sirke ve boraks gibi doğal temizlik maddelerinin kullanımı yaygınlaştırılabilir. Boraksın kokuları alma, küf ve bakterilerin üremesini durdurma, leke çıkarma; çamaşır sodasının yağ ve leke çıkarma, sert suyu yumuşatma özellikleri vardır. Kötü kokuları alan karbonat bazı metalleri parlatmakta, leke çıkarmakta ve suyu yumuşatmakta kullanılabilir. Birikmiş mineral ve yağları çözerek camları parlatan sirke, mikrop öldürücü özelliğede sahiptir. TUZLAR Asit ve bazların tepkimesinden oluşan iyonik yapılı bileşiklere tuz denir. Asit + Baz Tuz + Su HCl + NaOH ! NaCl + H2O Asit ve bazın tepkimeye girerek tuz ve su oluşturmasına nötrleşme tepkimesi adı verilir. Tuzların Genel Özellikleri Kristal yapılı ve saf maddelerdir. İyonik yapılı katı maddelerdir. Erime ve kaynama noktaları yüksektir. Katı halde elektrik akımını iletmezler. Oda koşullarında katı haldedirler. Turnusol kağıdına etki etmeyebilirler. Suda iyonlarına ayrılarak çözünürler. Sıvı halde ve sulu çözeltilerinde iyon içerdikleri için elektrik akımını iletirler. Kuvvetli asit ve kuvvetli bazların nötrleşme tepkimesiyle oluşan tuzların sulu çözeltisi nötrdür. Yani pH değeri 7'dir. Nötr tuzların sulu çözeltilerinde H+ iyonu sayısı, OH– iyonu sayısına eşittir. Kuvvetli asit + Kuvvetli bazNötr tuz + Su HNO3 + KOH KNO3 + H2O Kuvvetli bazlar ile zayıf asitlerin oluşturduğu tuzların sulu çözeltileri baziktir. Baziktuzların sulu çözeltilerinde; OH– iyonlarının sayısı, H+ iyonlarının sayısından fazladır. Kuvvetli baz + Zayıf asit Bazik tuz + Su KOH + HF KF + H2O Kuvvetli asitler ile zayıf bazların oluşturduğu tuzların sulu çözeltileri asidiktir. Asidik tuzların sulu çözeltilerinde; H+ iyonlarının sayısı, OH– iyonlarının sayısından fazladır. Kuvvetli asit + Zayıf baz Asidik tuz + Su HCl + AgOH AgCl + H2O NOT: Tuzlar, asitler ile bazların reaksiyonu sonucu oluşabildiği gibi asitlerin metaller ile reaksiyonu sonucunda oluşabilir. Mg(k) + 2HCl(suda) MgCl2(suda) + H2(g) Metal Asit Tuz Gaz Formülü Yaygın adı Sistematik adı Özellikleri Kullanım alanları NaCI Sofra tuzu Sodyum klorür Nötr tuzdur. Toprakta kaya halinde ve deniz suyunda bulunur. Na2SO4 Sodyum sülfat Na2CO3 Soda külü Sodyum karbonat Suda iyi çözünür. Beyaz renkli bir katıdır. Zehirlidir. Bazik karakterli bir tuzdur. Yağda çözünürse sabun etkisi yapar. Suda iyi çözünür. NaHCO3 Kabartma tozu Sodyum bikarbonat Güherçile Potasyum nitrat Kalsiyum sülfat Yemeklerde tatlandırıcı olarak, besinlerin saklanmasında, salamura yapımında, yollarda buzlanmaya karşı, mandıralarda et ve balığın bozulmasını önlemede, derileri saklamada ve suyu yumuşatmada Cam sanayisinde, boya sanayisinde ve tıpta, deterjan üretiminde, kağıt sanayisinde Sabun, deterjan, ilaç ve yiyecekkatkı maddelerinin hazırlanmasında, suyun arıtılmasında, cam, kağıt, petrol endüstrisinde Çamaşır sodası olarak bilinir. Suda sertlik yapan iyonları karbonatlar halinde çöktürür Gıda endüstrisinde, tıpta mide asidinin fazlalığının yol açtığı sancıları gidermede, yangın söndürücülerde KNO3 CaSO4 CaCO3 NH4CI NH4NO3 (NH4)3PO4 AI2(SO4)3 KAI(SO4)2 .12H2O (NH4)2SO4 Kireç taşı Kalsiyum karbonat Nişadır Amonyum klorür Amonyum nitrat Amonyum fosfat Alüminyum sülfat Şap Potasyum alümina sülfat Amonyum sülfat Suda iyi çözünür. Bazik karakterlidir. Anti asit özelliği gösterir. Beyaz renkli katı bir maddedir. Kuşların dışkısında bolca bulunur. Suda iyi çözünür. Beyaz renkli katı bir maddedir. Bünyesindeki su miktarına göre alçı adını alır. Beyaz renklidir. En saf haline kalsit denir. Doğada mermer, tebeşir formları vardır. Beyaz renkli olup, ısıya karşı dayanıksızdır. Gübre sanayisinde, barut, kibrit yapımında, patlayıcı imalatında Kararsız, suda iyonlaşarak çözünür. Azotlu gübre imalatında, emniyetli patlayıcı imalatında Katı, kararsız beyaz bir maddedir. Gübre sanayisinde Beyaz kristal halindedir. Çözeltisi aşındırıcıdır. Boya sanayisinde, kağıdı tutkallamak için tekstil sanayisinde, mordan (renklendirici) olarak, içme ve atık sularda çöktürme işleminde Tekstil ve deri sanayisinde, ilaç ve gübre üretiminde Suda iyi çözünür. Işığı iyi geçirir. Harç olarak bina yapımında, alçı olarak heykel yapımında İnşaat malzemesinde, metal dökümünde, yağlı boya dolgu maddesinde Metallerin lehimlenmesinde, kuru pil imalatında, yapay gübrelerde Yapay gübrelemede, kimya endüstrisinde, tekstilde, dericilikte, demirin galvanizlenmesinde, proteinlerin çöktürülmesinde https://hasanfirat.com