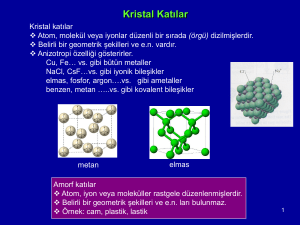
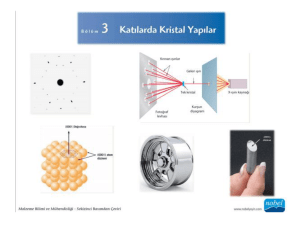
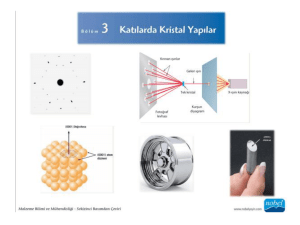
Mineraloji
Yard. Doç.Dr. Davut LAÇİN
davut@istanbul.edu.tr
MİNERALOJİ (Minera +logos)
• Giriş:
Mineralojinin bir bilim dalı olarak ortaya çıkışı çok
eskilere gitmemekle beraber mineraloji ile ilgili sanatların
uygulanması medeniyetin ilk zamanlarına kadar uzanır
(Yaklaşık 5000 yıl).
Örnek: Mezarların boyanması (Mısır medeniyeti), metal
izabeciliği ve süs taşları işletmeciliği gibi.
Bugün doğada varlığı bilinen yaklaşık 2000-2500
civarında mineral bilinmektedir.
Yerkabuğunu teşkil eden kayaçları oluşturan bu
mineralleri, yerkabuğunun geçmişini gösteren elle tutulan
en önemli fiziki bağ olarak ta düşünebiliriz.
Bu
nedenle
mineralojinin
amaçlarından
biri
yerkabuğunun fiziksel, kimyasal ve tarihsel özelliklerini
aydınlatmaktır.
YERKÜRENİN İÇ YAPISI
Şekil . 1
• Dolayısıyla mineraloji terimi ve mineralojinin çalışma
alanı içine giren maddeler doğal olmak zorundadır.
Bu nedenle çimento, çelik ve cam gibi insan eli ile
işlenerek üretilen yapay olan bu maddeler mineralojinin
kapsamı dışında kalırlar.
• Mineral tanımına getirilen diğer bir sınırlama da bu
maddelerin kimyasal element veya bileşiklerden
meydana gelmeleri koşuludur.
Böyle bir sınırlamanın nedeni; kristalen maddelerde
atom veya atom gruplarının kristal içinde belli bir
geometrik düzen içinde yerleşmeleridir. Dolayısı ile böyle
bir madde elektrik yükü yönünden nötr olacak ve belli bir
kimyasal formülü olacaktır.
O HALDE MİNERAL NEDİR
?
• Tanım: Doğada bulunan, kimyasal element veya
bileşiklerden oluşan doğal, homojen ve inorganik olarak
gelişen maddelerdir. Örnek: Pirit (FeS2), hematit (Fe2O3) ,
Civa (Hg) (Sıvı olan tek mineraldir).
Not: Su bir mineral değildir.
Mineraller birkaç istisna dışında katı halin karakteristik
özelliği olan düzenli bir iç yapıya sahiptirler. Koşulların
uygun olması halinde kristal olarak bilinen düzgün yüzeyli
geometrik şekilleri oluştururlar.
O HALDE KRİSTAL NEDİR ?
• Kristalograflara göre; dış görünümleri ne olursa olsun
düzenli bir iç yapısı olan, üç boyutta kesintisiz devamlılık
gösteren bir iç yapıya sahip homojen katılardır.
Kristalografi; Kristal denen katıları inceleyen, bunların iç ve
dış yapıları ile büyümelerini denetleyen kanunları ortaya
çıkarmaya çalışan bilim dalıdır.
NOT: Kristallerdeki yüzeylerin gelişimi büyüme esnasındaki
rastlantılara bağlı olduğu için, yüzeylerin bozulması veya iyi
gelişmemesi kristal için esas olan unsura etki etmez.
•Kristalen; yapıdaki atomları düzenli yerleşmiş demektir.
•Kristal; düzgün yüzeyler ile çevrilmiş geometrik katıdır.
Kristal terimi; gelişmenin mükemmelliğini vurgulamak için
kullanılır;
Euhedral: Kristalen maddede yüzeyler mükemmel gelişme
göstermişlerse,
Subhedral; Yüzeyler kusurlu gelişmişlerse,
Anhedral; Yüzeyler hiç gelişmemişler ise bu ismi alır.
Mikrokristalen; Kristalen maddelerin ancak mikroskop
altında görülebilecek boyutta olanlarına denir.
Kriptokristalen; mikroskop altında bile görülemeyip ancak
X-ışını (XRD) ile saptanabilen boyuttaki kristalen
maddelere denir.
NOT: Gerek doğal ve gerekse yapay maddelerin birçoğu
kristalen olmasına rağmen, bazı maddeler düzenli bir iç
yapı göstermezler.
Amorf madde; düzenli bir iç yapı göstermeyen maddelere
denir.
Mineraloid; düzenli bir iç yapı göstermeyen amorf maddelerin
doğal olarak bulunanlarına denir.
• Diğer disiplinlerle ilişkisine gelince; mineraloji bilimi bir
yandan jeoloji ile diğer yandan ise fizik ve kimya ile çok sıkı
bir işbirliği yapmak zorundadır.
Çünkü arazi çalışmaları sırasında jeolojik yöntemler,
laboratuar çalışmaları sırasında ise fiziksel ve kimyasal
yöntemler kullanılır
KRİSTALLEŞME MEKANİZMASI
Kristal denen katı maddeler, içinde bulundukları 3
ortamdan gelişerek meydana gelirler:
1- Çözeltilerden,
2- Eriyiklerden ve
3- Buharlardan
Bu ortamlarda atomlar düzenli olarak değil tam tersine
genel olarak gelişigüzel bir durum gösterirler.
Ancak sıcaklığın düşmesi, basınç koşullarının değişimi
ve konsantrasyonun yeterli seviyelere ulaşması ile
gelişigüzel hareket eden atomlar birleşerek, katı halin
karakteristik özelliği olan muntazam (düzenli) bir dizilime
geçerler.
1- Çözeltiden kristalleşme mekanizması
Örnek: Su içinde çözülmüş NaCl2’ü incelersek;
Çözeltideki su buharlaşmaya bırakılırsa, birim hacimdeki
çözünmüş tuzun miktarı (Na ve Cl) artar.
Bu halin devam etmesi durumunda; öyle bir noktaya gelinir
ki, artık çözelti, içindeki tuzun tümünü içinde tutamaz ve bir
miktar tuz katılaşarak çöker.
Eğer buharlaşma işlemi yavaş olursa; dış yüzeyleri gelişmiş
kristaller meydana gelir.
Eğer buharlaşma işlemi hızlı olursa; o zaman kristallenme çok
merkezli olarak gelişir ve bunun sonucu olarak çok küçük
kristaller meydana gelir.
2- Eriyikten kristalleşme mekanizması
Eriyiklerden kristalleşme mekanizması çözeltilerden
kristalleşme mekanizması ile benzerlik gösterir.
Örnek: Suyun buza dönüşmesidir.
Gerçekte
su,
buzun
ergimiş
halidir.
Sıcaklık
düşürüldüğünde, su halinde (düzensiz) hareketli olan
moleküller, katı oluşturacak şekilde bir araya gelerek
kristalen (düzenli) maddeyi meydana getirirler.
Magma ile karşılaştırıldığında; benzer durum söz
konusudur.
Şöyle ki; magma içinde gelişigüzel olarak dağılmış halde
hareket eden pek çok element, magma soğuduğunda
birbirine yanaşır ve farklı mineralleri oluşturacak olan kristal
nüvelerini yaparlar. Bu noktadan sonra ilk oluşan
çekirdeklerin (nüve) büyümeleri ile kayaç yapan mineraller
gelişir.
3- Buharlardan kristalleşme mekanizması
İlk iki mekanizmaya nazaran çok daha nadir olmakla
beraber oluşum prensipleri yönünden benzerdir.
Buharın soğuması ile birbirinden uzak olan atomlar yan
yana gelerek sonuçta katı maddeyi oluştururlar.
Örnek; Havadaki su buharından kar taneciklerinin
oluşması.
KRİSTAL İÇ YAPISI
Kristallerde atomları birbirine bağlayan kuvvetler, atomları
geometrik bir düzene (motif = atom topluluğu) sokarlar.
Bu motiflerin şekilleri, yapıya giren atomların;
Cinsine ve
Sayısına bağlıdır.
Bu motiflerin kristal içindeki birbirlerine göre olan
konumlarını ve aralarındaki mesafeleri başka kuvvetler
yönlendirir.
Böylece üç boyutta motiflerin sonsuz tekrarından oluşan
bir yapı meydana gelir.
Örnek: Duvar kağıdında iki boyutta görülen motiflerin
tekrarlanması.
Kristallerde tekrarlanma mesafeleri, üç koordinat ekseni
yönünde birbirinin aynı olabileceği gibi farklı da olabilir.
Koordinat eksenleri birbirine dik olmak zorunda değildirler.
Motifler tek bir nokta ile temsil edilirler ise üç boyutlu
periyodik nokta dizileri meydana gelir ki, bunlara “kristal
yapı veya kristal kafesi” denir.
Bir malzemenin kristal yapısı, 1) kristal kafesi içindeki
atomların dizilişi, 2) kafesin boyutu ve 3) kafesin şekline
bağlı olarak belirlenir.
Birim hücre: Kristal yapının tekrarlanan en küçük hacimsel
birimine “birim hücre” adı verilir.
Birim hücreler yan yana gelerek kristal kafesini oluşturur.
Birim hücre kristal kafesin bütün geometrik özelliklerini
taşıdığı için, birim hücrenin yapı düzeni bilinirse, kristal
kafesin de yapı düzeni kolayca tarif edilebilir.
Kristal kafesi içerisinde atomların bulunduğu yerlere “kafes
noktaları” adı verilir.
Atomlar birim hücrenin köşelerinde, merkezinde, her bir
yüzeyinde veya yüzey kenarlarında bulunur.
Dolayısıyla atomların bulundukları bu yerler kafes
noktaları olarak adlandırılır.
Bir birim hücrenin geometrisi iki farklı parametre ile tarif
edilir: Bu parametreler (Kafes parametreleridir ve birim
hücrenin boyut ve şeklini tarif eder);
1-) x,y,z eksenleri veya birim hücre kenarları arasındaki
α,β ve ȣ açılarıdır.
2-) a,b,c harfleri ile ifade edilen birim hücre kenarlarının
uzunluğudur.
Kafes parametrelerinin farklı kombinasyonları sonucu
ortaya çıkan ve farklı geometrik şekillere sahip 7 kristal
sistemi mevcuttur (Küp, heksagonal, romboedrik v.s).
Yedi kristal sistemine ait toplam 14 farklı kristal kafes
geometrisi (uzay grubu = uzay kafesi = Bravais kafesleri)
ortaya çıkar.
BRAVAİS KAFESLERİ
Tahtaya çizildi
KRİSTALLERİN ÖZELLİKLERİ
Kristaller, üç boyutta birim hücre tekrarlanması ile gelişirler.
Dolayısıyla kristal yüzeyleri bu biçime göre oluşurlar ve aynı
zamanda kristallerin büyüdüğü ortamın özelliğine de bağlıdırlar.
Bu ortam özellikleri;
Basınç,
Sıcaklık,
Kristallerin geliştikleri sıvıların doğası,
Bu sıvıların akış yönleridir.
Örnek: Kübik bir birim hücre 3 boyutta tekrarlanarak bir kristal
oluşturur ve her kenar üzerinde n birim bulundurursa kristal n3
kadar birimden oluşarak daha büyük bir küp şeklini alacaktır.
Aynı mekanizma ile bir birim hücre üç boyutta birbirinden
farklı bir yığılma gösterir ise oluşacak kristallerin şekli farklı
olacaktır.
Örnek:
Eğer bir birim hücre 2 yönde “n” birim, diğer yönde ise “n/5”
birim yığılmış ise ortaya çıkacak kristal “tabuler şekilli” (tablet
şeklinde),
Eğer yalnız 1 yönde “n”, diğer 2 yönde “n/5” birim yığılma
gösterir ise kristal “iğne şekilli” olacaktır.
Ortam koşulları nedeni ile bazı birimlerin yapıda simetrik
olarak yer almayışı sonucu, iç yapıları aynı olmasına
rağmen çok farklı dış şekiller (kristal habitusları) gelişebilir.
Örnek: Küp, oktaeder ve rombusludodekaeder şekilleri için
bu durum tipiktir.
• Kristal içinde bulunan birim hücre boyutlarının
oldukça küçük olması nedeniyle, kristali oluşturan
birim hücrelerin yüzeyler üzerinde meydana
getirdiği basamaklı (girintili-çıkıntılı) yapı gözle
görülemez dolayısıyla kristal yüzeyleri düz görülür.
• İç yapı sınırlı olunca, bu iç yapı ile gelişebilecek
kristal şekli ve bu kristali sınırlayacak yüzey sayısı
fazla değildir. Genellikle çok iyi tanınan birkaç
yüzey ortaya çıkar.
• Bir kristalde yüzeylerin dağılımına bakıldığında;
kristal yüzeyleri kristal kafesi içindeki düğüm
noktalarının en yoğun olduğu yönlerde daha iyi
gelişir.
Şekil. 2: Oktaeder habitusu
Bir yüzeyin bir kristal
üzerinde tekrar gelişebilmesi
bu yüzeyde yer alan düğüm
sayısı ile orantılıdır.
Bu düğümler ne kadar
fazla olur ise o yüzey kristal
üzerinde çokça gözükür.
Şekil: 3: Kristal kafesinde düğüm
nokta pozisyonları